Vi khuẩn lam Chất chuyển hóa thứ cấp là thành phần công nghệ sinh học trong mỹ phẩm chống lão hóa tự nhiên 2
Aug 24, 2022
Xin vui lòng liên hệoscar.xiao@wecistanche.comđể biết thêm thông tin
2.3 Hoạt động sinh học
2.3.1. Hoạt động nhặt rác
Gốc anion superoxide là một gốc tự do sinh lý cực kỳ quan trọng đối với cơ thể con người. Khi có sự sản xuất quá mức ROS này trong quá trình hô hấp hiếu khí, hoặc khi các cơ chế giải độc nội sinh bị lỗi hoặc không đủ, sẽ làm tăng nguy cơ bị tổn thương do oxy hóa với các tác động có hại nghiêm trọng. Theo nghĩa này, việc tìm ra các cơ chế để ức chế các tác động có hại của Oz * là điều quan trọng hàng đầu, không chỉ trong lĩnh vực mỹ phẩm mà còn trong việc xem xét cải thiện và ngăn ngừa nhiều loại bệnh. Hành vi thu gom O2 "của các chất chiết xuất từ vi khuẩn lam được hiển thị trong Hình 1, và các giá trị IC được tóm tắt trong Bảng 6.
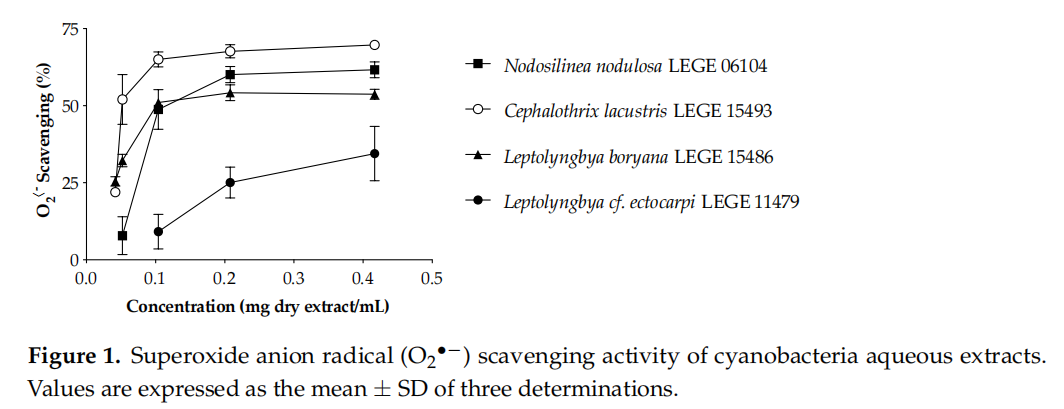

Các chất chiết xuất từ nước có hiệu quả hơn đáng kể trong việc lọc Oz * so với các chất chiết xuất từ axeton (Bảng 6) và thể hiện hoạt tính phụ thuộc vào liều lượng (Hình 1), với các dòng nước ngọt nổi bật hơn các dòng biển. Cephalothorax lacustris LEGE 15493 là chủng hiệu quả nhất, có giá trị ICso thấp nhất (65,5 ug chiết xuất khô / mL, p<0.05), followed="" by="" leptolyngbya="" boryana="" lege="" 15486="" and="" nodosilinea="" nodulosa="" lege="" 06104.="" leptolyngbya="" cf.="" ectocarpi="" lege="" 11479="" was="" the="" only="" strain="" that="" did="" not="" reach="" the="" ic5o="" for="" the="" aqueous="" extract="" (table="" 6).="" on="" the="" other="" hand,="" the="" acetone="" extract="" of="" this="" strain="" was="" the="" most="" effective="" in="" o2*-="">

Vui lòng bấm vào đây để biết thêm
Việc so sánh khả năng chống oxy hóa giữa các vi khuẩn lam khác nhau là một thách thức do các phương pháp áp dụng khác nhau. Morone và các đồng nghiệp đã đánh giá khả năng loại bỏ tận gốc của chiết xuất ethanol (70% v / v) của các chủng vi khuẩn lam khác nhau [26], giá trị ICso thấp nhất là 822,70 ug / mL đối với Phormidium sp.LEGE 02 05292, trong khi không hoạt động được phát hiện đối với Nodosilinea nốt sần LEGE 06102. Lopes và đồng nghiệp đã báo cáo hoạt động thu gom O2 đối với Nodosilinea (Leptolynbbya) Antarctica LEGE13457 và Cuspidothrix Issatschenkoi LEGE 03282 chiết xuất axeton, với giá trị IC25 là 319 và 286 ug / mL, và không có hoạt tính đối với Leptolynbby như sp.LEGE 13412 [27]. Các tác giả cũng báo cáo hiệu quả cao hơn trong các chất chiết xuất từ axeton khi so sánh với các chất chiết xuất từ etanol. Một nghiên cứu khác được thực hiện bởi Amaro và các đồng nghiệp cho thấy giá trị IC50 là 1394 và 826 ug / mL đối với Gloeothece sp. và Scenedesmus seekquus (M 2-1), tương ứng [37]. Các kết quả thu được ở đây đối với chiết xuất axeton có vẻ ít hứa hẹn hơn so với các kết quả đã báo cáo trước đây, mặc dù chúng có cùng mức độ. Mặt khác, các chất chiết xuất từ nước cho thấy một tiềm năng to lớn đáng được khai thác hơn nữa liên quan đến các ứng dụng mỹ phẩm trong lĩnh vực lão hóa da.
2.3.2 Ức chế enzyme
MMPs là một họ các enzym ngoại bào phụ thuộc vào kẽm, có chức năng chính là tái tạo và phân hủy ECM [38], một vật liệu giống như gel cần thiết để giữ các tế bào lại với nhau và cung cấp đường dẫn chất dinh dưỡng và oxy [39]. Những thay đổi trong các thành phần ECM, chẳng hạn như collagen và elastin, gây ra bởi MMPs là cơ sở của tổn thương da và hình thành nếp nhăn [40]. Cùng với những enzym này, liên kết với cấu trúc da và sự hình thành nếp nhăn, một loại enzym khác đóng một vai trò quan trọng trong quá trình lão hóa do hoạt động của nó trong quá trình hình thành hắc tố: tyrosinase. Trong số các yếu tố khác, tiếp xúc với tia UVR gây ra sự tích tụ một lượng melanin bất thường, do tăng sản xuất ROS. Các loài phản ứng này ảnh hưởng đến hoạt động của tế bào hắc tố, làm tăng quá trình chuyển đổi tyrosine thành melanin do quá trình oxy hóa, dẫn đến tăng sắc tố và các mảng da không đều [41].

Cistanche có thể chống lão hóa
Trong quá trình tìm kiếm các giải pháp thay thế tự nhiên cho các thành phần chống lão hóa thương mại, tập trung vào các enzym được đề cập ở trên, hoạt động của các chất chiết xuất từ vi khuẩn lam đã được khám phá (Hình 2). Về HAase, chỉ có ba chủng có thể ức chế enzym này, hoạt động phụ thuộc vào liều lượng: chiết xuất nước của Leptolyngbya cf. ectocarpiLEGE 11479 (IC 50=863 ug / mL), và các chất chiết xuất axeton của Cephalothrix lacustris LEGE 15493 và Nodosilinea nodeulosa LEGE 06104, hai chất sau chỉ đạt IC25 (832 và 995 ug / mL, tương ứng). Mặc dù các giá trị này có vẻ cao, phạm vi hoạt động của chúng tương tự như phạm vi hoạt động của thuốc đối chứng di-natri cromoglicate (DSCG) (IC 50=105 ug / mL). Hơn nữa, điều đáng nói là, đối với nồng độ cao nhất được thử nghiệm (1 mg / mL), Leptolyngbya cf. ectocarpi LEGE 11479 ức chế 80% enzym này (Hình 2), điều này làm cho chiết xuất này có triển vọng như một thành phần mỹ phẩm.
Rất ít nghiên cứu đã báo cáo về tác động tiềm tàng của các hợp chất và chất chiết xuất từ vi khuẩn lam đối với hoạt động của hyaluronidase, và bất kỳ so sánh nào về tiềm năng sinh học của chất chiết xuất cũng phải tính đến rằng sự trao đổi chất của vi khuẩn lam bị thay đổi đáng kể tùy thuộc vào điều kiện canh tác, ảnh hưởng đến thành phần hóa học của chất chiết xuất. Morone và cộng sự [26] đã đánh giá tác dụng của chiết xuất ethanol của nấm Tychonema sp. LEGE 07196 và Cyanobium sp. LEGE 07175 trên hyaluronidase, và tìm thấy hoạt tính ức chế mạnh hơn, với giá trị ICso tương ứng là 182,74 và 208,36 ug / mL. Hoạt tính của chiết xuất etanol cũng đã được báo cáo đối với một phần không hòa tan của Spirulina platensis, với IC5o là 150 ug / mL [42]. Một nghiên cứu khác do Yamaguchi và Koketsu [19] thực hiện cho thấy Nostochopsis lobatus MAC0804NAN tạo ra một lượng lớn polysaccharid có tác dụng ức chế cao (IC 50=7. 18 ug / mL). Người ta cũng báo cáo rằng Arthrospira- peptide dẫn xuất có thể tham gia vào quá trình ức chế hyaluronidase [4]. Kết hợp với nhau, những kết quả này hỗ trợ tiềm năng của các hợp chất và chiết xuất từ vi khuẩn lam làm thành phần chống lão hóa cho các ứng dụng thẩm mỹ.

Xem xét elastase, chỉ các chất chiết xuất từ axeton mới có hoạt tính sinh học thú vị. Leptolyng-bya cf. ectocarpi LEGE 11479 lại hoạt động tích cực nhất (Hình 2), là chủng duy nhất đạt được ICso, với giá trị 391 ug / mL. Nodosilinea nodeulosa LEGE 06104, Cephalothrix lacustris LEGE 15493 và Leptolyngbya boryana LEGE 154 86 chỉ đạt IC25, với các giá trị tương ứng là 126,86 và 99 ug / mL. Đối với hyaluronidase, các chủng sinh vật biển có triển vọng nhất.
Theo hiểu biết tốt nhất của chúng tôi, không có báo cáo nào trước đây về hoạt động ức chế elastase đối với các chủng được khám phá ở đây. Về các chủng khác, người ta đã phát hiện ra rằng Nostoc min đờm tạo ra peptit loại microviridin và nostopeptin, với ICso =1. 3 và 11. 0 ug / mL [44,45]. Microviridin B và Chứa từ Microcystis aeruginosa cũng ức chế elastase một cách hiệu quả, với giá trị ICso là 0. 0 44 và 0,084 ug / mL [46]. Hầu hết các dữ liệu có sẵn liên quan đến sự ức chế elastase tập trung vào các hợp chất cô lập, vì vậy việc so sánh với các chiết xuất từ các chủng của chúng tôi rất khó thực hiện.

Sắc tố da không đồng đều, liên quan đến cả quá trình lão hóa và tiếp xúc với tia cực tím, vẫn là mối quan tâm lớn của dân số già và ngành công nghiệp mỹ phẩm. Phần lớn các nghiên cứu hiện có là sơ sài và sử dụng tyrosinase của nấm làm mô hình enzym, gây khó khăn cho việc dịch kết quả sang môi trường con người, tuy nhiên, enzym này có độ tương đồng cao và tương đồng với tyrosinase của người [47]. Do đó, mô hình enzym tương tự đã được sử dụng ở đây để khám phá tiềm năng của chất chiết xuất từ vi khuẩn lam trong việc ức chế tyrosinase. Đối với elastase, chỉ có chiết xuất axeton mới có thể ức chế tyrosinase. Nodosilinea nốt sần LEGE 06104 là hiệu quả nhất (Hình 2), là chủng duy nhất đạt đến IC # N (989,26 ± 4,3 ug / mL). Dưới đây là Leptolyngbya boryana LEGE 15486, với IC 25=784 78 ± 4,33 ug / mL, và cuối cùng là Leptolyngbya cf.ectocarpi LEGE 11479, với kết quả hứa hẹn nhất được tìm thấy cho các chủng biển.
Morone và các đồng nghiệp [26] trước đây đã khám phá hoạt động của các chất chiết xuất từ ethanolic cyanobacteria trong cùng một mô hình, nhưng không tìm thấy hoạt động nào. Một khía cạnh thú vị của điều này là một trong những chủng được nghiên cứu là Nodosilinea nốt sần LEGE 06102, cho thấy kết quả tốt nhất ở đây, một lần nữa nhấn mạnh tầm quan trọng của dung môi chiết xuất trong việc thu được các chiết xuất có hoạt tính sinh học được nhắm mục tiêu. Đối với các enzym khác được khám phá, các cuộc khảo sát tập trung vào vi khuẩn lam cũng rất khan hiếm tyrosinase. Nghiên cứu do Yabuta và nhóm của ông tiến hành [48], người ta báo cáo rằng chiết xuất nước nóng của Nostochopsis spp. ức chế đáng kể hoạt động của tyrosinase (IC 50=250 ug / mL) Đây là một kết quả rất thú vị, vì nó là kết quả từ một chất chiết xuất trong nước, mà không có hoạt tính nào được tìm thấy trong nghiên cứu này. Các tác giả cho rằng kết quả là do các hợp chất có trọng lượng phân tử thấp được giải phóng từ PBPs bằng cách xử lý nhiệt, cụ thể là một phân tử biline hoạt động như một chất thu hồi gốc peroxyl mạnh. Một nghiên cứu khác đã đánh giá hoạt động ức chế của các chất chiết xuất từ Arthrospira platensis ethanol (IC 50=14, 000 ug / mL) và nước (IC 50 =72, 000 ug / mL), trong đó giá trị được cho là do sự hiện diện của các hợp chất phenolic như axit ferulic và caffeic trong dịch chiết etanol [49].
2.3.3 Bảo vệ UV
Mặc dù ngày càng có nhiều công ty mỹ phẩm tích hợp kem chống nắng vào sản phẩm của họ, vẫn khó thuyết phục người tiêu dùng về lợi ích của việc sử dụng hàng ngày để làm chậm quá trình lão hóa da sớm. Nếu một mặt, việc thoa kem chống nắng hàng ngày là một thói quen ít ăn sâu thì mặt khác, người ta lại lo sợ nhất định việc sử dụng các chất tổng hợp, do những rủi ro liên quan không mong muốn của chúng [50]. Sau đó, nghiên cứu về bảo vệ quang tự nhiên đã tăng lên đáng kể trong vài năm qua, xem xét khả năng phân hủy sinh học và độc tính thấp hơn của chúng, làm cho chúng có lợi hơn cho con người và môi trường. Để khám phá các chất chiết xuất từ vi khuẩn lam trong lĩnh vực này, khả năng hoạt động như kem chống nắng của chúng đã được đánh giá trong ống nghiệm đối với UVR-B, vì đây là bức xạ có hại nhất. Các kết quả được tìm thấy đối với chất chiết xuất từ nước và axeton của vi khuẩn lam được trình bày trong Bảng7.

Về chiết xuất axeton, giá trị hứa hẹn nhất (19,2) được tìm thấy cho Leptolyngbya boryana LEGE 15486, tiếp theo là Leptolyngbya cf.ectocarpiLEGE 1479 (10,7), cả hai đều ở nồng độ thấp nhất được thử nghiệm, 200 ug / mL. Nodosilinea nốt sần LEGE 06104 kém hứa hẹn nhất trong số các chất chiết xuất từ axeton. Trong các chất chiết xuất từ nước, các kết quả hứa hẹn nhất đã thu được đối với nồng độ cao nhất được thử nghiệm, với Leptolyngbya boryana LEGE 15486 và Cephalothrix lacustris LEGE 15493 nổi bật với các giá trị SPF trong ống nghiệm lần lượt là 17,1 và 14,9 (Bảng 7).cistanche life extensionThảo luận về các nghiên cứu trước đây trong lĩnh vực này, Hossain và nhóm của ông [51] đã báo cáo rằng giá trị SPF cho chiết xuất Cephalothrix komarekiana là 2,37. Một nhóm khác nhận thấy rằng SPF của chiết xuất methanol của Aphanizomenon flos-aquae là 4 [52]. Tuy nhiên, thông tin về nồng độ của đoạn trích được các tác giả sử dụng không có sẵn, nên khó có thể so sánh.

Số lượng các chủng vi khuẩn lam được khám phá trong lĩnh vực mỹ phẩm, đặc biệt là về SPF, rất khan hiếm, xét về tiềm năng của các nguồn này. Kết quả nghiên cứu lại được trình bày ở đây chứng minh rằng các loài đang được nghiên cứu có thể là lựa chọn tốt như chất bảo vệ ảnh sinh học và có thể hoạt động như chất thúc đẩy các loại kem chống nắng khác hiện được bán trên thị trường, cho phép giảm nồng độ kem chống nắng tổng hợp trong công thức. Do đó, điều quan trọng là phải tăng cường nghiên cứu về các sinh vật này, đặc biệt là các chất chiết xuất có hoạt tính sinh học của chúng, có chi phí thấp hơn đáng kể, năng suất cao hơn và thu được nhanh hơn các hợp chất phân lập thân thiện với môi trường hơn và hấp dẫn hơn về mặt kinh tế.
2.4. Phân biệt các chất chiết xuất từ vi khuẩn lam bằng phân tích PCA
Việc tìm kiếm các hợp chất hoạt tính sinh học từ các nguồn tự nhiên, có tiềm năng sử dụng làm thành phần trong lĩnh vực mỹ phẩm đã phát triển trong những năm gần đây. Ngoài khả năng ít độc hại hơn và hoàn toàn có thể phân hủy sinh học, các hợp chất có nguồn gốc từ vi khuẩn lam có sẵn từ các nguồn tái tạo và có thể thu được với chi phí thấp trong môi trường được kiểm soát.cistanche nzViệc phân loại các chất chiết xuất hoạt tính sinh học theo thành phần hóa học và hoạt tính sinh học của chúng có thể có giá trị để chỉ ra các mối quan hệ tiềm năng. Về vấn đề này, phân tích thành phần chính (PCA) đã được áp dụng, xem xét thành phần hóa học của chất chiết xuất từ vi khuẩn lam và hoạt tính sinh học của nồng độ cao nhất được thử nghiệm trong mỗi thử nghiệm (Hình 3). Như có thể quan sát, 72,99 phần trăm sự biến đổi có thể được giải thích bởi hai thứ nguyên đầu tiên: PCl chiếm 5 0. 41 phần trăm phương sai, trong khi PC2 chịu trách nhiệm 22,58 phần trăm. Ba nhóm được phân biệt (Hình 3A ): Gl, liên quan đến chiết xuất nước Leptolyngbya cf.exocarp LEGE 11479; G2, liên quan đến các chất chiết xuất từ nước Cephalothrix lacustris LEGE 15493, Leptolyngbya boryama LEGE 15486 và Nodosilinea nodeulosa LEGE 06104; và G3, liên quan đến tất cả các dịch chiết axeton. Theo Hình 3B, Gl khác biệt về mặt hóa học so với các mẫu khác do hàm lượng PE; Chất chiết xuất từ nước Cephalothrix lacustris LEGE 15493, Leptolyngbya boryana LEGE 15486 và Nodosilinea Nodosilinea LEGE 06104 được nhóm theo hàm lượng của chúng trong PC, APC và tổng số protein (G2), trong khi tất cả các chất chiết xuất axeton được tìm thấy trong cùng một nhóm (G3) do đối với hàm lượng của chúng trong carotenoid, và chất diệp lục a và các dẫn xuất của nó. Các hợp chất nằm ngoài các hoạt động của enzym được hiển thị, với các mặt phẳng được tạo thành với trục dương PCl (Hình 3B). Có thể quan sát thấy rằng các mẫu có hàm lượng cao hơn trong chất diệp lục a và carotenoit có liên quan chặt chẽ với sự ức chế elastase a và tyrosinase. Điều này được chứng minh bằng mối tương quan thuận chặt chẽ giữa carotenoid và elastase (0,725, p<0.01) and="" tyrosinase=""><0.01) inhibition,="" with="" similar="" observations="" between="" chlorophyll="" a="" and="" the="" same="" enzymes=""><0.01 and=""><0.05,respectively). on="" the="" other="" hand,="" hyaluronidase="" inhibition="" is="" more="" correlated="" vvith="" pe="" content="" (figure="" 3b),="" with="" a="" significant="" positive="" correlation="" between="" the="" values=""><0.01).the compounds="" responsible="" for="" the="" radical="" scavenging="" activity="" of="" the="" extracts="" are="" displayed,="" with="" the="" planes="" formed="" with="" the="" pcl="" negative="" axis.="" the="" closest="" correlation="" is="" observed="" for="" tpc=""><0.05); other="" compounds="" such="" as="" total="" proteins,="" pc,and="" apc="" also="" contribute="" to="" the="" activity,="" although="" to="" a="" lower="" extent="" (figure="" 3b).regarding="" the="" spf,="" there="" is="" a="" close="" correlation="" between="" the="" activity="" of="" the="" extracts="" and="" their="" pbp="" content,mainly="" apc=""><0.01)and pc="" (0.838,="" p="" <="" 0.01),="" which="" points="" to="" these="" compounds="" as="" predominantly="" responsible="" for="" blocking="" uv-b="" radiation.="" the="" total="" protein="" content="" also="" contributed="" to="" this="" biological="" activity="" (0.670,=""><0.01), with="" the="" lowest="" contribution="" being="" observed="" for="" pe="" (0.210,p="">0. 05). Nói chung, phân tích PCA cho phép nhóm các chất chiết xuất theo các hoạt động sinh học được hiển thị trong lĩnh vực lão hóa da, dẫn đến kết luận rằng chất chiết xuất axeton có hiệu quả hơn trong việc ức chế các enzym gây ra sự thoái hóa của ma trận da và mất cấu trúc da, trong khi chiết xuất từ nước có hiệu quả hơn trong việc loại bỏ các gốc tự do và bảo vệ da khỏi các tác động có hại của bức xạ UV.
Theo những gì chúng tôi được biết, đây là lần đầu tiên mối quan hệ giữa thành phần hóa học và hoạt tính sinh học của các chất chiết xuất từ các chủng vi khuẩn lam này được thiết lập.
3. vật liệu và phương pháp
3.1. Sản xuất sinh khối vi khuẩn lam
Bốn chủng vi khuẩn lam dạng sợi, Cephalothrix lacustris LEGE 15493 và Lep-tolyngbya boryana LEGE 15486, từ các hệ sinh thái nước ngọt Brazil và Leptolyngbya cf. ectocarpi LEGE 11479 và Nodosilinea nodeulosa LEGE 06104, từ các hệ sinh thái biển của Bồ Đào Nha, đã được sử dụng trong nghiên cứu này. Các chủng này đã được duy trì trong Bộ sưu tập Công nghệ Sinh học và Nuôi cấy Độc tố Sinh thái Xanh (LEGE CC) tại Trung tâm Nghiên cứu Môi trường và Biển liên ngành (CIIMAR). điều kiện kiểm soát, tuần tự mở rộng quy mô lên đến 4 L. Các chủng được nuôi trong môi trường Z8 [53], bổ sung 10 ug / L vitamin B12 và 25g / LNaCl cho các chủng biển. Việc nuôi cấy được duy trì ở 25 độ, với cường độ ánh sáng 10 umol photon m -2 s -4 và với chu kỳ quang học là 14 giờ sáng: 10 giờ tối. Sinh khối tươi được thu thập sau 120 hoặc 150 ngày tăng trưởng (tùy thuộc vào chủng) thông qua lọc, và đông lạnh, đông khô và được bảo quản ở -20 độ cho đến khi chuẩn bị chiết xuất.
3.2.Chuẩn bị chi tiết
Hai chất chiết xuất khác nhau được chuẩn bị tuần tự từ mỗi chủng: axeton và dung dịch nước. Đầu tiên, chiết xuất axeton được chuẩn bị, sử dụng 2g sinh khối khô. Sinh khối được lơ lửng trong axeton và chiết xuất trong 10 phút trong bể siêu âm (Fisherbrand [FB15053, Loughborough, Vương quốc Anh). Sau khi chiết bằng axeton, phần mẫu thu được được để khô trong tủ hút, và sau đó chiết bằng 70 mL nước cất, theo quy trình tương tự. Các mảnh vụn tế bào được loại bỏ bằng cách ly tâm ở 10, 00 ×× g Gs trong 5 phút ở 4 độ, trong máy ly tâm siêu nhỏ HERAEUS MegafugeTM 16R (Thermo ScientificTM, Waltham, MA, USA). Presure (BUCHIR -210 Thiết bị bay hơi quay) (chiết xuất axeton), hoặc đông lạnh và đông khô (chiết xuất dạng nước). Việc chiết với phần nổi tương ứng được lặp lại 3 lần. Các chất chiết khô được giữ ở -20 độ cho đến khi phân tích thêm về hóa học và sinh học.
3.3 Thử nghiệm bán hàng
3.3.1 Văn hóa tế bào
Tế bào sừng ở người HaCAT (ATCC), nguyên bào sợi của chuột 3L1 (ATCC) và tế bào nội mô ở người hCMEC (do Tiến sĩ POCouraud (INSERM) cung cấp) đã được sử dụng để đánh giá cytotox-icity. Các dòng tế bào được nuôi cấy trong Môi trường Đại bàng Biến đổi của Dulbecco (DMEM GlutaMAXTM, Gibco, Glasgow, Vương quốc Anh), được bổ sung 1 0 phần trăm (v) huyết thanh bò thai (Gibco), 1 phần trăm penicillin-streptomycin (Pen-Strep 100 IU / mL và 10 mg / mL, tương ứng) (Gibco) và 0,1% Amphotericin B (Gibco). Các xét nghiệm và bảo dưỡng tế bào được thực hiện ở 37 độ trong môi trường làm ẩm 5% CO2, và môi trường nuôi cấy được thay mới hai ngày một lần. Tại 80-90 phần trăm tế bào hợp lưu, các tế bào kết dính được rửa bằng nước muối đệm photphat (PBS, Gibco), tách ra bằng enzym TrypLEX express (1 ×) (Gibco), được đưa qua để bảo dưỡng và được gieo mầm cho các xét nghiệm theo kế hoạch.
3.3.2 Độc tính — Thử nghiệm MTT
Khả năng tồn tại của tế bào được đánh giá bằng cách giảm {{0}} (4, 5- dimethylthiazole -2- yl) -2, 5- diphenyltetrazolium bromide (MTI, Xét nghiệm Sigma-Aldrich, Đức), như đã được chuyển trước đây [26]. Tất cả các dòng tế bào (tế bào nội mô, nguyên bào sợi và tế bào sừng) được cấy vào 96- đĩa giếng, với mật độ lần lượt là 1,0 × 10 tế bào / mL, 3,3 × 104 tế bào / mL và 2,5 × 104cells / mL.kích thước dương vật cistancheSau 24 giờ kết dính tế bào, môi trường nuôi cấy được lấy ra, và các tế bào được tiếp xúc trong 24 và 48 giờ với môi trường tươi có chứa các chiết xuất vi khuẩn lam khác nhau ở năm nồng độ nối tiếp, từ 12,5 đến 200 ug / mL. Đối với dịch chiết axeton, dung dịch gốc được chuẩn bị trong dimethyl sulfoxide (DMSO) (Gibco), và được pha loãng với DMEM trước khi tế bào tiếp xúc để nồng độ DMSO tối đa không vượt quá 1 phần trăm. Chất chiết xuất từ nước được chuẩn bị trong PBS và được pha loãng với DMEM trước khi kiểm tra tế bào. Kiểm soát tiêu cực là PBS và kiểm soát tế bào chết là DMSO 20%. Sau khi ủ, xét nghiệm độc tính tế bào MIT được thực hiện. Một cách ngắn gọn, 20 μL dung dịch MTT được thêm vào mỗi giếng và ủ ở 37 độ trong 3 giờ. Sau khi ủ, môi trường được loại bỏ cẩn thận và các muối formazan có màu tím được hòa tan trong DMSO. Độ hấp thụ được đọc ở bước sóng 550 nm bằng đầu đọc vi tấm đa dò Synergy HT (Biorek, Bad Friedrichshall, Đức) vận hành bằng phần mềm GEN51M. Thử nghiệm được thực hiện trong bốn lần và được tính trung bình. Để có độ tái lập, mỗi phép thử được lặp lại độc lập ít nhất ba lần. Độc tính tế bào được biểu thị bằng phần trăm khả năng sống sót của tế bào, xem xét khả năng sống sót 100 phần trăm trong việc kiểm soát dung môi.
3.4. Hồ sơ hóa học của các chất chiết xuất từ vi khuẩn lam
3.4.1 Tổng hàm lượng phenolic (TPC)
Để xác định TPC của các chất chiết xuất, một thử nghiệm so màu đã được sử dụng, dựa trên phương pháp Folin-Ciocalteu [54] với những sửa đổi nhỏ. Các chất chiết xuất axeton được hòa tan trong DMSO, và các chất chiết xuất dạng nước trong nước. Tóm lại, 25 μL của mỗi dịch chiết (1 0 mg / mL) được trộn hoàn toàn với 25 μL thuốc thử Folin-Ciocalteu (Sigma-Aldrich) 2 0 {{2 0}} μL dung dịch NagCO3 và 500 μL nước khử ion. Đối với mẫu trắng, thuốc thử Folin-Ciocalteu được thay thế bằng nước khử ion. Độ hấp thụ của sản phẩm màu được tạo thành được đo ở bước sóng 725 nm, sử dụng đầu đọc vi tấm đa phát hiện Synergy HT (Biotek, Bad Friedrichshall, Đức) hoạt động thông qua phần mềm GEN51M. Các đường cong chuẩn để định lượng TPC thu được khi sử dụng bảy nồng độ axit gallic (GA) (0,025 đến 0,5 mg / mL), được chuẩn bị trong cùng dung môi với chất chiết xuất được thử nghiệm (y =2. 097x + 0,01560 R² {{ 22}}. 9989, đối với axeton và y =2. 204x + 0,01401, R 2=0. 9982, đối với nước, trong đó "y" là độ hấp thụ và "x" là nồng độ) . Ba phép xác định độc lập được thực hiện trùng lặp. Tổng hàm lượng phenol được biểu thị bằng đơn vị đương lượng GA (GAE) trên mỗi mg dịch chiết khô.
3.4.2 Tổng số Protein
Tổng nồng độ protein được xác định bằng cách sử dụng bộ xét nghiệm protein BCA (# 23227, Thermo-Scientific). Các chất chiết xuất từ nước được chuẩn bị trong nước, trong khi các vùng ngoại vi axeton được chuẩn bị trong DMSO. Tóm lại, trong một đĩa giếng 96-, 25 uL của mỗi dịch chiết (1 mg / mL) được trộn với 200 μL của thuốc thử làm việc. Độ hấp thụ được đo ở bước sóng 562 nm, sử dụng đầu đọc vi tấm đa phát hiện Synergy HT (Biotek, Bad Friedrichshall, Ger-many) hoạt động thông qua phần mềm GEN5IM. Đường cong chuẩn (y =-126. 87x3 + 547,73. 353 -10. 017; R 2=0. 999 và y =162. 87x 3-248. 51x² + 932,13x -11. 715; R 2=0. 99, trong đó "y" là độ hấp thụ và "x" là nồng độ) thu được cho mỗi chiết xuất, sử dụng chín nồng độ albumin (BSA) (25 đến 2000 ug / mL) để định lượng protein. Ba thí nghiệm độc lập được thực hiện ba lần. Tổng hàm lượng protein được biểu thị bằng đơn vị đương lượng albumin huyết thanh bò (BSA) trên mỗi mg dịch chiết khô.
3.4.3.
Các chất màu có trong cả chiết xuất dung dịch nước và axeton đều được định lượng bằng phương pháp đo nhiệt độ cụ thể. Chất diệp lục a và các dẫn xuất của nó được định lượng bằng cách sử dụng đường chuẩn thu được với chất chuẩn thương mại (Sigma-Aldrich): y =8. 0 791x -0. 0 {{19} } 22 (R 2=0. 996), trong đó "y" là độ hấp thụ và "x" là nồng độ. Tổng số carotenoid được định lượng dưới dạng -carotene (Sigma-Aldrich), thông qua đường chuẩn của nó (y =17. 133x + 0,0099; R² =0. 990, trong đó "y" là độ hấp thụ và "x" là nồng độ). Tổng nồng độ carotenoid được biểu thị bằng ug -carotene trên mỗi mg chiết xuất khô. Các đường cong hiệu chuẩn cho cả hai chất chuẩn thu được khi sử dụng năm nồng độ khác nhau (0,001 đến 0,025 mg / mL). đầu đọc vi tấm đa dò Synergy HT (Biotek, Bad Friedrichshall, Đức) hoạt động thông qua phần mềm GEN5TM.
Hàm lượng PBP được xác định bằng phương pháp đo quang phổ bằng cách đo độ hấp thụ của các chất chiết xuất trong nước ở các bước sóng khác nhau (562,615 và 645 nm), và áp dụng các công thức tương ứng, như đã được Pagels et al mô tả trước đây. [34]: Chất chiết xuất từ nước được trộn lại đến nồng độ cuối cùng là 0. 5 mg / mL. Thử nghiệm được thực hiện ba lần, và kết quả được biểu thị bằng ug / mg dịch chiết khô. 3.5. Hoạt động sinh học
3.5.1.Superoxide Anion Radical (O2 * -)
Theo Barbosa và các đồng nghiệp [55], thử nghiệm thu dọn gốc tự do của Oz * - được thực hiện để đánh giá tiềm năng chống oxy hóa của các chất chiết xuất từ vi khuẩn lam, với những sửa đổi nhỏ. Các chất chiết xuất từ nước được chuẩn bị trong nước, trong khi chất chiết xuất axeton được chuẩn bị trong DMSO. Năm dung dịch pha loãng nối tiếp được chuẩn bị cho mỗi dịch chiết và được thử nghiệm để đánh giá hoạt động của các chất chiết xuất và các giá trị IC. Tất cả các thuốc thử được hòa tan trong dung dịch đệm phosphat (19 uM, pH7,4). Một thể tích 50μL của mỗi độ pha loãng được trộn với 50 uL của dung dịch 166 uM -nicotinamit adenin dinucleotit dạng khử (NADH) và 150 uL của 43 uM nitrotetrazolium clorua xanh (NBT) trong một đĩa giếng 96-. Sau khi bổ sung 50 μL của 2,7 μM phenazine methosulphate (PMS), hoạt động thu gom tận gốc của các mẫu được theo dõi bằng đầu đọc vi tấm đa phát hiện Synergy HT (Biotek, Bad Friedrichshall, Đức) hoạt động thông qua phần mềm GEN51M, trong chức năng động học, ở nhiệt độ phòng trong 2 phút ở bước sóng 562 nm. Ba thử nghiệm độc lập được thực hiện trong ba lần. GA được sử dụng như một đối chứng tích cực. Kết quả được biểu thị bằng tỷ lệ phần trăm loại bỏ triệt để so với đối chứng không được xử lý. Kết quả đối với các giá trị IC tính toán được biểu thị bằng giá trị trung bình ± SD (ug / mL) của ít nhất ba phép thử độc lập được thực hiện lặp lại. Các giá trị IC và đường cong đáp ứng liều tương ứng được tính toán bằng phần mềm Graphpad Prism @ (San Diego, CA, USA; phiên bản 9, dành cho MacOS).
3.5.2 Ức chế Hyaluronidase
Thử nghiệm ức chế hyaluronidase được sửa đổi một chút so với thử nghiệm được đề xuất bởi Ferreres và cộng sự. 【56】. Tóm lại, 25 μL của mỗi chiết xuất (9mg / mL), 175 μL axit hyaluronic (HA) (0. 7 mg / mL), và 25 μL hyaluronidase (HAase) (9 0 {{ 14}} U / mL trong NaCl0,9 phần trăm) được trộn trong một ống phản ứng. Chất chiết xuất từ nước được chuẩn bị trong nước, và chất chiết xuất axeton được chuẩn bị trong DMSO. Sau 30 phút ủ ở 37 độ, phản ứng dừng lại bằng cách thêm 25 μL di-natri tetraborat (0,8 M vào nước), tiếp theo là ủ 3 phút ở 90 độ trong nồi cách thủy. Các ống phản ứng được làm lạnh đến nhiệt độ phòng trước khi thêm 375 uL dung dịch DMAB [4- (Dimethylamino) benzaldehyde] vào. Sau 20 phút ủ ở 37 độ, độ hấp thụ của sản phẩm màu được tạo thành được đo ở bước sóng 560 nm, trong thiết bị đọc vi tấm đa phát hiện Synergy, HT (Biotek, Bad Friedrichshall, Đức) hoạt động thông qua phần mềm GEN5IM. Việc kiểm soát âm tính được thực hiện trong trường hợp không có chiết xuất. Disodium cromoglycate (DSCG) được sử dụng như một đối chứng tích cực.
Ba thử nghiệm độc lập được thực hiện trong ba lần, và kết quả được biểu thị bằng tỷ lệ phần trăm ức chế enzym so với đối chứng không được xử lý.
3.5.3 Ức chế men gan
Thử nghiệm ức chế elastase tuyến tụy ở heo được thực hiện theo Mota và cộng sự [57] với những sửa đổi nhỏ. Chất chiết xuất từ nước được chuẩn bị trong nước, trong khi chất chiết xuất axeton được chuẩn bị trong DMSO. Một cách ngắn gọn, trong một 96- đĩa giếng, 5 0 μL dịch chiết được trộn với 90 uL dung dịch đệm HEPES (0,1 M), 10 uL chất nền p-nitroanilide N-succinyl-Ala-Ala-Ala (100 uM), 70 uL dung dịch đệm axetat (200 mM) và 30 μL elastase (1 U / mL) Đĩa được ủ ở 37 độ cho 10 phút và độ hấp thụ của sản phẩm phản ứng được đo ở bước sóng 405 nm, trong đầu đọc vi tấm đa phát hiện Synergy HT (Biotek, Bad Friedrichshall, Đức) vận hành qua GEN51M. Đối chứng âm tính được thực hiện trong trường hợp không có chiết xuất, và axit ascorbic được sử dụng làm đối chứng dương tính.bột cistancheBa thử nghiệm độc lập được thực hiện trong ba lần. Kết quả được biểu thị bằng tỷ lệ phần trăm ức chế enzym so với đối chứng không được xử lý.
3.5.4 Ức chế menrosinase
Thử nghiệm ức chế tyrosinase được thực hiện theo Adhikari và cộng sự. [58] với những sửa đổi nhỏ. Tóm lại, trong một 96- đĩa giếng, 2 0 μL của mỗi dịch chiết được trộn với 1 0 0 μL tyrosinase (30 U / mL trong dung dịch đệm phốt phát). Chất chiết xuất từ nước được chuẩn bị trong nước, trong khi chất chiết xuất axeton được chuẩn bị trong DMSO. Hỗn hợp được ủ ở 30 độ trong 8 phút. Sau đó, 80 μL L-DOPA (L -3, 4- dung dịch dihydroxyphenylalanin) 2,5 mM trong dung dịch đệm photphat) được thêm vào và ngay lập tức sự hấp thụ (T0, độ hấp thụ tại thời điểm "không") được đo bằng đầu đọc vi tấm đa dò Synergy HT (Biotek, Bad Friedrichshall, Đức) hoạt động thông qua phần mềm GEN5TM, ở bước sóng 475 nm. Việc xác định độ hấp thụ ở T0 (trước khi sản phẩm phản ứng được hình thành) cho phép loại bỏ các nhiễu có thể có do màu sắc tự nhiên của các chất chiết được nghiên cứu. Sau 8 phút ủ ở 30 độ, độ hấp thụ được đo một lần nữa (T8). {21}} T0) tương ứng với 100 phần trăm hoạt động của enzym. Đối chứng âm tính được thực hiện trong trường hợp không có chiết xuất, và axit kojic được sử dụng làm đối chứng dương tính. Ba thử nghiệm độc lập được thực hiện trong ba lần. Kết quả được biểu thị bằng tỷ lệ phần trăm ức chế enzym so với đối chứng không được xử lý.
3.5.5 Hệ số bảo vệ chống nắng (SPF)
Theo Rohr và cộng sự [59], hệ số bảo vệ chống nắng trong ống nghiệm được xác định với những sửa đổi nhỏ. Các chất chiết xuất từ nước được chuẩn bị trong nước, trong khi các chất chiết xuất từ axeton được chuẩn bị trong axeton. Một cách ngắn gọn, độ hấp thụ 2mL của mỗi dịch chiết (20 và 1000 ug / mL), được đo trong máy quang phổ (từ 290 đến 320 nm, 5 trong 5 nm). SPF được tính bằng công thức do Mansur [60] đề xuất: trong đó EE (A) là phổ hiệu ứng ban đỏ, I (A) là phổ cường độ mặt trời, Abs (λ) là độ hấp thụ của chiết xuất và CF là hiệu chỉnh Yếu tố (28) được xác định bằng cách sử dụng kem chống nắng thương mại có giá trị SFP đã biết là 30.
3.6 Phân tích thống kê
Phân tích thống kê được thực hiện bằng phần mềm thống kê SPSS của IBM (phiên bản 23. 0 dành cho macOS, IBM Corporation, New York, NY, USA, 2015). Dữ liệu được phân tích về tính chuẩn mực và tính đồng nhất của các phương sai bởi Kolmogorov-Smirnov và Leven's các bài kiểm tra, sau đó được gửi tới ANOVA một chiều bằng cách sử dụng HSD của Tukey (sự khác biệt đáng kể trung thực) như một bài kiểm tra sau tài liệu hoặc cho một bài kiểm tra t không ghép nối. Một thử nghiệm tương quan Pearson được sử dụng để so sánh dữ liệu biểu hiện chuẩn hóa giữa các cấu hình hóa học và hoạt động sinh học của các chất chiết xuất từ vi khuẩn lam.
3.7.Phân tích thành phần đô thị (PCA)
PCA được sử dụng để biến đổi một số biến có khả năng tương quan thành một số biến tương đối độc lập, có thể được xếp hạng dựa trên đóng góp của chúng trong việc giải thích sự biến đổi của toàn bộ tập dữ liệu [61]. Có thể xác định thành công các thành phần tương đối quan trọng của các mẫu chiều cao. Dữ liệu chiều cao ban đầu có thể được ánh xạ vào không gian có chiều thấp hơn, và do đó độ phức tạp của bài toán phân loại mẫu chiều cao được giảm đáng kể [62]. Đối với nghiên cứu này, nhận dạng mẫu dựa trên PCA đã được thực hiện bằng phần mềm thống kê SPSS của IBM (phiên bản 23. 0 dành cho macOS, IBM Corporation, New York, NY, USA, 2015). Ma trận dữ liệu bao gồm các chất chuyển hóa có trong dịch chiết nước và axeton của bốn chủng vi khuẩn lam, và hoạt động của chúng ở nồng độ cao nhất đã được kiểm tra.
4.Kết luận
Hoạt tính sinh học được hiển thị bởi các chất chiết xuất từ vi khuẩn lam được phân tích ở đây được chứng minh là có mối tương quan rõ ràng. Theo sự hiện diện của PBP hoạt tính sinh học, các chất chiết xuất từ nước là hiệu quả nhất để bảo vệ tia cực tím, cùng với khả năng loại bỏ tận gốc của chúng, cho thấy chúng là thành phần hứa hẹn được sử dụng trong các công thức chống lão hóa nhằm ngăn ngừa lão hóa da trầm trọng hơn do các yếu tố bên ngoài. Mặt khác, chiết xuất axeton tỏ ra hiệu quả hơn trong việc ức chế hoạt động của các enzym gây ra sự suy thoái của nền da và mất cấu trúc da, do đó phù hợp hơn với quá trình lão hóa da do tuổi tác.chiết xuất cistanche salsaSơ đồ chiết xuất tuần tự mà chúng tôi đề xuất có thể tỏ ra thuận lợi, cho phép thu được các chất chiết xuất có hoạt tính sinh học khác nhau về mặt hóa học thông qua việc kiếm tiền từ sinh khối vi khuẩn lam, làm cho quy trình bền vững hơn và hấp dẫn hơn về mặt kinh tế. Nhìn chung, chất chiết xuất từ vi khuẩn lam đã được chứng minh là xứng đáng để khai thác hơn nữa trong lĩnh vực lão hóa da, nhắm mục tiêu tìm kiếm các thành phần tự nhiên, an toàn và bền vững cho các công thức mỹ phẩm.
Bài viết này được trích từ Mar. Drugs 2022, 20, 183. https://doi.org/10.3390/md20030183 https://www.mdpi.com/journal/marinedrugs






