Xóa Alox15 cải thiện rối loạn chức năng thận và ức chế fbrosis bằng cách tăng PGD2 trong thận
Mar 12, 2022

CISTANCHE SẼ CẢI THIỆN NHIỄM TRÙNG THẬN/THẬN
Giới thiệu
Axit béo không bão hòa đa (PUFA) và các chất chuyển hóa của chúng có liên quan đến viêm và độ phân giải của nó ở một số cơ quan [1]. Oxylipin, được sản xuất bởi quá trình oxy hóa PUFA, rất quan trọng đối với hoạt động sinh học của PUFA với tư cách là chất trung gian lipid [1, 2]. Sinh tổng hợp oxylipin được trung gian bởi một số enzyme, chẳng hạn như lipoxygenase (LOX), cyclooxygenase (COX) và cytochrome P450 (CYP) [3]. Các enzyme này tạo ra một số chất chuyển hóa lipid, chẳng hạn như prostaglandin, leukotrienes và lipoxin, tất cả đều liên quan nhiều đến việc điều chỉnh viêm [1, 4]. Ví dụ, ALOX15, một phân nhóm chính của LOX, có khía cạnh kép của các đặc tính tiền viêm và chống gây ô nhiễm thông qua các chất chuyển hóa của nó [5]: ALOX15 được thể hiện cao trong bạch cầu ái toan, tế bào biểu mô phế quản-phế nang và đại thực bào phế nang trong điều kiện không nhiễm trùng [5, 6] và thúc đẩy mức độ nghiêm trọng của hen suyễn [7], tổn thương phổi [8] và suy tim [9], trong khi nó chống lại tình trạng viêm trong viêm khớp [10] và thiếu máu cục bộ [11]. Ngoài ra, các chất trung gian lipid và các enzyme của chúng ảnh hưởng đến xơ hóa cơ quan cũng như viêm. Các chất trung gian lipid cụ thể có liên quan đến cơ chế bệnh sinh của xơ hóa phổi [12], gan [13] và tim [14]. Tương tự, ALOX15 nói trên cũng có liên quan đến cơ chế bệnh sinh của xơ hóa như xơ hóa da [15].
Một trong những bệnh mãn tính phổ biến là mãn tính bệnh thận(CKD), ảnh hưởng đến khoảng 8–16% dân số nói chung trong tất cả các giai đoạn cộng lại [16]. Mặc dù sinh bệnh học CKD rất phức tạp và thay đổi tùy thuộc vào bệnh tiềm ẩn,thậnmô thường trở nên rối loạn chức năng, dẫn đến giai đoạn cuốisuy thậngây ra bởi viêm mãn tính và xơ hóa sau đó [17]. Như đã đề cập, các chất trung gian lipid có nguồn gốc từ PUFA có liên quan chặt chẽ đến tình trạng viêm và xơ hóa dẫn đến của nó. Ví dụ, lipoxin và resolvin ức chế xơ hóa thận [18, 19], nhưng những hiệu quả này chưa được kiểm tra trong mô hình CKD bị suy yếuchức năng thận.Hơn nữa, hồ sơ lipidomic toàn diện trong CKDthậncác mô vẫn chưa được báo cáo. Do đó, vai trò của các enzyme chuyển hóa lipid và các sản phẩm của chúng trong sinh bệnh học CKD vẫn chưa được hiểu rõNghiên cứu này nhằm làm sáng tỏ sự tham gia của các enzyme chuyển hóa axit béo và các sản phẩm của chúng trongThậnsuy giảm 5/6 chuột mô hình CKD nephrectomized (Nx). Nghiên cứu này tiết lộ rằng cả mức độ phiên mã và biểu hiện protein của Alox15 đều tăng lên trong CKDthận, và chuột Alox15−/− cho thấy sự cải thiệnthậnrối loạn chức năng và xơ hóa trong mô hình CKD. Hơn nữa, PGD2, là chất chuyển hóa lipid tăng trong CKDthậnchuột Alox15−/−, ức chế quá trình chuyển tiếp biểu mô-trung mô (EMT) trong các tế bào nuôi cấy hình ống gần. Do đó, ức chế Alox15 và /hoặc quản lý PGD2 có thể là một mục tiêu điều trị mới của CKD và xơ hóa.
Từ khoá:bệnh thận mãn tính; Lipoxygenase; ALOX15; Lipidomics trung gian; Axit béo không bão hòa đa; Thận

CISTANCHE SẼ CẢI THIỆN CHỨC NĂNG THẬN / THẬN
Vật liệu và phương pháp
Động vật và thí nghiệmNghiên cứu này đã sử dụng chuột C57BL /6 J đực 8 tuần tuổi (CLEA Nhật Bản), đã được thích nghi trong 1 tuần trước khi tất cả các thí nghiệm được thực hiện. Hơn nữa, chuột Alox15−/− được tạo ra trong nền C57BL/6 J (Phòng thí nghiệm Jackson), và mô hình 5/6 Nx được thiết lập theo một nghiên cứu trước đó [20]. Chúng tôi đã thu thập các mẫu máu để đánh giáchức năng thậnvàthậncác mẫu mô để thấm miễn dịch và phản ứng chuỗi polymerase ở 8 tuần sau 5/6 Nx, và để phân tích mô học ở 40 tuần sau 5/6 Nx. Tất cả các thí nghiệm đều tuân thủ các hướng dẫn nghiên cứu trên động vật của TMDU và Ủy ban Chăm sóc và Sử dụng Động vật của TMDU đã phê duyệt giao thức nghiên cứu của chúng tôi (số phê duyệt: A2019-117C4).
Lipidomics hòa giải dựa trên LC – MS / MSChúng tôi đã tiến hành phân tích LC-MS / MS như được mô tả trước đây [21, 22]. Chi tiết của thủ tục được mô tả trong Phương pháp bổ sung,Các phương pháp thí nghiệm khácChúng tôi đã mô tả các phương pháp thử nghiệm khác trong Phương pháp bổ sung.
Kết quả
Nồng độ mRNA của Alox15 đã tăng ở 5/6 Nx thậnNhững thay đổi định lượng của các enzyme oxylipin trong CKDthậnđã được điều tra bằng cách áp dụng C57BL / 6 con chuột vào hoạt động giả hoặc 5/6 Nx như được mô tả trước đây [20]. Để phân tích sự biểu hiện của các enzyme oxylipin chính biểu hiện trong thận (Alox15, Alox5, Ptgs1 (COX1), Ptgs2 (COX2), Cyp4a12 và Cyp2c44) [23, 24], chúng tôi đã chiết xuấtthậnMẫu. Trong số các enzyme, Alox15 trong 5/6 Nxthậncó mức mRNA tăng đáng kể (P = 0,0004) so với mức giả mạothận(Hình 1). Ngược lại, nồng độ mRNA của các enzyme chính khác không thay đổi đáng kể trong mô hình CKD này.
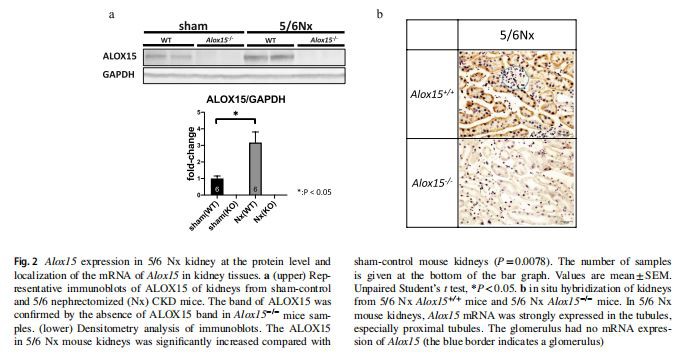
Nồng độ protein của Alox15 đã được tăng lên trong các tế bào ống gần thậnTrong 5/6 Nxthận, nồng độ protein ALOX15 cũng tăng lên (P = 0,0078), như mong đợi bởi mức phiên mã tăng (Hình 2a). Để xác định loại tế bào nào đã làm tăng mức protein Alox15 trong CKDthậnchúng tôi đã kiểm tra nội địa hóa của Alox15 mRNA bằng cách lai tạo tại chỗ. Lai tạo tại chỗ với mRNA cho thấy mức độ biểu hiện cao của Alox15 đã được bản địa hóa tạiThậncác tế bào hình ống trong mô hình 5/6 Nx, nhưng không phải trong cầu thận (Hình 2b). Các đặc điểm mô học cho thấy mRNA Alox15 được thể hiện mạnh mẽ trong các ống gần.
Chuột Alox15−/− có khả năng kháng tổn thương thận và xơ hóa gan trong mô hình 5/6 NxTrong 5/6 Nx CKDthận, nồng độ biểu hiện phiên mã và protein của ALOX15 đã tăng cao. Do đó, chúng tôi đã điều tra xem ALOX15 có đóng vai trò như thế nào trong CKD về mặtthậnrối loạn chức năng và xơ hóa thận. Với mục đích này, chuột Alox15−/− đã được áp dụng cho mô hình 5/6 Nx CKD. Điều thú vị là nồng độ Cre và nitơ urê máu (BUN) trong huyết thanh thấp hơn ở chuột Alox15 −/− 5/6 Nx

so với những con chuột loại hoang dã (WT) (Hình 3a), chỉ ra rằng sự suy giảm Alox15 cho thấy tác dụng bảo vệ trong sinh bệnh học CKD. Theo đó, NGAL (mộttổn thương thậnchất đánh dấu) biểu hiện protein đã bị ức chế ở chuột Alox15 −/− so với biểu hiện ở chuột WT (Hình 3b). Ngoài ra, Chuột Alox15−/−thậncho thấy mức mRNA Col1a1, Fn và Acta2 (αSMA) giảm (Hình 3c), đồng thời cho thấy biểu hiện protein fibronectin và αSMA (Hình) giảm. 3d). Hơn nữa, Alox15 −/− chuộtthậnthể hiện rõ ràng những thay đổi xơ hóa kẽ bị ức chế rõ ràng được thể hiện trong nhuộm ba màu của Masson (Hình 3e). Do đó, alox15 xóa amelioratesthậnrối loạn chức năng và xơ hóa trong mô hình động vật CKD.

Lipidomics trung gian cho thấy chuyển hóa PUFA thay đổi ở Thận Alox15−/− CKDNhư đã đề cập trong phần Giới thiệu của bài báo này, các efects sinh học của Alox15 có liên quan đến các chất trung gian lipid được tạo ra bởi Alox15. Để làm sáng tỏ hồ sơ của các chất chuyển hóa lipid được sản xuất bởi Alox15 trong CKDthậnchúng tôi đã kiểm tra và so sánh sự giả mạo và 5/6 Nxthậncác mẫu của lipidomics trung gian dựa trên LC-MS / MS để xác định cấu hình chất trung gian lipid giữa chuột WT và chuột Alox15 −/− CKD (Bảng bổ sung 1). Bảng 1 cho thấy các chất chuyển hóa lipid có sự khác biệt đáng kể giữa chuột Alox15 +/+ và Alox15 −/− trong điều kiện 5/6 Nx. Ngoài ra, chúng tôi đã tạo ra các bản đồ con đường của các chất trung gian lipid với sự phân loại theo chất nền của chúng và các enzyme chuyển hóa của chúng (Hình 4). Một loạt các chất chuyển hóa PUFA có nguồn gốc từ Alox15 như 14-HDoHE, 17-HDoHE và 15-HEPA [5, 25–27] đã được tăng lên đáng kể trong các mô hình CKD tương quan tốt với mức độ biểu hiện ALOX15 tăng lên trongthận(P = 0,0018, 0,0008,<0.0001, respectively),="" and="" their="" elevations="" under="" ckd="" conditions="" were="" completely="" suppressed="" in="" alox15−/−="" mice="" (fig. 5).="" besides="" 14-hdohe,="" 17-hdohe,="" and="" 15-hepa,="" the="" levels="" of="" 18-hepa,="" 10-hdohe,="" 11-hdohe,="" 13-hdohe,="" 16-hdohe,="" and="" dgla="" were="" also="" significantly="" decreased="" in="" alox15−/−="" ckd="">thậnso với những người ở thận WT CKD, trong khi chỉ có PGD2 tăng đáng kể ở alox15−/− CKD thận (Hình 6).
PGD2 ức chế EMT trong các tế bào thận nuôi cấyCác efects của các chất chuyển hóa lipid có sự khác biệt đáng kể giữa chuột Alox15 +/+ và Alox15 −/− trong tình trạng 5/6 Nx đã được kiểm tra bằng cách đưa các lipid này vào các tế bào NRK-52E được kích hoạt bởi cytokine pro-fibrotic TGF-β1. Chúng tôi đã đánh giá biểu hiện mRNA của Cola1a và Acta2 (αSMA) để đáp ứng với TGF-β1 để xác định hiệu quả của các lipid này trong nuôi cấy (Hình 7a). Trong số đó, PGD2 đã mang lại tác dụng chống xơ hóa mạnh mẽ đối với các tế bào NRK-52E để đáp ứng với TGF-β1. Tác dụng ức chế của PGD2 đối với biểu hiện COL1A1 và αSMA phụ thuộc vào liều lượng với EC50 lần lượt là 7,12 μM và 6,48 μM (Hình 7b). Ngoài ra, chúng tôi đã tiến hành các thí nghiệm tương tự trong các tế bào HK-2, là các tế bào biểu mô ống gần bất tử từ người trưởng thành bình thườngthậnvà tìm thấy một kết quả tương tự, đó là ức chế COL1A1 và αSMA theo cách phụ thuộc vào liều lượng, để đáp ứng với điều trị bằng PGD2 (Hình 7c). Do đó, tăng nồng độ PGD2 trong Alox15−/− CKDthậncó thể góp phần vào efects antifibrotic trong CKD.

CISTANCHE SẼ CẢI THIỆN CƠN ĐAU THẬN / THẬN
15-PGDH, một enzyme chuyển hóa PGD2 chính, đã giảm ở thận Alox15−/− CKDĐể làm rõ cơ chế tăng PGD2 trongthậncủa chuột mô hình Alox15 −/− CKD, chúng tôi đã đo mức mRNA của PGD2 synthase. PGD2 synthase (PGDS) có hai đồng phân: lipocalin PGDS (L-PGDS) và PGDS tạo máu (H-PGDS) [28]. Cả hai mức L-PGDS và H-PGDS đều tăng đáng kể trong điều kiện 5/6 Nx khi so sánh với những người trong điều kiện giả mạo trong điều kiệnthậncủa chuột WT (Hình 8a, cả P<0.0001) indicating="" that="" increased="" pgd2="" in="" ckd="" is="" due="" to="" increased="" pgd2="" synthases.="" conversely,="" the="" increase="" in="" l-pgds="" and="" h-pgds="" under="" 5/6="" nx="" conditions="" was="" significantly="" inhibited="" in="" alox15−/−="" mice="" (fig. 8a)="" indicating="" that="" the="" increase="" in="" pgd2="" in="" alox15−/−="" ckd="" model="" mice="" was="" not="" due="" to="" increased="" production="" by="" pgds.="" then,="" we="" examined="" mrna="" levels="" of="" cox-1="" and="" cox-2="" as="" more="" upstream="" synthases="" of="" the="" prostaglandin-producing="" pathway.="" we="" also="" measured="" mrna="" levels="" of="" 15-pgdh="" and="">1C18, được biết đến là các enzyme chuyển hóa PGD2 chính [29, 30]. Trong khi nồng độ mRNA của COX-1, COX-2 và AKR1C18 không thay đổi, mức mRNA của 15-PGDH đã giảm đáng kể trong CKDthậncủa chuột Alox15−/− khi so sánh với chuột WT (Hình 8b, P=0,0325), có khả năng dẫn đến sự gia tăng PGD2 trong CKDthậncủa chuột Alox15−/−.


Sự thảo luận
Nghiên cứu này đã chứng minh rằng trong CKDthậncác mẫu, cả nồng độ phiên mã và protein của Alox15 đều tăng lên, vàthậnrối loạn chức năng và xơ hóa đã được cải thiện ở chuột Alox15−/−. Ngoài ra, lipidomics hòa giải dựa trên LC-MS / MS tiết lộ rằng chuột Alox15 −/− CKDthậnđã tăng đáng kể mức ĐỘ PGD 2 so với chuột WT. PGD2 ức chế EMT của các tế bào NRK-52E và HK-2; do đó, sự gia tăng PGD2 có thể góp phần vào sức đề kháng của chuột Alox15−/−tổn thương thậnvà xơ hóa. Mối quan hệ giữabệnh thậnvà hồ sơ lipid sử dụng lipidomics trên huyết thanh hoặc huyết tương của con người đã được nghiên cứu rộng rãi [31–33], nhưng không phải trênthậnmô. Tương tự, mặc dù các báo cáo về lipidomics sử dụng mô hình động vật CKD rất ít [34–36], tất cả các nghiên cứu này đều thực hiện lipidomics trên các mẫu huyết tương từ mô hình động vật CKD; tuy nhiên, không có lipidomics toàn diện trênthậncác mô từ mô hình CKD đã được báo cáo. Lipidomics trực tiếp trên mô cũng có hiệu quả, cũng như các mẫu huyết tương, trong việc xác định các chất chuyển hóa chức năng. Hơn nữa, những thay đổi chất chuyển hóa trong các mô, cũng như các mẫu máu, khác nhau đáng kể theo cơ quan [20]. Trong nghiên cứu hiện tại, chúng tôi đã phân tích kỹ lưỡng hồ sơ của các chất trung gian lipid có nguồn gốc từ PUFA trongthậncác mô của mô hình động vật CKD.


Nghiên cứu này tập trung vào ALOX15, một trong những enzyme chính chuyển hóa PUFA. Trong nghiên cứu này, cả mức độ biểu hiện protein và mRNA của ALOX15 đều tăng rõ ràng trong CKDthận. Chúng tôi đã giải quyết các loại ô chịu trách nhiệm về biểu thức ALOX15 trong CKDthậnvà bằng cách lai tạo tại chỗ, chúng tôi đã tìm thấy sự gia tăng biểu hiện của ALOX15 mRNA trongThậntế bào hình ống trong mô hình 5/6 Nx.

ALOX15 có liên quan đến các bệnh mãn tính, chẳng hạn như xơ vữa động mạch và việc xóa nó trong các mô hình bệnh động vật giúp cải thiện các bệnh này [5]. Về sự liên kết của ALOX15 vớibệnh thận, protein niệu giảm ở chuột Alox15−/− dưới tổn thương cầu thận do mô hình bệnh thận đái tháo đường do streptozotocin gây ra [37]. Tuy nhiên, mô hình chuột đái tháo đường này không cho thấy bất kỳ sự suy giảm nào trongchức năng thận; do đó, cơ chế về cách ALOX15 có liên quan đến suy yếuchức năng thậntrong các mô hình CKD vẫn chưa rõ ràng. Trong nghiên cứu hiện tại, sử dụng mô hình chuột 5/6 Nx, chúng tôi thấy rằng việc xóa ALOX15 đã được cải thiệnthậnrối loạn chức năng vàThậnxơ hóa trong một mô hình CKD. Cho đến nay, chỉ có IL-4 và IL-13 trong bạch cầu đơn nhân được biết đến là các yếu tố điều tiết làm tăng trực tiếp sự biểu hiện của ALOX15 [5]. Tuy nhiên, vẫn chưa rõ điều gì làm tăng ALOX15 trongThậntế bào hình ống. Một loạt các cytokine và độc tố uremic được biết là được tăng lên trong huyết tương và thận trong CKD [38, 39]. Trong số đó, có thể có các cơ quan quản lý mới của ALOX15. Các nghiên cứu sâu hơn là cần thiết để làm sáng tỏ các yếu tố quy định chính của ALOX15 trong CKD. Trong các nghiên cứu của chúng tôi để xác định các oxylipin can thiệp cụ thể liên kết việc xóa Alox15 với tác dụng bảo vệ của nó trong mô hình 5/6 Nx, chúng tôi nhận thấy rằng PGD2 có thể liên quan đến khả năng chống lạitổn thương thậngây ra bởi việc xóa ALOX15. Như một sự hiểu biết chung, để tạo ra PGD2, COX-1 và

CCOX-2 sản xuất PGG2 từ axit arachidonic, sau đó được chuyển đổi thành PGH2. Khi PGH2 được chuyển hóa bởi PGD2 synthase (PGDS), PGD2 được tạo ra [28]. PGDS có hai đồng phân riêng biệt về mặt di truyền, đó là LIPOCALINTYPE PGDS (L-PGDS) và PGDS kiểu tạo máu (H-PGDS) [28]. Mặc dù PGD2 đã được tăng lên trong chuột Alox15−/− CKDthận, cả L-PGDS và H-PGDS đều không được tăng lên trong chuột Alox15−/− CKDthận, bất chấp sự gia tăng lớn PGDS trong chuột WT CKDthận(Hình 8a). Hơn nữa, chúng tôi cũng tiết lộ rằng cả COX-1 và COX-2 đều không được tăng lên trong thận chuột Alox15 −/− CKD (Hình 8b). Những kết quả này cho thấy sự gia tăng PGD 2 trong thận chuột Alox15 −/− CKD không phải do sự gia tăng synthases mà là do sự sẵn có của chất nền tăng lên hoặc ức chế sự thoái hóa, và trên thực tế, chúng tôi đã tiết lộ sự giảm 15-PGDH, một trong những enzyme chuyển hóa PGD2 chính [29], trong thận chuột Alox15 −/− CKD (Hình 8b). Cần điều tra thêm để làm sáng tỏ lý do tại sao việc xóa Alox15 dẫn đến giảm 15-PGDH.
Như đã đề cập ở trên, PGD2 có thể tham gia vào cuộc kháng chiếntổn thương thậngây ra bởi sự mất mát ALOX15. Trong nghiên cứu này, PGD2 đã ức chế EMT bằng TGF-β1 trong các tế bào NRK-52E và HK-2, đại diện cho các tế bào hình ống gần. PGD2 liên kết với hai thụ thể kết hợp protein G khác nhau, đó là DP1 và DP2, có chức năng khác nhau [28]. Tuy nhiên, trong các thí nghiệm trong ống nghiệm của chúng tôi, PGD2 có hiệu quả ở nồng độ từ 4 đến 32 μM, tương đối cao, xem xét rằng các giá trị Ki của DP1 và DP2 lần lượt là 1,7 nM và 2,4 nM [28]. Kết quả này chỉ ra rằng PGD2 có thể phát huy tác dụng efects antifibrotic không thông qua các thụ thể kết hợp protein G mà thông qua các con đường khác như PPARγ, qua đó 15-d-PGJ2, một chất chuyển hóa PGD2 hạ lưu, được biết là tác động hiệu quả của nó [28]. Trong nghiên cứu này, tập trung vào các enzyme chuyển hóa lipid và các chất chuyển hóa của chúng, ức chế ALOX15 và / hoặc quản lý PGD2 có thể là một mục tiêu điều trị đầy hứa hẹn cho CKD. Thật không may, không có chất ức chế đặc hiệu ALOX15 có thể được sử dụng trong thực hành lâm sàng đã được phát triển [40, 41]. Nhắm mục tiêu điều trị các chất chuyển hóa chức năng xuôi dòng, chẳng hạn như PGD2, thay vì ức chế các enzyme chuyển hóa axit béo, ảnh hưởng đến các chất chuyển hóa khác nhau, có thể là một liệu pháp CKD lý tưởng mới.

CISTANCHE SẼ CẢI THIỆN LỌC THẬN /THẬN
