Phần 2: Ceramide -1- Phosphate như một chất điều chỉnh tiềm năng của máy bơm natri thứ hai từ các ống gần thận bằng cách kích hoạt các con đường protein Kinase riêng biệt theo cách phân cấp
Jul 27, 2022
Để biết thêm thông tin. tiếp xúctina.xiang@wecistanche.com
4. Thảo luận
Sự vận chuyển chất lỏng qua biểu mô ống là một trong những sự kiện quan trọng liên quan trực tiếp đến phần lớn cácchức năng thận[49]. Trong số các chất hòa tan khác nhau được xử lý trongquả thận, Nat đặc biệt quan trọng. Do có nhiều trong dịch ngoại bào, cần phải hiểu cơ chế Nat được tái hấp thu hoặc bài tiết qua nước tiểu vì sự thay đổi nồng độ Na cộng thêm trong kẽ và trong mạch dẫn đến thay đổi thể tích và có thể gây rối loạn huyết áp [50] . Việc điều chỉnh nồng độ Nat trong các ngăn chứa chất lỏng của cơ thể chủ yếu được điều khiển bởi các chất vận chuyển tích cực chính với Nat cổ điển cộng với Kt-ATPase [51] tham gia vào quá trình vận chuyển khối lượng, trong khi bơm Nat "thứ hai" hoặc Nat-ATPase tham gia vào quá trình mịn- Điều chỉnh điều chỉnh tái hấp thu Nat [52,53] Có nhiều báo cáo trong tài liệu liên quan đến việc điều chỉnh Nat cộng với K cộng với -ATPase của hormone và autacoids [50,54] cũng như vai trò của quá trình điều hòa phosphoryl hóa [50,55]. Ngược lại, ít nhóm hơn trích dẫn quy định củaNa plus -ATPase vì vẫn còn một số tranh cãi liên quan đến danh tính của nó, mặc dù các báo cáo cho thấy hoạt động Nat-ATPase nhạy cảm với furosemide từ động vật có vú [41,56,57] đến động vật nguyên sinh [58,59 ] cũng như sao chép máy bơm từ các sinh vật khác nhau [60-63]. Từ các kết quả được trình bày ở đây, nhóm của chúng tôi đã chỉ ra rằng không chỉ các hormone và autacoids có thể kích hoạt các con đường truyền tín hiệu tế bào điều chỉnh Nat-ATPase, mà tác động của ClP được bổ sung ngoại sinh vào các phân đoạn BLM chỉ ra sự tương tác có thể xảy ra của lipid hoạt tính sinh học. với các lĩnh vực kỵ nước của bộ điều chỉnh, hoặc chính máy bơm; hoặc, phải có một loại thụ thể C1P trong BLM, chưa được xác định [20,22,23]. Hình 6 cho thấy một kế hoạch được đề xuất để tóm tắt những cách thức hành động có thể có của ClP. Khả năng kích hoạt kinase của ceramides và tạo ra một phản ứng sinh lý khác nhau đã được báo cáo trong tế bào gan [24]. Các tác giả không chỉ cho thấy khả năng điều biến phụ thuộc ceramide của điều hòa Nat / K cộng với -ATPase và kinase, mà họ còn báo cáo các phản ứng hai pha xem xét sự kích thích phụ thuộc vào thời gian của các dòng tế bào đó, điều này minh họa rằng phải có nhiễu xuyên âm phức tạp giữa ceramide - Tín hiệu phụ thuộc và các hệ thống tín hiệu khác có trong màng tế bào. màng (Hình 2). Hơn nữa, các kết quả được trình bày ở đây kết hợp với các kết quả trước đó từ nhóm của chúng tôi cho thấy rõ ràng rằng Cer [33] và ClP đã điều chỉnh PKA và PKC liên quan đến BLM, dường như làm trung gian cho các tác động gây ra bởi ceramide trên Nat-ATPase Khi các phân đoạn BLM được được xử lý bằng 100 nM C1P, sự ức chế bơm không thể do PKA (Hình 4) vì việc ủ trước với PKAi không ảnh hưởng đến hoạt động ức chế C1P. Mặt khác, sự ức chế đáng kể hoạt động của Nat-ATPase khi xử lý bằng ClP được ngăn chặn hoàn toàn bởi calphostin C (Hình 3). Các báo cáo trước đây đã chỉ ra rằng PKA kích thích hoạt động Nat-ATPase ở thận theo con đường liên kết các thụ thể kết hợp với Gs với hoạt động của bơm [41]. Các hệ thống tín hiệu có ở đây trong bản thảo của chúng tôi — PKA và PKC — đã được nghiên cứu kỹ lưỡng, vì vậy có rất nhiều thông tin trong tài liệu cho thấy nồng độ đối với các đối chứng dương tính như được sử dụng ở đây (tương ứng là cAMP và phorbol myristate acid PMA). Vì trọng tâm của chúng tôi không phải là nghiên cứu đáp ứng theo liều lượng với các chất kích hoạt hoặc chất ức chế cổ điển cho các hệ thống tín hiệu khác nhau, chúng tôi chỉ sử dụng nồng độ của chất kích hoạt hoặc chất ức chế đã được sử dụng hiệu quả trong các nghiên cứu khác từ chúng tôi hoặc các nhóm khác.
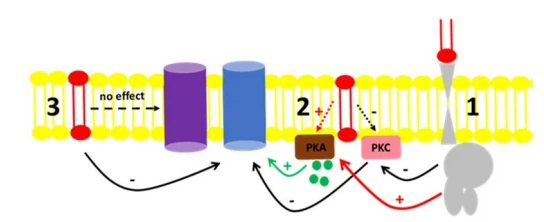
Hình 6. Cơ chế đề xuất cho tác dụng của ClP đối với hoạt động Na cộng với -ATPase từ BLM. (1) C1P (lipid đỏ) ức chế PKC thông qua một thụ thể kết hợp với protein G chưa được biết đến, dẫn đến ức chế Na cộng -ATPase (protein xanh lam). Tuyến đường tương tự có thể kích hoạt BLM PKA (mũi tên màu đỏ) mà không ảnh hưởng đến máy bơm. (2) CIP có thể liên kết trực tiếp với các tác nhân có trong BLM, chẳng hạn như PKC, dẫn đến tác dụng ức chế hoạt động Na plus -ATPase được mô tả. Kết quả của chúng tôi cho thấy rằng mặc dù PKA có mặt trong BLM và sẵn sàng điều chỉnh máy bơm bằng cAMP (vòng tròn màu xanh lá cây và mũi tên màu xanh lá cây), việc kích hoạt nó bằng CIP không ảnh hưởng đến máy bơm (mũi tên gạch ngang màu đỏ). (3) CIP liên kết trực tiếp với Nat-ATPase hoặc được làm giàu trong vi môi trường màng lipidic bao quanh Nat-ATPase, do đó điều chỉnh nó. Từ các kết quả được trình bày ở đây, chúng tôi không thể phát hiện bất kỳ hành động điều biến nào của ClP trên Nat / K cộng với -ATPase (protein màu tím) có trong các phân đoạn BLM.
Nhấp vào đây để tìm hiểu cistanche mở rộng tuổi thọ được chuẩn hóa
Việc phát hiện ra sự phân cấp trong quá trình phosphoryl hóa Nat-ATPase được đề xuất khi chúng tôi kích thích BLM bằng Cer [33] và chúng tôi quan sát thấy rằng sự tắc nghẽn của BLM-PKCZ, làm giảm tác dụng ức chế của Cer trên máy bơm và cho phép cAMP- kích hoạt PKA để kích thích nó. Mặc dù ngày càng có nhiều báo cáo cho thấy các vai trò khác nhau đối với kinase kích hoạt Cer [44, 64-66], đây là báo cáo đầu tiên về hoạt động sinh lý của C1P trên kinase thường trú BLM, chắc chắn đóng một vai trò trong việc điều chỉnh Nat xử lý ở thận. Chúng tôi không thể khẳng định chắc chắn rằng Nat-ATPase được phosphoryl hóa trực tiếp bởi các kinaza đã nghiên cứu, vì không có công cụ thí nghiệm nào cho việc này, chủ yếu là do cấu trúc hoàn chỉnh của bơm natri thứ hai vẫn chưa được xác định. Tuy nhiên, ai cũng biết rằng Nat-ATPase là một ATPase loại P, và thực tế này cho phép chúng ta công nhận rằng nó có thể được điều chỉnh trực tiếp bằng cách phosphoryl hóa ở các vị trí điều hòa giả định [46,55] Chúng ta không thể loại trừ rằng sự hoạt hóa của các kinase tương ứng sẽ dẫn đến sự phosphoryl hóa của một protein khác trong mạng lưới điều hòa này, điều này sẽ gây ra sự ức chế ATPase.
Trong số các sphingolipid có hoạt tính sinh học khác nhau, C1P ít được ghi nhận trong các hệ thống sinh lý khác nhau. Mặt khác, sphingosine -1- phosphate, có thể là lipid hoạt tính sinh học quan trọng nhất, được nghiên cứu rất kỹ trong sinh lý học và sinh lý bệnh của thận [2,6,7,67]. Vì các thành viên S1P và ClP là một loại phân tử tín hiệu với các tiền chất chung và chia sẻ các bước chuyển đổi lẫn nhau, nên có thể tưởng tượng rằng ClP cũng sẽ hiện diện dọc theo toàn bộ nephron. Công trình của Sugiura và cộng sự, 2002 [11], một dấu ấn trong lĩnh vực này, đã chỉ ra rằng CerK được biểu hiện rất nhiều ở thận. Mặc dù có dữ liệu mạnh mẽ trong tài liệu cho thấy vai trò của ClP trong tế bào nang và bệnh cầu thận [68,69], chưa có công trình nào cho thấy biểu hiện CerK và tác động của ClP trong bất kỳ đoạn nephron nào. Nếu không, ClP có thể hiện diện trong tất cả các tế bào thận do sự hiện diện của sphingomyelin, điều này sẽ cho phép con đường cứu cánh để tổng hợp ClP, hoặc do ClP có thể được cung cấp cho mô thận theo đường máu. Đây là những cách rất hợp lý để nghĩ rằng lipid tín hiệu này sẽ đóng các vai trò khác nhau trong các phân đoạn nephron khác, mặc dù chúng tôi không khám phá nó ở đây.
Nó đã được chứng minh một cách đáng kể rằng mức Cer đã được nâng lên đáng kể trongchấn thương thậndo sự gia tăng hoạt động sphingomyelinase do Ca2t kích thích đã được báo cáo sau khi cân bằng nội môi Ca2t của tế bào bị phá vỡ [2,4,24,70]. Quan sát này cho phép chúng tôi giả định rằng sự điều biến qua trung gian kinase của hoạt động BLM Nat-ATPase của Cer và C1P có thể đặc biệt liên quan trong mô thận bị tổn thương, điều này có thể mở ra một vai trò mới cho ceramide trong việc hình thành và tiến triển bệnh thận. Với sự có mặt của C1P, các BLMkinase được nghiên cứu đã được điều chế vi sai (Hình 5). Trong khi ClPin ức chế PKC, dẫn đến ức chế đáng kể hoạt động Nat-ATPase, sự hoạt hóa PKA phụ thuộc C1P không ảnh hưởng đến hoạt động Nat-ATPase. Điều này cho phép chúng ta giả định rằng có một hệ thống phân cấp liên quan đến các kinaza khác nhau, dẫn đến việc chuyển đổi phức tạp vào / tắt Nat-ATPase. Sự chuyển đổi này có thể liên quan đến các dạng đồng dạng khác nhau của PKC và PKA, hoặc, phải có nhiễu xuyên âm với khả năng chuyển đổi C1P thành Cer và các lipid hoạt tính sinh học khác kích hoạt các con đường tín hiệu khác được chứa trong BLM, vốn đã được mô tả trong tế bào gan [24].
Sự cân bằng giữa Cer và ClP có thể là một mục tiêu đầy hứa hẹn mới cho việc phát triển các nhóm thuốc mới với hành động hiệu quả hơn để cố gắng ngăn chặn tiến trình củasuy thận, hoặc ít nhất, nâng cao chất lượng cuộc sống cho bệnh nhân thận.

5. Kết Luận
Từ các kết quả được trình bày ở đây, một dòng tín hiệu bắt đầu với sản xuất Cer và tiếp tục phosphoryl hóa thành ClP là một con đường hiệu quả để ức chế Nat-ATPase trongtế bào ống thận gầnthông qua PKA liên kết với BLM và PKC làm hiệu ứng [17]. Những quan sát này cho thấy tầm quan trọng của protein kinaza trong việc kiểm soát tốt dòng chảy Nat trong một đoạn nephron nơi hơn 2/3 siêu lọc cầu thận được tái hấp thu, là ống lượn gần. Theo hiểu biết tốt nhất của chúng tôi, công trình nghiên cứu hiện tại lần đầu tiên cho thấy ClP có thể điều chỉnh BLM-Nat-ATPase từ các tế bào ống lượn gần thận bằng cách kích hoạt các kinase liên kết với màng (PKA và PKC). Do đó, các kết quả trên là bằng chứng cho quan điểm rằng Cer và ClP tham gia vào mạng lưới điều tiết của các sphingolipid và glycerolipid có hoạt tính sinh học cư trú trong phân đoạn nephron này, điều này sẽ đúng với nephron tổng thể. Giả thuyết này có thể được hỗ trợ bởi quan điểm rằng Cer là một lipid hầu như hiện diện trong tất cả các phân đoạn nephron cũng như sự sẵn có của Cer sẽ cho phép hình thành C1P.

