Hiệu quả của chất chống oxy hóa sản phẩm phụ trong chế độ ăn uống đối với sự biểu hiện gen CYP cảm ứng và sự thay đổi mô học ở lợn con Gan và thận liên quan đến Aflatoxin B1 và Ochratoxin A
Feb 26, 2022
Trừu tượng:Mục đích của nghiên cứu này là để điều tra tiềm năng của một hỗn hợp phụ phẩm có nguồn gốc từ dầu hạt nho và dầu hắc mai biển để giảm thiểu tác hại gây ra bởi ochratoxin A và aflatoxin B1 ở gan vàthậnmức độ ở heo con sau cai sữa. Bốn mươi lợn con lai TOPIGS -40 con lai sau khi cai sữa được giao cho ba nhóm thí nghiệm (E1, E2, E3) và một nhóm đối chứng (C), và được nuôi bằng khẩu phần thí nghiệm trong 30 ngày. Chế độ ăn cơ bản được dùng để kiểm soát và chứa thức ăn hỗn hợp bình thường cho heo con mới bắt đầu không có độc tố nấm mốc. Các nhóm thí nghiệm được cho ăn như sau: E1 - khẩu phần cơ bản cộng với hỗn hợp (1: 1) của hai sản phẩm phụ (hạt nho và bột hắc mai biển); E2 - chế độ ăn cơ bản bị nhiễm độc tố nấm mốc (479 ppb OTA và 62ppb AFB1); và E3 - chế độ ăn cơ bản chứa 5% hỗn hợp (1: 1) bột hạt nho và hắc mai biển và bị nhiễm hỗn hợp OTA và AFB1. Sau 4 tuần, những con vật được giết mổ, và các mẫu mô được lấy từ gan và quả thận để thực hiện biểu hiện gen và phân tích mô học. Phân tích biểu hiện gen cho thấy rằng khi lợn con cai sữa được cho ăn bằng chế độ ăn bị ô nhiễm, sự biểu hiện của hầu hết các gen được phân tích bị điều hòa. Trong số họ CYP450, CYP1A2 là gen có điều hòa giảm cao nhất. Theo những kết quả này, ở gan, chúng tôi nhận thấy rằng độc tố nấm mốc gây ra những thay đổi về hình thái học ở gan vàquả thậnvà có ảnh hưởng đến mức độ biểu hiện của CYP1A2, CYP2A19, CYP2E1 và CYP3A29, nhưng chúng tôi không phát hiện thấy những thay đổi quan trọng trong mức độ biểu hiện của các gen CY4A24, MRP2 và GSTA1.
Từ khóa: heo con; tác dụng chống oxy hóa; phụ gia thức ăn chăn nuôi; độc tố nấm mốc; Biểu hiện gen CYPs; thận; thận
Giới thiệu
Độc tố nấm mốc là chất độc chuyển hóa thứ cấp được tạo ra bởi một số chủng nấm sợi. Các hợp chất có trọng lượng phân tử thấp này (lên đến 500 Da) có thể gây ô nhiễm nhiều loại nguyên liệu thô và gây tăng nguy cơ đối với sức khỏe con người và động vật [1]. Số lượng độc tố nấm mốc được đặc trưng và có tác dụng nổi tiếng là tương đối ít do có vô số chất chuyển hóa có khả năng gây độc do nấm tạo ra [2 - 4]. Chúng được phân thành năm nhóm, với các cấu trúc hóa học cụ thể thường xuất hiện trong thức ăn và thực phẩm: trichothecenes, zearalenone, ochratoxins, fumonisins và aflatoxin. Các loại nấm sản xuất độc tố mycotoxin có trong thực phẩm và thức ăn chăn nuôi được chia thành hai nhóm: nhóm xâm nhập trước khi thu hoạch ngũ cốc, được gọi là nấm đồng ruộng, và nhóm chỉ phát triển sau khi thu hoạch được gọi là nấm bảo quản [5]. Ở cấp độ châu Âu, có các quy định và khuyến nghị về mức tối đa được chấp nhận đối với sáu loại độc tố nấm mốc thường thấy trong thức ăn của lợn: aflatoxin, fumonisin, ochratoxin, deoxynivalenol, độc tố T2, và zearalenone [6 - 8]. Trong số các loài động vật trang trại, lợn rất nhạy cảm với độc tố nấm mốc do chúng tiếp xúc với thức ăn gia súc làm từ ngũ cốc [9]. Sự trao đổi chất của lợn không hiệu quả trong việc giải độc và bài tiết độc tố nấm mốc, làm tăng nguy cơ nhiễm độc nấm. Tính nhạy cảm này cũng thay đổi theo độ tuổi, nồng độ độc tố nấm mốc trong thức ăn và thời gian tiếp xúc. Gan là cơ quan bị ảnh hưởng nhiều nhất bởi việc tiêu hóa các chất độc này [10]. Hơn nữa, những chất độc này làm tăng tính thấm của hàng rào biểu mô ruột ở lợn và gia cầm, có thể tạo ra khuynh hướng gây viêm ruột hoại tử [11] và giảm khả năng miễn dịch bẩm sinh.

CISTANCHE SẼ CẢI THIỆN KIDNEY / RENAL FUCTION
Aflatoxin đại diện cho các loại độc tố nấm mốc nhiều nhất được tìm thấy trong thực phẩm, hạt có dầu, ngũ cốc, sữa, đất, động vật và con người. Tất cả các loại aflatoxin đều có nguồn gốc từ các loài nấm thuộc giống Aspergillus và được coi là một trong những loại độc tố nấm có hại nhất cho động vật và con người [4, 1 0 - 17]. Như đã đề cập ở trên, ở lợn con còn bú và lợn đang lớn, thành phẩm và lợn giống, tác dụng sinh học chính của aflatoxin là gây ung thư, ức chế miễn dịch, gây đột biến, gây quái thai, giảm hiệu quả và tăng trọng kém, suy gan và thay đổi các thông số sinh hóa huyết thanh [18, 19] . Ảnh hưởng nghiêm trọng ở lợn có thể dẫn đến viêm gan cấp tính, xuất huyết toàn thân, thận hư và tử vong [20], cũng như giảm khả năng chống chịu với stress [21]. Một số tác giả cũng đã chỉ ra rằng lợn được nuôi với hàm lượng aflatoxin thấp có dấu hiệu phù phổi, giảm tiêu thụ thức ăn và tăng trọng, giảm hoạt động của các enzym liên quan đến quá trình khử cacbon oxy hóa, cũng như tổng protein huyết thanh, huyết áp, và tổng số bạch cầu [18, 22 - 24]. Trong bối cảnh này, theo Chỉ thị 2003/100 / EC của Ủy ban Châu Âu, mức aflatoxin B1 (AFB1) tối đa được chấp nhận đối với lợn được đặt ở mức 0,02 mg / kg. Ochratoxin là chất chuyển hóa thứ cấp được tạo ra bởi các loài nấm thuộc giống Aspergillus và Penicillium. Các ý kiến khác nhau về cơ chế gây độc gen hoặc không độc đối với độc tính của ochratoxin đã được công bố [25, 26]. Các nghiên cứu in vitro và in vivo cho thấy rằng các sản phẩm bổ sung DNA đặc hiệu cho guanine-OTA vẫn tồn tại hơn 16 ngày ởthậnmức độ, trong khi ở gan và lá lách, chúng được loại bỏ sau 5 ngày [27]. Do đó, tác dụng độc hại và gây ung thư chính của chúng đã được tạo ra trongquả thận[28].
Hầu hết các chất chuyển hóa của ochratoxin từ giai đoạn I và giai đoạn II giải độc có độc tính thấp. Trong dạ dày, một phần ochratoxin bị thủy phân thành ochratoxin nhờ các enzym phân giải protein. Một khả năng khác cho sự thủy phân của chúng là mở vòng lacton trong điều kiện kiềm của ruột, do đó tạo ra một hợp chất có độc tính cao. Do liên kết mạnh với albumin, sự thải trừ ochratoxin qua quá trình lọc ở cầu thận là không đáng kể, với sự bài tiết chủ yếu qua bài tiết ở ống thận. Sự tái hấp thu ở ống được coi là nguyên nhân một phần cho sự tích tụ nội bào của ochratoxin [29,30]. Nói chung, ở động vật trang trại, ochratoxin được hấp thu nhanh chóng sau khi ăn qua đường tiêu hóa (dạ dày và phần gần của hỗng tràng) theo cách thụ động, được ưa chuộng bởi ái lực cao của liên kết ochratoxin với protein huyết tương và ở dạng không ion hóa , điều này giải thích sự tồn tại của chúng trong cơ thể. Trong huyết thanh lợn, ochratoxin liên kết đặc biệt hơn với protein có khối lượng phân tử nhỏ hơn 20 kDa, cho phép chúng đi qua màng đáy cầu thận và gây độc cho thận. Ochratoxin cũng tích tụ trong gan và cơ. Tuy nhiên,thậnlà nơi dự trữ ochratoxin chính, với sự tái hấp thu của chúng ở ống gần và ống xa góp phần làm cho cơ thể tồn tại lâu bền và tăng độc tính trên thận [27,31]. Mặt khác, một khi AFB1 được hấp thụ ở cấp độ ruột, nó sẽ đến gan, nơi nó được chuyển hóa bởi các enzym chuyển hóa Giai đoạn I bằng cách hydroxyl hóa, hydrat hóa, khử methyl và oxy hóa epoxid. Ba phản ứng đầu tiên tạo ra các chất chuyển hóa không độc hại, trong khi phản ứng thứ tư tạo ra AFB 1-8, 9 epoxit tạo thành các sản phẩm bổ sung với DNA tại vị trí N7 của guanin [32]. Ngoài ra, AFB1 có thể được liên hợp với glutathione khử trong một phản ứng được xúc tác bởi glutathione-S-transferase [33] và axit glucuronic [34]. Sự bài tiết AFB1 xảy ra chủ yếu qua đường mật, sau đó là đường tiết niệu [35].
Một trong những khó khăn chính gặp phải trong việc kiểm soát độc tố nấm mốc là có nhiều hơn một loại độc tố nấm mốc có trong một lô thức ăn gia súc hoặc ngũ cốc cùng một lúc. Do đó, cho lợn con và lợn ăn thức ăn bị ô nhiễm với một số loại độc tố nấm mốc, ngay cả khi chúng ở nồng độ tối thiểu, có thể gây ra nhiều hậu quả tiêu cực do tác dụng cộng hưởng của chúng [36 - 40]. Trong bối cảnh này, việc giảm thiểu và loại bỏ các tác động tiêu cực của độc tố nấm mốc có trong thức ăn cho lợn có thể làm giảm chi phí sản xuất và tổn thất trong ngành chăn nuôi lợn. Cho đến nay, nhiều chiến lược đã được phát triển để ngăn ngừa, giảm thiểu hoặc thậm chí loại bỏ ô nhiễm độc tố nấm mốc từ thức ăn chăn nuôi bằng các phương pháp khử độc sinh học, hóa học và vật lý. Các phương pháp này cho phép phân hủy độc tố nấm mốc và các chất chuyển hóa tương ứng của chúng và duy trì giá trị dinh dưỡng của thực phẩm mà không đưa các chất khác có tiềm năng độc hại vào hệ thống sinh học [6,14,41]. Khử độc sinh học đối với mycotoxin bằng cách sử dụng sự ức chế cạnh tranh của các chủng nấm khác hoặc bổ sung các hợp chất chống oxy hóa trong thức ăn chăn nuôi để giảm tác động độc hại của mycotoxin và / hoặc để ức chế sự phát triển của các loài nấm sản xuất mycotoxin là một giải pháp tốt. Phương pháp được sử dụng nhiều nhất để chống lại tác động tiêu cực của độc tố nấm mốc đối với động vật trang trại là thêm "chất kết dính độc tố nấm mốc" hoặc "chất điều chỉnh độc tố nấm mốc", là những chất aluminosilicat có cấu trúc xốp có khả năng hấp thụ và bẫy độc tố nấm mốc [42 - 44]. Chúng rất hiệu quả đối với aflatoxin và có hoạt tính hạn chế đối với các loại mycotoxin khác. Tuy nhiên, không đặc hiệu, chúng cũng liên kết với các vitamin và nguyên tố vi lượng, tạo ra sự thiếu hụt [45 - 47]. Bổ sung một số chất chống oxy hóa có nguồn gốc thực vật trong thức ăn có thể là một giải pháp tốt hơn [48] để giảm tác động có hại của độc tố nấm mốc đối với sức khỏe động vật.
Enzyme P450 cytochromes, chủ yếu hiện diện trong gan, đường ruột vàquả thận,đóng một vai trò quan trọng trong quá trình biến đổi sinh học pha I của xenobiotics, đặc biệt là những chất thuộc họ 1 và 3 [49]. Độc tố nấm mốc có thể là chất nền, chất ức chế hoặc chất cảm ứng các enzym chuyển hóa này. Những thay đổi trong hoạt động cụ thể và khả năng cảm ứng của cytochromes P450 cuối cùng sẽ xác định sự thay đổi tương đối trong quá trình chuyển hóa của xenobiotic. Độc tố nấm mốc có thể làm thay đổi biểu hiện gen của các protein này, dẫn đến thay đổi sự hấp thụ và biến đổi sinh học của các chất dinh dưỡng và các loại thuốc cơ chất khác từ thức ăn. Do đó, mục đích của nghiên cứu này là để điều tra tiềm năng của hỗn hợp sản phẩm phụ có nguồn gốc từ ngành công nghiệp dầu Vitis vinifera (hạt nho) và Hippophae rhamnoides (hắc mai biển) để giảm thiểu tác hại gây ra bởi sự hiện diện đồng thời ochratoxin A (OTA) và aflatoxin B1 (AFB1) trong thức ăn tại gan vàthậnmức độ ở heo con sau cai sữa.
Kết quả
Thành phần chế độ ăn uốngThành phần hóa học của bột phụ phẩm cho thấy bột hắc mai biển giàu protein (cộng 38,4%), chất béo (cộng 66,6%), carbohydrate và ít tro hơn so với bột hạt nho (Bảng 1).
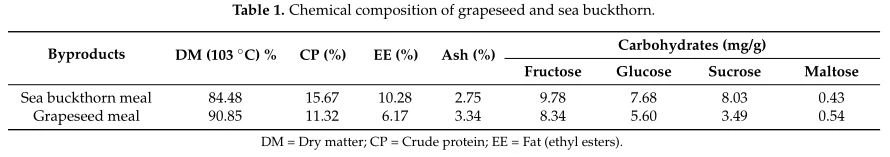
Phân tích hóa học cũng cho thấy một hồ sơ khác nhau của hai sản phẩm phụ trong axit béo, flavonoid, axit phenolic và khoáng chất. Do đó, bột hắc mai biển có hàm lượng axit béo bão hòa (palmitic và palmitoleic), axit omega -9 (axit cis oleic) và axit omega -3 (axit -linolenic) cao hơn so với bột hạt nho . Ngược lại, bột hạt nho có hàm lượng axit omega -6 (axit linoleic) rất cao (67,35% so với 18,59% trong bột hắc mai biển) (Bảng 2).
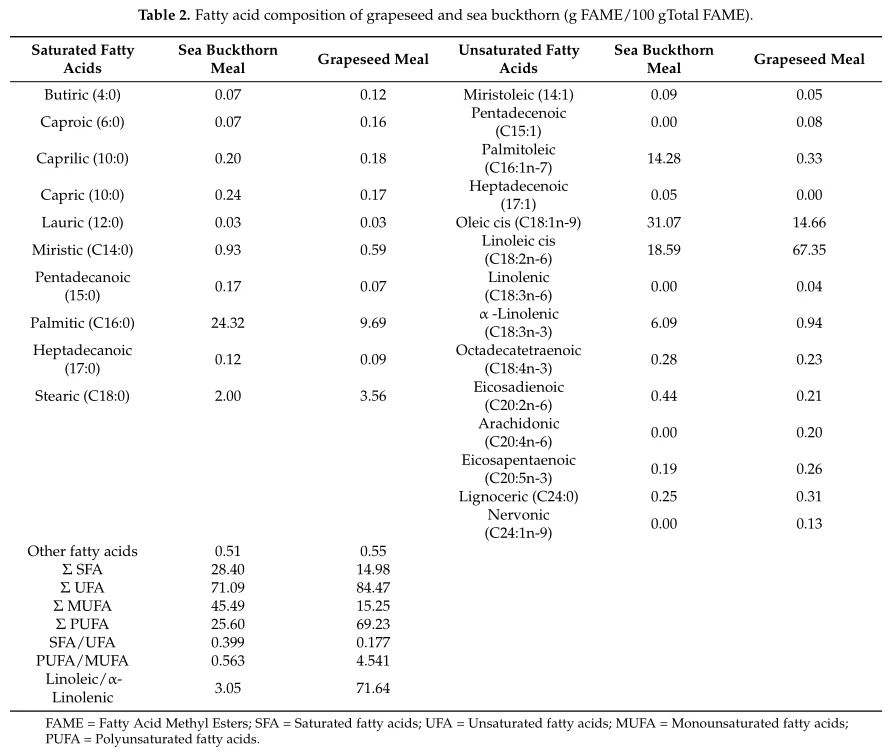
Cả hai sản phẩm phụ đều chứa flavonoid và axit phenolic, các hợp chất hoạt tính sinh học được biết đến với đặc tính chống oxy hóa, chống viêm và điều hòa miễn dịch [50, 51]. Do đó, tổng hàm lượng polyphenol trong bột hạt nho (133,84 mg GAE / L) cao hơn 74,8% so với trong hắc mai biển (76,57 mg GAE / L). Liên quan đến các loại polyphenol khác nhau, bột hạt dẻ chứa hàm lượng catechin và axit vanillic cao hơn hắc mai biển, trong khi hắc mai biển giàu rutin, quercitrin, luteolin, axit p-coumaric và axit ferulic (Bảng 3). Về thành phần khoáng chất, bột hắc mai biển có hàm lượng K, Mg, Fe, Mn và Zn cao hơn so với bột hạt nho. Ngược lại, bột hạt nho chứa lượng đồng gấp đôi so với bột hắc mai biển. Đáng chú ý là hàm lượng sắt cao từ bột hắc mai biển (Bảng 4).
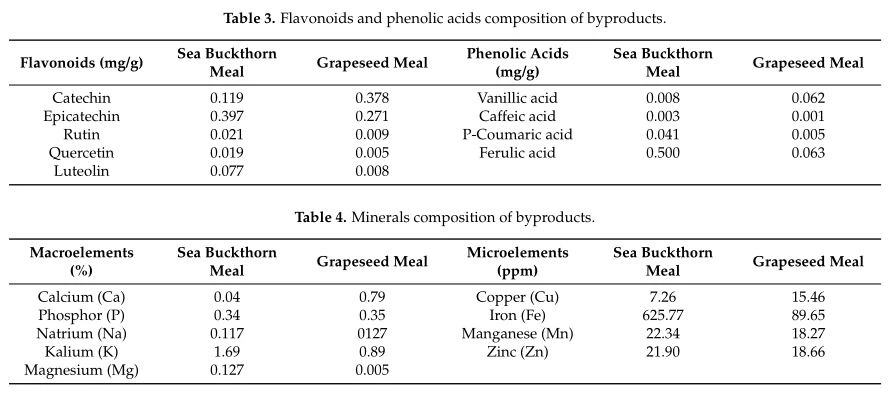
Động vật biểu diễn
Sự tiếp xúc của heo con từ nhóm E2 với hỗn hợp ochratoxin cộng với aflatoxin B1 không có tác động xấu đến trọng lượng cơ thể, tăng trọng và lượng thức ăn ăn vào, vì sự khác biệt không có ý nghĩa so với đối chứng. Ngược lại, việc áp dụng chế độ ăn chỉ có hỗn hợp các sản phẩm phụ (E1) đã làm tăng đáng kể trọng lượng cơ thể của lợn con được cho ăn theo chế độ này khi so sánh với đối chứng (32,14 ± 1,63 so với 27,09 ± 1,31) và đối với nhóm E2, được cho ăn thức ăn bị ô nhiễm. chế độ ăn (32,14 ± 1,63 so với 28,72 ± 1,07). Cần lưu ý rằng nhóm heo con ăn thức ăn bị ô nhiễm và hỗn hợp phụ phẩm có xu hướng tăng trọng so với nhóm heo con bị nhiễm độc tố nấm mốc, mặc dù sự khác biệt không có ý nghĩa. Phân tích các thông số sinh hóa, đặc trưng cho tình trạng chung của sức khỏe động vật và chức năng của gan vàthận, các giá trị bình thường đã đăng ký cho loại tuổi và trọng lượng của lợn con cai sữa. Không có sự khác biệt đáng kể nào được xác định giữa các nhóm đối với hầu hết các nhóm (Bảng 5). Tuy nhiên, hỗn hợp độc tố nấm mốc làm tăng hoạt tính ALP và gamma GT so với đối chứng và giảm hoạt tính ở mức đối chứng ở nhóm E3 nhận hỗn hợp sản phẩm phụ.
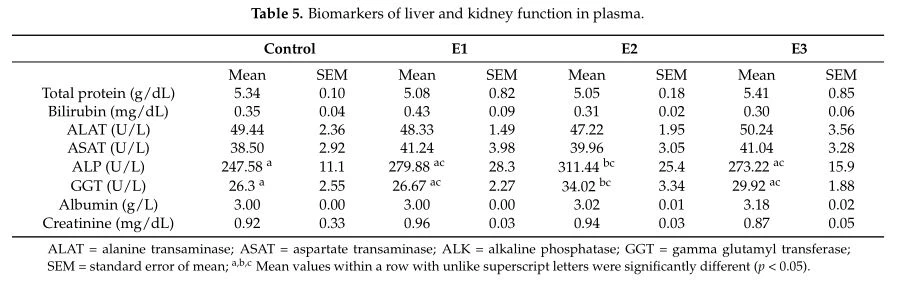
Mô học của gan và thậnPhân tích bằng kính hiển vi ánh sáng của gan từ nhóm E2, được nuôi bằng chế độ ăn cơ bản bị nhiễm hỗn hợp OTA và AFB1, cho thấy các khu vực khu trú của hoại tử, giãn các xoang và thâm nhiễm nhu mô viêm. Các khu vực cổng cho thấy thâm nhiễm tế bào đơn nhân và xơ hóa quanh cổng. Các vách ngăn xơ sợi quanh tế bào cũng được chú ý (Hình 1)
Sử dụng độc tố nấm mốc gây ra những thay đổi cấu trúc trongthậnảnh hưởng đến cả vỏ não và tủy. Người ta nhận thấy sự teo các búi cầu thận và sự thay đổi của bao Bowmann (Hình 2). Các ống cho thấy sự hoại tử của các tế bào biểu mô lót với sự xâm nhập của các tế bào viêm ở giữa. Các tập hợp tiêu điểm của các tế bào viêm được quan sát thấy ở giữa các cầu thận và ống thận liên quan đến các khu vực trọng điểm của tắc nghẽn trong mạch máu, đặc biệt là ở vùng tủy. Rõ ràng, sự tăng sinh collagen chủ yếu được quan sát thấy ở những vùng tổn thương ống thận. Hơn nữa,quả thậncác phần từ các nhóm E3, nhóm được cho ăn với chế độ ăn cơ bản chứa hỗn hợp hạt nho và bột hắc mai biển và bị nhiễm hỗn hợp OTA và AFB1, cho thấy những thay đổi bệnh lý nhỏ, gần như tương tự với đối chứng.
Ở gan, biểu hiện gen CYP1A2 giảm 18% đối với E2 và 44% đối với E3, tương ứng so với nhóm E1. Biểu hiện gen CYP2A19 không bị thay đổi trong nhóm E1 và E2, trong khi ở nhóm E3, nó giảm gần 62%. Đã quan sát thấy sự gia tăng đáng kể 29% trong biểu hiện gen CYP2E1 ở nhóm E1 được nuôi bằng chế độ ăn uống cơ bản bổ sung hỗn hợp hạt nho và bột hắc mai biển so với nhóm E2. Ngược lại, việc áp dụng chế độ ăn uống cơ bản được làm giàu với hỗn hợp hạt nho và bột hắc mai biển (nhóm E1) đã làm giảm 24% biểu hiện gen CYP3A29 so với mức nhóm E2. Một sự tương phản khác đã được quan sát thấy trong biểu hiện gen CYP4A24, với mức giảm 33% đối với nhóm E1 và giảm 24% đối với nhóm E3, và mức tăng đáng kể 41% ở nhóm E2 được nuôi bằng chế độ ăn cơ bản bổ sung hỗn hợp AFB1 và OTA, so với mức kiểm soát. Trong trường hợp MRP2, kiểu biểu hiện gen tương tự như của gen CYP4A24, với mức giảm không đáng kể 35% đối với nhóm E1 và giảm 24% đối với nhóm E3, và mức tăng đáng kể 28% ở nhóm E2. đến mức kiểm soát. Tương tự, đối với biểu hiện gen CYP4A24, biểu hiện gen GSTA1 cho thấy mức tăng đáng kể 14% ở nhóm E2, tăng 9% ở nhóm E1 và giảm 30% đối với nhóm E3. Rõ ràng, việc sử dụng đồng thời hỗn hợp hạt nho và bột hắc mai biển và OTA và AFB1 đã làm giảm tất cả các biểu hiện gen được phân tích trong gan so với đối chứng. Về mức độ biểu hiện của các gen này trongthận,so với các mẫu gan, không quan sát thấy những thay đổi có ý nghĩa thống kê (Hình 4). Tuy nhiên, những thay đổi trong quy định mức độ biểu hiện gen có thể được quan sát thấy.
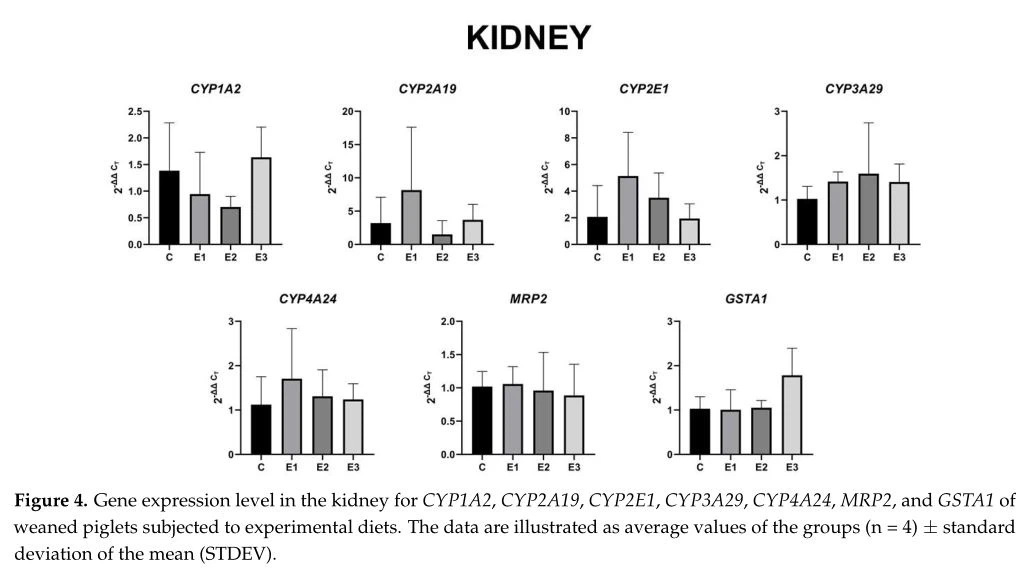
Phân tích Hình 4, có thể nhận thấy rằng hỗn hợp hạt nho và bột hạt gai biển đã điều chỉnh giảm biểu hiện gen CYP1A2 và điều chỉnh tăng cường biểu hiện gen CYP2A19, CYP2E1, CYP3A29 và CYP4A24 theo một cách không đáng kể, trong khi biểu hiện gen MRP2 và GSTA1 vẫn không bị thay đổi . Ngoài ra, sự hiện diện của OTA và AFB1 trong thức ăn của lợn con nuôi biểu hiện gen CYP1A2 và CYP2A19 điều hòa theo một cách không đáng kể, trong khi MRP2 và GSTA1 không bị thay đổi. Việc sử dụng đồng thời hỗn hợp hạt nho và bột hắc mai biển và OTA và AFB1 đã xác định sự trở lại của tất cả các mức biểu hiện gen về mức kiểm soát ngoại trừ GSTA1, mức tăng quan trọng so với nhóm E1.
Thảo luận
Các độc tố nấm mốc như AFB1 và OTA là những độc tố tự nhiên gây ô nhiễm cho nhiều loại sản phẩm thực vật. Kết quả là AFB1, OTA, và các chất chuyển hóa của chúng có trong thực phẩm và thức ăn chăn nuôi, cũng như trong các sản phẩm có nguồn gốc động vật [52]. Hầu hết các nghiên cứu về chất độc học liên quan đến tác động của độc tố nấm mốc đều xem xét sự phơi nhiễm với một loại độc tố nấm mốc đơn lẻ mà không xem xét sự kết hợp và tương tác giữa chúng, tương ứng, tác dụng hiệp đồng hoặc đối kháng thường xảy ra trong tự nhiên. Dữ liệu liên quan đến tác động độc hại của sự kết hợp độc tố nấm mốc còn hạn chế, do đó, nguy cơ tiếp xúc với một số loại độc tố vẫn chưa được biết rõ. Sự xuất hiện của các độc tố nấm mốc như AFB1, DON, ZEA, OTA, FB1 và FB2 trong ngũ cốc, sản phẩm ngũ cốc và thức ăn bổ sung và hoàn chỉnh cho lợn [16] có liên quan đến vị trí địa lý và biến đổi khí hậu, làm tăng nguy cơ liên quan nhiễm độc tố nấm mốc trong quá trình bảo quản và chế biến sản phẩm thức ăn cho lợn [53]. Sự đồng nhiễm của ngũ cốc và các nguyên liệu thô khác xảy ra trong thực tế thường xuyên hơn so với nhiễm độc tố nấm mốc đơn lẻ [7]. Ví dụ, sự đồng xuất hiện của aflatoxin B1 và ochratoxin A đã được tìm thấy trong các nguyên liệu thực phẩm hoặc thức ăn chăn nuôi khác nhau, chẳng hạn như lúa mì [54], lúa mạch [55], bột ngũ cốc [56], gia vị [57], v.v. Tỷ lệ giữa AFB1 và OTA trong nguồn cấp dữ liệu được tìm thấy là khoảng 1 đến 6 [37]. Ngoài ra, hàm lượng thức ăn toàn cầu trong AFB1 và OTA dao động giữa không xác định và 100 ppb và không xác định và 211 ppb, tương ứng [58]. Trong bối cảnh này, để bắt chước các điều kiện thực địa, chúng tôi đã nghiên cứu tác động của các độc tố nấm mốc này cùng nhau và để đánh giá hiệu quả của hỗn hợp sản phẩm phụ trong việc chống lại các tác động của độc tố nấm mốc. Các chất phụ gia tự nhiên (phụ phẩm từ hạt nho và hắc mai biển) được lựa chọn dựa trên khả năng cải thiện tình trạng nhiễm độc cơ của chúng khi bổ sung vào chế độ ăn uống [59,60].
Trong nghiên cứu này, việc lợn con (nhóm E2) tiếp xúc với hỗn hợp độc tố nấm mốc không ảnh hưởng đến năng suất của động vật (27,83 ± 1,1 so với 27. 0 9 ± 1,3 đối với trọng lượng cơ thể và 1,48 ± 0 .9 so với 1.4 0 ± 0. 8 đối với lượng thức ăn đưa vào) và các thông số sinh hóa khi so sánh với đối chứng. Tương tự, Balogh et al. [61] báo cáo rằng heo con được cho ăn với khoảng 0,4 mg / kg OTA trong giai đoạn bắt đầu (0–28 ngày) và cho con lớn (29–49 ngày) không ghi nhận những thay đổi đáng kể trong các đặc điểm sản xuất và các dấu hiệu lâm sàng của độc tính ở người nuôi. giai đoạn. Ngược lại, sự giảm trọng lượng cơ thể giảm đáng kể trong giai đoạn khởi động khi động vật nhạy cảm hơn. Trong nghiên cứu này, chế độ ăn chỉ bao gồm hỗn hợp phụ phẩm đã có ảnh hưởng đáng kể đến năng suất vật nuôi (nhóm E1) và có xu hướng tăng trọng lượng lợn con khi hỗn hợp được kết hợp với thức ăn bị ô nhiễm (nhóm E3).
Theo quan điểm độc học, OTA được IARC (Cơ quan Nghiên cứu Ung thư Quốc tế) xếp vào cùng nhóm (2B) các chất gây ung thư cho người, có độc tính tương tự AFB1 [62]. Các mô hình hấp thụ, phân phối và loại bỏ độc tố động học đối với các độc tố nấm mốc này, phần lớn, đã hoàn toàn được làm sáng tỏ. Ngược lại, bất chấp những tiến bộ gần đây, kiến thức của chúng ta về các bước biến đổi sinh học động học gây độc vẫn chưa được làm sáng tỏ một cách chi tiết. Một số nghiên cứu đã chỉ ra rằng AFB1 và OTA được chuyển hóa bởi các microsome gan của người, lợn và chuột thành một số epimers [63]. Những thay đổi trong hoạt động cụ thể và khả năng cảm ứng của cytochromes P450 cuối cùng xác định sự thay đổi tương đối trong quá trình chuyển hóa của bất kỳ xenobiotic nào.
Người ta đã phát hiện ra rằng việc tiếp xúc với AFB1 và OTA làm giảm biểu hiện gen của các gen CYP1A2, CYP2E1, CYP3A29 và MRP2 trong gan lợn và dẫn đến một số thay đổi về mô học và siêu cấu trúc gan, bao gồm các vùng tiêu điểm của hoại tử, giãn hình sin, mô viêm thâm nhiễm, và xơ hóa chu vi. Về mức độ biểu hiện gen của đồng dạng CYP450 ở lợnquả thận,không có dữ liệu nào trong tài liệu khoa học. Các gen CYP1A2, CYP2A19, CYP2E1, CYP3A29, CYP4A24, MRP2 và GSTA1 được chọn cho nghiên cứu này vì chúng mã hóa các protein có hoạt tính enzym hoặc chức năng vận chuyển liên quan đến giai đoạn I và giai đoạn II của quá trình chuyển đổi sinh học và giải độc xenobiotics để tạo thành phản ứng điện phân chất chuyển hóa [64]. Theo các kết quả này, có vẻ như việc sử dụng sản phẩm phụ đã xác định sự giảm biểu hiện gen CYP1A2 và tăng biểu hiện gen GSTA1. Kết quả tương tự cũng được nhận thấy ở HT -29 tế bào ung thư ruột kết ở người được điều trị bằng chiết xuất Salicornia freitagii, được biết đến với hoạt tính chống oxy hóa và chống viêm. Trong trường hợp này, do hàm lượng của nó trong các phenol hoạt tính sinh học, sự điều hòa giảm của mRNA CYP1A2 và sự điều hòa của mRNA GSTA1 đã xảy ra [65]. Ngược lại với kết quả của chúng tôi, mRNA và sự biểu hiện protein của CYP1A2 đã tăng lên trong gan của lợn ăn rau diếp xoăn [66]. Những kết quả khác nhau này có lẽ là do các hợp chất tự nhiên khác nhau có trong rau diếp xoăn so với các sản phẩm phụ được sử dụng trong nghiên cứu này, chủ yếu là axit chlorogenic, caffeic và p-coumaric [67].
Mặt khác, OTA và AFB1 có thể đã tương tác và kích hoạt thụ thể hydrocacbon thơm, dẫn đến sự chuyển vị hạt nhân của nó. Sau khi dị hóa, OTA và AFB1 có thể đã tương tác với chất chuyển vị hạt nhân thụ thể hydrocacbon, heterodimer, liên kết với các yếu tố đáp ứng với xenobiotic và các gen được chuyển hóa như CYP1A1, CYP1A2 và GST [68]. Yếu tố đáp ứng với xenobiotic này được chia sẻ giữa các gen CYP1A1 và CYP1A2 [69], và hai enzym được mã hóa bởi chúng thể hiện tính đặc hiệu của cơ chất chồng lên nhau [70]. Trong gan lợn, chỉ có hoạt động CYP1A2 là có, và tổng lượng CYP450 tương đối được phát hiện là 4% [71]. Trong gan người, AFB1 và OTA là chất cảm ứng CYP1A1, 1A2, 2B6, 2C9, 3A4 và 3A5 [72]. AFB1, cũng như phơi nhiễm OTA, tạo ra rối loạn chức năng ty thể, đặc trưng bởi sự gia tăng sản xuất ROS [14] có thể làm tăng biểu hiện TGF - 1 hoặc kích hoạt TGF tiềm ẩn - 1 [73]. Khi xem xét, bằng chứng trước đây cho thấy TGF - 1 làm giảm biểu hiện CYP1 ở người và chuột, có thể cơ chế tương tự [74] đã xảy ra trong điều kiện của chúng tôi. Tác động của việc tiếp xúc đồng thời với cả độc tố nấm mốc và các sản phẩm phụ của hạt nho và hắc mai biển có lẽ là hiệp đồng, và sự biểu hiện của CYP1A2 ở E3 thấp hơn so với E1, E2 và nhóm đối chứng. CYP1A2 được biểu hiện ở mức độ thấp hơn trong các mô ngoài gan [75].

CISTANCHE SẼ CẢI THIỆN KIDNEY / RENAL THẤT BẠI
Cácquả thậnlà anorganthatreceivesabout 25 phần trăm năng lượng tim và thanh lọc dư lượng trao đổi chất và xenobiotics từ hệ thống tuần hoàn. Trong quá trình thải này, các chất độc hại tập trung trongquả thận[76]. Trong heo conthận, sự biến đổi của biểu hiện gen CYP1A2 tương tự với mức độ biểu hiện ở gan đối với E1 và E2. Điều thú vị là ở nhóm E3, sự biểu hiện của gen này ở mức độ cao hơn so với nhóm đối chứng. Điều này có thể là do sự kích hoạt của con đường tín hiệu không hình chuẩn cho quá trình phiên mã AhR trongquả thậnô [77]. Trong gan lợn, số lượng tương đối của CYP2A19 và CYP2E1 đại diện cho 31 phần trăm tương ứng là 13 phần trăm của tổng số CYP450 [71]. Các gen CYP2A19 và CYP2E1 của lợn chịu trách nhiệm chuyển đổi sinh học cho các hợp chất nội sinh (skatole, hormone sinh dục) cũng như các hợp chất exoge-nous (thành phần thực phẩm). Cả hai loại hợp chất này đều được biểu hiện nhiều ở gan và ít hơn ởquả thậnvà mô mỡ. Phiên mã CYP2A19 được kiểm soát bởi yếu tố phiên mã CAR [78]. Trực tiếp của con người, CYP2A6 được kiểm soát bởi CAR, PXR, thụ thể glucocorticoid (GR), thụ thể estrogen, HNF 4 và PGC -1 [79]. Ngoài ra, biểu hiện gan cấu thành của CYP2A6 ở chuột bị chi phối bởi sự tác động lẫn nhau giữa HNF 4, CCAAT-hộp / protein liên kết chất tăng cường (C / EBP, C / EBP) và yếu tố phiên mã octamer -1 (Tháng 10 {{13} }) [80]. Trước đây, mối tương quan thuận giữa mRNA và mức protein đối với gen CYP2A19 đã được quan sát [81]. Không giống như các gen CYP 450 khác, CYP2A19 đóng một vai trò ít quan trọng hơn trong quá trình chuyển hóa của xenobiotics nhưng lại tham gia vào phản ứng của tế bào với căng thẳng, Nrf -2, cũng tham gia vào quá trình phiên mã CYP2A19 [82]. Gen CYP2A19 có thể có tính đa hình cao so với gen CYP2A6 [83], và có thể xảy ra sự biến đổi giữa các cá nhân rộng rãi về sản phẩm của nó. Các nghiên cứu trước đây cho thấy vịt P450 trực hệ của CYP2A6 và CYP3A4 ở động vật có vú có liên quan đến hoạt tính sinh học AFB1 thành dạng epoxit của nó [84]. Không giống như những kết quả này, trong nghiên cứu này, không có thay đổi đáng kể nào về biểu hiện gen CYP2A19 được nhận thấy ở nhóm E1 và E2, có thể là do mức độ biểu hiện cao của gen này trong gan lợn con. Hiện tại, rất khó để giải thích tại sao sự đồng tiếp xúc của cả độc tố nấm mốc và hỗn hợp hạt nho và bột hắc mai biển lại làm giảm sự biểu hiện của CYP2A19. Tuy nhiên, sự giảm biểu hiện này làm giảm nguy cơ tạo ra các chất chuyển hóa độc hại.
Ở lợnquả thận,sự biểu hiện của CYP2A19 thấp hơn so với biểu hiện ở gan [79]. Có thể là do biểu hiện thấp hơn này, việc động vật tiếp xúc với hỗn hợp hạt nho và bột hắc mai biển đã tạo ra sự điều hòa biểu hiện gen Nrf -2 gây ra CYP2A19 do hàm lượng luteolin [85] và axit ferulic [86] . Mặt khác, có bằng chứng cho thấy chỉ có hai yếu tố phiên mã, tức là yếu tố phiên mã ngược dòng của gen ovalbumin ở gà (COUP-TF1) và yếu tố nhân tế bào gan (HNF -1), có liên quan đến việc điều hòa phiên mã CYP2E1 ở lợn [87]. CYP2E1, giống như các P450 chuyển hóa xenobiotic khác, chủ yếu nằm trong màng của lưới nội chất (ER) và có thể được tạo ra trong nhiều điều kiện trao đổi chất hoặc dinh dưỡng khác nhau. Căng thẳng ER có thể được gây ra bởi căng thẳng chuyển hóa, gây ra bởi quá tải sinh tổng hợp protein / lipid và căng thẳng oxy hóa, có thể kích hoạt con đường tín hiệu nội môi phức hợp được bảo tồn tiến hóa được gọi là phản ứng protein mở ra (UPR) [88].
Có khả năng là mức mRNA CYP2E1 xấp xỉ như nhau ở nhóm E1 và nhóm chứng do các hoạt động đối kháng của axit palmitic [89], axit linoleic và -linolenic [90] đã làm tăng phiên mã gen này và các hoạt động vanillic và axit p-coumaric làm giảm nó [65]. Gần đây, người ta đã chứng minh rằng thức ăn có chứa OTA đã làm thay đổi hệ vi sinh vật đường ruột ở vịt, ảnh hưởng đến sự đa dạng và thành phần của hệ vi sinh vật manh tràng cũng như hàng rào đường ruột. Kết quả là các lipopolysaccharid có nguồn gốc từ vi khuẩn Gram âm xâm nhập vào máu và gan, gây viêm gan [91]. Trong trường hợp tổn thương gan qua trung gian miễn dịch, sự biểu hiện của CYP2E1 đã giảm [92]. Tình huống này có thể xảy ra ở nhóm E2. Có khả năng là tác động tích lũy của hai độc tố nấm mốc và các sản phẩm phụ trong chế độ ăn uống đã làm giảm sự biểu hiện của CYP2E1 trong gan của nhóm E3. bên trongquả thận,các axit béo tự do, chẳng hạn như palmitate, oleate và linoleate, được lưu trữ trong nephron [93], và các axit này có thể làm tăng sự biểu hiện của gen CYP2E1 trongthậncủa nhóm E1 so với mức đối chứng. Theo Pfohl-Leszkowicz và Manderville [25], OTA hình thành adduct với DNA, tạo rathậnđộc tính di truyền và sinh ung thư. Có khả năng là mức độ cao của OTA kích thích biểu hiện gen CYP2E1 trongthậncủa nhóm E2 so với mức đối chứng. Trong nhóm E3, có vẻ như việc sử dụng đồng thời hai độc tố nấm mốc và các sản phẩm phụ trong chế độ ăn uống có tác dụng đối kháng, với sự biểu hiện của gen CYP2E1 trở lại mức kiểm soát. Hơn nữa, đánh giá mô học đối với nhóm E3 cho thấy rằng hỗn hợp sản phẩm phụ có nguồn gốc từ hạt nho và dầu hắc mai biển làm giảm tác hại gây ra bởi aflatoxin B1 và ochratoxin A ở gan vàthậnmức độ ở heo con sau cai sữa. CYP2E1, giống như các P450 chuyển hóa xenobiotic khác, chủ yếu nằm trong màng của ER và có thể được tạo ra trong nhiều điều kiện chuyển hóa hoặc dinh dưỡng khác nhau [89]. Sự điều hòa của gen CYP2E1 trong nhóm E1 có thể là do quá trình hydroxyl hóa các hợp chất có nguồn gốc từ coumarin được xúc tác bởi các enzym CYP2A, được coi là chất chỉ thị cụ thể cho sự hiện diện của các enzym CYP2 [94], với p-coumaric axit có trong hạt nho và các sản phẩm phụ từ hắc mai biển.
Đối với lợn, người ta biết rất ít về sự hiện diện của các enzym CYP3As trongmô thận,và không có gì được biết về khả năng cảm ứng của chúng [95]. Một số gen đã được xác định trong phân họ CYP3A của động vật có vú (ví dụ, 5 gen ở chuột và 4 gen ở người), nhưng sự biểu hiện của các gen này ởmô thậnđã được điều tra kém [96]. Về biểu hiện gen, Ayed-Boussema et al. (2012) [63] và Gonzalez-Arias et al. [97] đã mô tả sự gia tăng mức độ biểu hiện trong tất cả các cytochromes được xét nghiệm (CYP3A4, 2B6, 3A5 và 2C9) trong nuôi cấy tế bào gan người sơ cấp. Các nghiên cứu trước đây đã báo cáo các kết quả khác nhau về tác dụng của AFB1 và OTA trong tế bào gan người được nuôi cấy chính, trong đó việc tăng nồng độ của các độc tố nấm mốc này rõ ràng gây ra nồng độ mRNA CYP3A4 và CYP2B6 phụ thuộc vào liều lượng [63]. Ngược lại, người ta đã phát hiện ra rằng khi có OTA và AFB1 trong gan (Hình 3, nhómE2), thì mức độ biểu hiện của biểu hiện bị tăng lên, có lẽ do sự kích hoạt của AhR [98]. Những dữ liệu này khác với dữ liệu của Zepnik et al. [99], người đã báo cáo sự gia tăng quá trình thủy phân OTA bởi các enzyme microomal từ gan chuột, đặc biệt đối với P 450 3 A1 / 2 và 3A4, cho thấy rằng biểu hiện gen này được điều chỉnh theo cách phụ thuộc vào loài. Trong một số trường hợp, sự ức chế các enzym P450 bởi polyphenol có thể có tác dụng ngăn ngừa hóa học do khả năng kích hoạt các chất gây ung thư bởi các enzym P450 trong quá trình hoạt động trao đổi chất tự nhiên của chúng. Sự ức chế các enzym giai đoạn I chuyển hóa xenobiotic có thể là một trong những mục tiêu của tác dụng phòng ngừa hóa trị của polyphenol vòng xuất hiện tự nhiên. Sự gia tăng CYP4A24 được quan sát thấy ở gan có thể là một phản ứng sinh lý trong bối cảnh bất thường của sự tích tụ lipid không bình thường và không có hoạt động của CYP2E1, do thực tế là CYP2E1 và CYP4A là các tế bào vi mô gan cảm ứng P -450 liên quan đến quá trình hydroxyl hóa chất béo axit, và cả hai đều có thể bắt đầu quá trình tự động lan truyền của quá trình peroxy hóa lipid. Chúng có thể bổ sung cho nhau, dẫn đến tương tác trong việc điều hòa các enzym riêng lẻ [100]. Do đó, rõ ràng là protein CYP4A là trung gian chính trong phản ứng thích ứng với sự xáo trộn chuyển hóa lipid ở gan [101]. Mức CYP4A24 giảm trongquả thậncó thể dẫn đến các tác động độc hại được tạo ra ở gan do chế độ ăn nhiễm độc tố nấm mốc, có nghĩa là CYP4A24 điều chỉnh căng thẳng ER ở gan [102,103].

CISTANCHE SẼ CẢI THIỆN ĐAU KIDNEY / RENAL
Trong nghiên cứu này, việc bổ sung hỗn hợp bột hạt nho và bột hắc mai biển đã làm tăng mức độ biểu hiện trongquả thận,điều này được cho là sẽ hỗ trợ các quá trình loại bỏ và duy trì sự cân bằng của các chất nội bào [104]. Hơn nữa, OTA được hấp thụ trong ruột nơi protein kháng đa thuốc 2 (gen MRP2) đóng một vai trò quan trọng, hoạt động như một chất vận chuyển xenobiotic ra ngoài để giảm sinh khả dụng qua đường miệng và tải lượng độc tố đến các cơ quan và do đó, độc tính của OTA. Một khi OTA đi đến máu, nó có thể đến các cơ quan khác như gan, và chất vận chuyển MRP2 lại là chất vận chuyển tích cực chính quan trọng tham gia vào quá trình liên hợp anion và đẩy xenobiotic vào không gian ngoại bào, góp phần hình thành mật và loại bỏ độc tố sau đó [ 97, 105]. Ngoài ra, chất vận chuyển MRP2 có trong màng đỉnh của tế bào ruột,quả thận-các ống gần, và các tế bào khác [105]. Độc tính của OTA được cho là do gốc isocoumarin của nó, và người ta đã biết rõ rằng OTA bị bất hoạt hoặc kích hoạt sinh học bởi các enzym cytochrom P450 [29]. Trước đây, sự hiện diện của OTA trong thức ăn chăn nuôi có liên quan đến sự phát triển của độc tính trên thận, ở chuột, có liên quan đếnthậnu tuyến vàquả thậnkhối u [97]. Trong nghiên cứu này, sự giảm biểu hiện MRP2 trong gan đã được tìm thấy, cho thấy sự suy giảm bài tiết độc tố nấm mốc ở nhóm E2.
Ở chuột, OTA được quan sát thấy bài tiết ít hơn 15% trong các ống gần củaquả thận,trong khi sự vận chuyển axit amin ở ống gần không bị suy giảm [97, 106]. Do đó, sự giảm MRP2 trong gan được tìm thấy trong nghiên cứu này có thể là cơ chế mà độc tố nấm mốc đạt đến tỷ lệ phần trăm sinh khả dụng cao trên cơ thể sống. Bằng cách này, sự phơi nhiễm AFB1 và OTA của heo con sẽ được tăng lên, góp phần gây độc cho gan. Xét khả năng gây độc cho thận của OTA và AFB1, sự giảm sản phẩm gen MRP2 cũng có thể có tác động lớn đến ống lượn gần, dẫn đến giảm khả năng đào thải OTA [97]. Tuy nhiên, cần có những nghiên cứu sâu hơn về cơ chế vận chuyển AFB1 và OTA để hỗ trợ giả thuyết này. Trong giai đoạn II của quá trình giải độc trao đổi chất, hợp chất xenobiotic ban đầu hoặc các chất chuyển hóa trung gian được sửa đổi trong giai đoạn I được liên hợp để phù hợp cho quá trình bài tiết. Glutathione S transferase (GSTs) và UDP glycurosyltranferase (UGTs) góp phần vào quá trình xử lý Giai đoạn II [107].
Với sự hiện diện của hỗn hợp các phụ phẩm từ hạt nho và bột hắc mai biển trong thức ăn cho lợn, mức độ biểu hiện GSTA1 trong gan tăng lên đáng kể, có thể do yếu tố đáp ứng với chất chống oxy hóa (ARE) và yếu tố đáp ứng -NF (-NF-RE), tương ứng, với sự có mặt của chất chống oxy hóa phenolic, kích hoạt các đồng dạng GST mà không cần các thụ thể aryl hydrocacbon (Ah) [108]. Đáng ngạc nhiên là trong nghiên cứu của Ghadiri et al. (2019) [109], sự điều hòa mRNA qua trung gian AFB 1- của GSTA1 đã được quan sát thấy trong gan bò với sự hiện diện của chất chống oxy hóa. Các nghiên cứu trước đây [110] cho thấy rằng OTA và AFB1 cạnh tranh cho cùng các enzym CYP450 đại diện cho con đường kích hoạt sinh học của AFB1, với ít sản phẩm bổ sung AFB 1- ADN được tạo ra. Do sự cạnh tranh này, AFB1 có thể được liên hợp với glutathione giảm trong một phản ứng được xúc tác bởi các enzym GST, với các gen mã hóa của chúng được điều chỉnh. AFB1 có thể tham gia vào các dạng phản ứng giai đoạn II khác, tức là glucuronidationa hóa và sulfat hóa, trong khi OTA chủ yếu liên hợp với glutathione đã khử [72]. Hơn nữa, để phản ứng với việc sử dụng đồng thời ở lợn, thức ăn chứa hai độc tố nấm mốc (AFB1 và OTA) đã làm tăng việc tạo ra các dấu ấn sinh học stress oxy hóa. Do đó, các cơ chế bảo vệ đã được kích hoạt, thúc đẩy sự thích nghi và tồn tại để phản ứng với stress oxy hóa [111]. Ví dụ, ROS và các chất oxy hóa có thể kích hoạt quá trình phiên mã các đồng dạng GST thông qua ARE [108], như được quan sát thấy ở cả gan vàthậnthông qua sự gia tăng mức độ biểu hiện của gen GSTA1.
Kết luận
Dữ liệu của chúng tôi cho thấy sự tồn tại của sự khác biệt giữa cácquả thậnvà gan liên quan đến phản ứng chống lại cả độc tố nấm mốc và các sản phẩm phụ được sử dụng trong nghiên cứu này. Nói chung, các sản phẩm phụ có tác dụng chống oxy hóa làm giảm sự biểu hiện của mRNA CYPs được phân tích trong gan và làm tăng chúng trongquả thận. Ngoài ra, ở cả hai cơ quan, sự đồng tiếp xúc của lợn con với OTA và AFB1 tạo ra sự tăng hoặc giảm biểu hiện gen phụ thuộc vào loại gen. Việc bao gồm bột hạt nho và bột hắc mai biển trong khẩu phần ăn của lợn say OTA và AFB 1- làm giảm biểu hiện gen CYP P450, cho thấy sự giảm hoạt tính sinh học của các độc tố nấm mốc này, có thể dẫn đến giảm độc tính ở cả hai cơ quan, vì nghiên cứu mô học đã tiết lộ. Những phát hiện này cho thấy chất thải bột hạt nho và bột hắc mai biển là một nguồn đầy hứa hẹn trong việc chống lại tác hại của ochratoxin A và aflatoxin B1. Mặc dù cần phải làm việc thêm để làm sáng tỏ cơ chế mà các sản phẩm phụ của hạt nho và hắc mai biển ảnh hưởng đến chuyển đổi sinh học AFB1 và OTA, và do đó tạo ra các chất chuyển hóa độc hại, các tác dụng bảo vệ dường như ít nhất một phần qua trung gian của việc tăng cường bảo vệ chống oxy hóa ở gan vàquả thậnmức độ.
Nguyên liệu và phương pháp
Thiết kế thử nghiệm và Bộ sưu tập mẫuBốn mươi con lai TOPIGS -40 lai (♀ Large White × Lai (Large White × Pietrain) × ♂ Talent, chủ yếu là Duroc) heo con sau khi cai sữa có trọng lượng cơ thể trung bình là 9,11 ± 0. {16 }} 3 kg được giao cho ba nhóm thí nghiệm (E1, E2, E3) và một nhóm đối chứng (C), nhốt trong chuồng (hai lần lặp lại 5 con lợn mỗi chuồng cho mỗi nghiệm thức) và được cho ăn bằng khẩu phần thực nghiệm cho 3 {{19} } ngày. Thức ăn và nước được cung cấp libitum trong quá trình thử nghiệm. Chế độ ăn cơ bản được dùng để kiểm soát và chứa thức ăn hỗn hợp bình thường cho lợn con mới bắt đầu không có độc tố nấm mốc (ngô 68,46%, bột đậu nành 19%, gluten ngô 4%, chất thay thế sữa 5%, L-lysine 0. 3%, DL-methionine 0. 1 phần trăm, đá vôi 1,57 phần trăm, monocalcium phosphate 0. 35 phần trăm, muối 0,1 phần trăm, hỗn hợp choline 0,1 phần trăm và 1 phần trăm vitamin-khoáng chất). Các nhóm thí nghiệm được cho ăn như sau: E1 - chế độ ăn cơ bản cộng với hỗn hợp (1: 1) của hai sản phẩm phụ (hạt nho và bột hắc mai biển) theo tỷ lệ 5% bằng cách thay thế bột ngô và bột đậu nành; E2 — chế độ ăn cơ bản bị nhiễm độc tố nấm mốc (hỗn hợp 62 ppb aflatoxin B 1- AFB1 và 479 ppb ochratoxin A-OTA); và E3 - chế độ ăn cơ bản chứa 5% hỗn hợp (1: 1) bột hạt nho và hắc mai biển và không bị ô nhiễm hỗn hợp AFB1 và OTA. Hỗn hợp độc tố nấm mốc OTA và AFB1 được cung cấp bởi Tiến sĩ Boudra và Tiến sĩ Morgavi từ INR A, Trung tâm Clermont Ferrand, và được sản xuất bằng cách trồng Aspergillus flavus và Aspergillus ochraceous trên lúa mì như đã được Boudra et al mô tả. [112]. Vật liệu bị ô nhiễm thu được được đưa vào chế độ ăn cho nhóm E2 và E3, dẫn đến nồng độ cuối cùng là 479 ppb OTA và 62 ppb AFB1. Động vật từ tất cả các nhóm thí nghiệm được tiếp cận miễn phí thức ăn và nước xử lý mỗi ngày trong giai đoạn thí nghiệm (30 ngày). Bữa ăn hạt nho và bột hắc mai biển được cung cấp bởi hai thương mại địa phương, SC OLEOMET-SRL và BIOCATINA, Bucharest, Romania. Sau 4 tuần, những con vật được giết mổ với sự chấp thuận của Ủy ban Đạo đức của Viện Nghiên cứu-Phát triển Quốc gia về Dinh dưỡng và Sinh học Động vật, Balote s, ti, Romania (Ủy ban Đạo đức số 118 / 02.12.2019) và theo quy định của Luật Romania 206/2004 và Chỉ thị 98/58 / EC của Hội đồng EU về xử lý và bảo vệ động vật được sử dụng cho mục đích thí nghiệm. Vào cuối giai đoạn thử nghiệm của nghiên cứu này, các thông số năng suất, trọng lượng và tiêu thụ thức ăn đã được đo lường. Gan vàquả thậnCác mẫu được thu thập từ bốn con cho mỗi nhóm và được tưới bằng dung dịch nước muối lạnh để loại bỏ máu. Các mảnh vỡ ~ 50 mg từ thùy gan phải vàthậnvỏ não (ba cái từ mỗi cái) được thu thập trong Thuốc thử ổn định RNAlater (Qiagen, Germantown, Maryland) và sau đó được bảo quản ở - 80 ◦ C cho đến bước phân lập RNA. Vì lý do đạo đức, việc sử dụng tối đa từng loài động vật, giảm thiểu thiệt hại về động vật, và phân tích thống kê, số lượng cá thể đã giảm càng nhiều càng tốt về mặt khoa học. Khoa học tốt và thiết kế thí nghiệm tốt giúp giảm số lượng động vật được sử dụng trong bất kỳ nghiên cứu nào, cho phép các nhà khoa học thu thập dữ liệu bằng cách sử dụng số lượng động vật tối thiểu cần thiết [113].

Đặc tính nguồn cấp dữ liệuKhẩu phần thức ăn chăn nuôi được phân tích thành phần hóa học cơ bản (chất khô, protein thô, chất béo thô, xơ thô và tro) theo phương pháp của Tổ chức Tiêu chuẩn Quốc tế (SR ISO 6496/2001, Standardized Bulletin (2010). Http: // www. asro.ro (truy cập vào ngày 13 tháng 2 năm 2021)). Các hợp chất hoạt tính sinh học từ các sản phẩm phụ của bữa ăn, chẳng hạn như polyphenol, axit béo không bão hòa đa (PUFA) và khoáng chất, được xác định bằng phản ứng Folin-Ciocalteu, HPLC-UV-Vis, và sắc ký khí như được mô tả bởi các tác giả của [113, 114]. Hoạt tính chống oxy hóa được xác định bằng phương pháp DPPH như đã được các tác giả của [115] mô tả trước đây.
Phân tích dấu ấn sinh học PlasmaVào ngày 30, các mẫu máu được thu thập vô trùng từ lợn con đã nhịn ăn. Các điểm đánh dấu phản ánh chức năng của gan (aspartate transaminase-AST, alanin transaminase-ALT, gamma glutamyl transferase-GGT, tổng số protein, phosphatase kiềm-AKL) và thận (albumin, creatinine) được xác định sau khi ly tâm máu bằng máy xét nghiệm Hóa học lâm sàng máy phân tích Horiba Medical — ABX Pentra 400, (Irvine, CA, Hoa Kỳ).
Kiểm tra bằng kính hiển vi ánh sángGan vàquả thậnsinh thiết được cố định trong dung dịch formaldehyde có đệm photphat 4%, được khử nước, làm rõ và được đưa vào các khối parafin. Các phần 5 µ m được xử lý thường xuyên để nhuộm hematoxylin-eosin và Gomori trichrome (Leica Biosystems, 38016SS1, Nussloch, Germany) tương ứng theo quy trình của Leica. Các phần hiển vi được phân tích bằng kính hiển vi Olympus BX43 được trang bị máy ảnh kỹ thuật số Olympus XC30. Các thay đổi mô bệnh học của gan vàquả thậnđược phân loại theo mức độ nghiêm trọng của tổn thương thuộc nhóm 1–4, như đã mô tả trước đây [116]. Đối với gan, độ 1: Bình thường; độ 2: Tế bào gan bình thường, hình sin giãn nhẹ và xung huyết; độ 3: Tế bào gan thiếu dịch, hình sin giãn ra và sung huyết; tăng sinh collagen vừa phải; độ 4: Hoại tử, thâm nhiễm viêm, tăng sinh collagen. Đối với thận, độ 1: Bình thường; lớp 2: Tổn thương nhẹ ở ống thận / cầu thận, viêm và tăng sinh collagen; mức độ 3: Tổn thương ống thận / cầu thận nhẹ, viêm và tăng sinh collagen; lớp 4: Tổn thương ống thận / cầu thận rõ rệt, viêm và tăng sinh collagen. "Giá trị đánh giá trung bình" (MAV) được tính là giá trị trung bình của tất cả dữ liệu cho mỗi nhóm thử nghiệm.
Phân lập RNAViệc phân lập RNA tổng số được thực hiện từ 10 mg mô bằng cách sử dụng RNeasy Plus Universal Mini Kit (Qiagen) theo quy trình của nhà sản xuất. Hơn nữa, nó bao gồm bước phân hủy DNase trên cột. Sau khi phân lập RNA, các phần nhỏ đã được thực hiện để ngăn chặn sự suy thoái do chu trình đông lạnh-tan băng gây ra. Nồng độ và độ tinh khiết của RNA tổng số được xác định bằng máy quang phổ NanoDrop 8000 (Thermo Scientific, Wilmington, DE, USA).
Số toàn vẹn RNA (RIN)Giá trị RIN của các mẫu RNA được xác định bằng cách sử dụng Agilent RNA 6000 NanoKit (Agilent, Santa Clara, CA, USA) và Agilent 2100 Bioanalyzer theo quy trình của nhà sản xuất. Các mẫu có giá trị RIN nhỏ hơn 8 không được đưa vào phân tích thêm và các bước phân lập được lặp lại.
Phiên mã ngượcĐể tổng hợp cDNA, 1000 ng RNA tổng số đã được phiên mã ngược bằng cách sử dụng bộ tổng hợp iScript cDNA (Bio-Rad, Hercules, CA, USA). Hỗn hợp phản ứng 4 µ L và 1 µ L men sao chép ngược được trộn với mẫu RNA 1 µ L và hoàn thành với nước tự do RNase đến tổng thể tích là 20 µ L. Nồng độ cuối cùng của RNA là 1000 ng cho mỗi phản ứng. Phản ứng được thực hiện bằng máy tuần hoàn nhiệt giếng Veriti 96- (Hệ thống sinh học ứng dụng, Thành phố Foster, CA, Hoa Kỳ) với chương trình sau: Một chu kỳ 25 ° C trong 5 phút, một chu kỳ 42◦ C trong 30 phút và một chu kỳ 85 ◦ C trong 5 phút. Nồng độ và độ tinh khiết của các mẫu cDNA được xác định bằng máy quang phổ NanoDrop 8000 (Thermo Scientific).
Thiết kế lớp lótDo thiếu dữ liệu liên quan đến các gen liên quan đến độc tính gan-thận khi phơi nhiễm độc tố nấm mốc của lợn cai sữa, trình tự mồi (Bảng 7) được thiết kế bằng silico bằng cách sử dụng Primer3Plus [59] và được xác minh bởi chương trình BLAST [117]. Những gen có độ đặc hiệu cao nhất cho trình tự đích được chọn để khuếch đại các gen CYP1A2, CYP2A19, CYP2E1, CYP3A29, CYP4A24, MRP2 và GSTA1 và ba gen tham chiếu mã hóa cho protein liên kết hộp TATA, protein ribosome L4 và beta { {19}} microglobulin trong Sus scrofa. Nhiệt độ ủ của mồi được xác định bằng PCR gradient nhiệt độ.
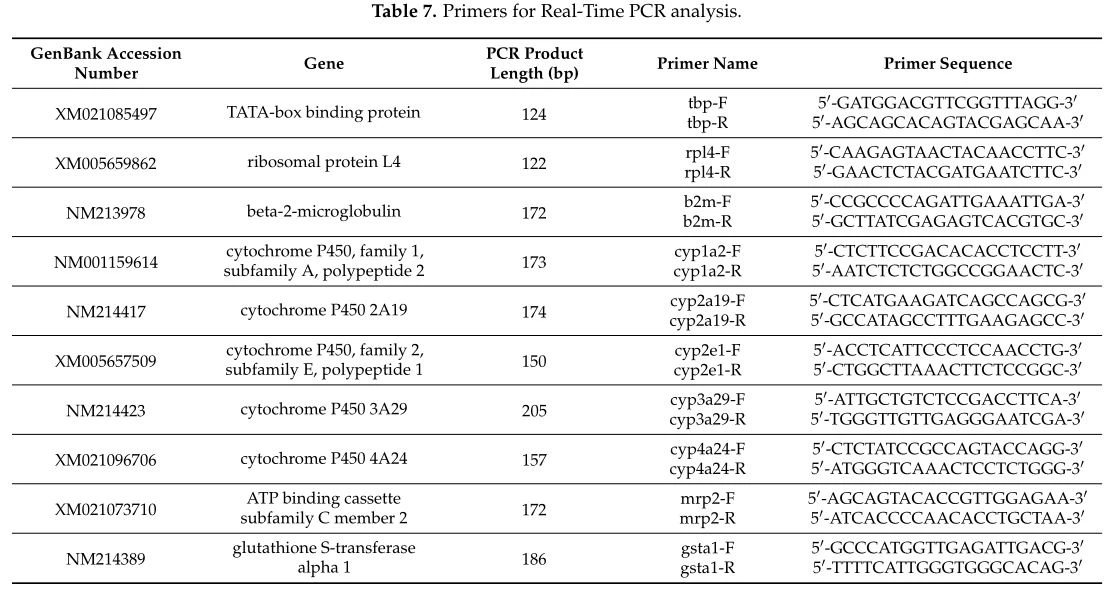
PCR thời gian thựcPhản ứng PCR thời gian thực được thực hiện trên Hệ thống phát hiện PCR thời gian thực iCycler iQ (Bio-Rad) sử dụng iQ SYBR Green SuperMix (Bio-Rad). Trong 96- đĩa giếng, 1 µ L trên 1 {{1 0}} 0 ng / µ L cDNA, 12,5 µ L iQ SYBR Green SuperMix (Bio-Rad), 0,5 µ L của mồi thuận 20 pmol / µ L, 0,5 µ L 20 pmol / µ L mồi ngược, và 10,5 µ L nước MilliQ được thêm vào. Tổng âm lượng là 25 µ L. Chương trình khuếch đại bao gồm 1 chu kỳ 95 ◦ C trong 5 phút, 45 chu kỳ 95 ◦ C trong 30 giây 55/56 ◦ C trong 30 giây, 72 ◦ C trong 45 giây, và 85 chu kỳ ở 55 ° C, với sự tăng nhiệt độ điểm đặt thêm 0,5 ° C mỗi chu kỳ trong 10 s. Các mẫu đã được chạy và các giá trị chu kỳ ngưỡng (Ct) đã được ghi lại. Các đường cong nóng chảy cũng được thực hiện.
Phân tích dữ liệuCác giá trị Ct được xử lý như đã nêu trong "Hướng dẫn MIQE: Thông tin tối thiểu để công bố các thử nghiệm PCR định lượng trong thời gian thực" [118] bằng cách sử dụng OpenOffice Calc theo phương pháp 2- ∆∆ Ct được mô tả bởi Livak và Schmittgen (2001 ) [119]. Các gen tham chiếu (TBP, RPL4 và B2M) được chọn để được biểu hiện ổn định trên các loại mô và phương pháp điều trị khác nhau trên mẫu vật lợn [120, 121]. Giá trị biểu thức tương đối (2 - ∆∆Ct) nhận được bằng cách chuẩn hóa, trừ đi trung bình cộng của các gen tham chiếu từ mỗi gen quan tâm. Các lần lặp kỹ thuật được tính trung bình trước khi phân tích thống kê. Dữ liệu được minh họa dưới dạng giá trị trung bình của các nhóm (n=4) ± độ lệch sai số chuẩn của giá trị trung bình (STDEV). Tất cả dữ liệu được phân tích thống kê bằng phương pháp ANOVA một chiều được thực hiện với phần mềm GraphPad Prism 3.03 (GraphPad Software, La Jolla, CA, USA). Các so sánh hậu kỳ giữa tất cả các nhóm được thực hiện bằng cách sử dụng thử nghiệm Bonferroni. Ý nghĩa thống kê (giá trị p) được trình bày cho tất cả các nhóm trái ngược với nhóm Đối chứng (C).
