Các yếu tố rủi ro và tác động liên quan đến quá trình khoáng hóa thận trong bệnh thận mãn tính ở mèo
Jul 24, 2023
TRỪU TƯỢNG
1. Bối cảnh
Nephrocalcinosis là một đặc điểm bệnh lý của bệnh thận mãn tính (CKD). Ý nghĩa sinh lý bệnh học của nó đối với mèo bị CKD vẫn chưa được khám phá.
2. Mục tiêu
Xác định các yếu tố nguy cơ gây ra bệnh canxi hóa thận và đánh giá ảnh hưởng của chúng đối với sự tiến triển của CKD và tỷ lệ tử vong do mọi nguyên nhân.
3. Động vật
Năm mươi mốt con mèo do khách hàng sở hữu tuyến giáp bình thường mắc bệnh CKD thiếu azotemia của Hiệp hội Lợi ích Thận Quốc tế (IRIS) ở giai đoạn 2-3.
4. Phương pháp
Nghiên cứu thuần tập hồi cứu. Các phần thận mô bệnh học được đánh giá để tìm canxi thận (nhuộm von Kossa). Mức độ nghiêm trọng của bệnh canxi hóa thận được xác định bằng phân tích hình ảnh (ImageJ). Hồi quy logistic thông thường đã được thực hiện để xác định các yếu tố nguy cơ gây bệnh thận. Ảnh hưởng của bệnh canxi hóa thận đối với sự tiến triển của CKD và nguy cơ tử vong được đánh giá bằng cách sử dụng mô hình hỗn hợp tuyến tính và hồi quy Cox, tương ứng. Mèo được phân loại theo lượng tiêu thụ trong chế độ ăn hạn chế phốt phát (PRD) trung bình theo thời gian do chủ sở hữu báo cáo, trong đó PRD bao gồm Lớn hơn hoặc bằng 50 phần trăm , 10-50 phần trăm hoặc không có lượng thức ăn nào.
5. Kết quả
Nhiễm canxi thận được đánh giá là từ nhẹ đến nặng ở 78,4% và từ nhẹ đến tối thiểu ở 21,6% trường hợp. Nồng độ canxi toàn phần trong huyết tương ban đầu cao hơn (tCa; tỷ lệ chênh lệch [OR]=3.07 trên 1 mg/dL; P=.02) và ăn PRD (10 phần trăm -50 phần trăm : OR=8.35; P=.01; Lớn hơn hoặc bằng 50 phần trăm : OR {{20 }}.47; P=.01) là các yếu tố nguy cơ gây bệnh canxi hóa thận độc lập. Những con mèo mắc bệnh thận không có canxi đến mức tối thiểu đã tăng creatinine huyết tương (0,250 ± 0,074 mg/dL/tháng; P=0,002), urê (5,06 ± 1,82 mg/dL/tháng; P=. 01) và nồng độ phốt phát (0,233 ± 0,115 mg/dL/tháng; P=.05) trong hơn 1 năm và có thời gian sống sót trung bình ngắn hơn so với mèo mắc bệnh canxi hóa thận từ nhẹ đến nặng.
6. Kết luận và tầm quan trọng lâm sàng
TCa huyết tương cao hơn khi chẩn đoán CKD và lượng PRD có liên quan độc lập với bệnh thận. Tuy nhiên, bệnh canxi hóa thận không liên quan đến sự tiến triển nhanh chóng của CKD ở mèo.

Nhấn vào đây để biết tác dụng của Cistanche đối với thận là gì
TỪ KHÓA
vôi hóa, CKD-MBD, tăng canxi máu, nhiễm canxi thận.
GIỚI THIỆU
Rối loạn chuyển hóa chất khoáng và xương xuất hiện ở mèo mắc bệnh thận mãn tính (CKD), ngay cả trong giai đoạn đầu của bệnh.1,2 Thận đóng vai trò cơ bản trong cân bằng nội môi canxi và phốt phát. Sự giảm dần chức năng của các nephron trong CKD dẫn đến hiện tượng giữ lại phốt phát, kích thích 3 hormone phosphaturic, yếu tố tăng trưởng nguyên bào sợi 23 (FGF23) và sau đó là hormone tuyến cận giáp (PTH), để duy trì nồng độ phốt phát sinh lý trong huyết tương.4-6 Tuy nhiên, không chỉ có vậy phản ứng thích ứng này có ảnh hưởng đến quá trình điều hòa chuyển hóa canxi mà còn cả quá trình tu sửa xương hay không. Khi phản ứng thích nghi này cuối cùng không ngăn được nồng độ phốt phát trong huyết tương tăng lên, nó sẽ thúc đẩy vôi hóa ngoài tử cung. Những phản ứng thích ứng này được gọi chung là bệnh thận mãn tính-rối loạn khoáng chất và xương (CKD-MBD).7
Bệnh canxi hóa thận được đặc trưng bởi sự lắng đọng tinh thể canxi photphat (CaP) hoặc canxi oxalat (CaOx) ở ống kẽ thận,8 ở người hầu như chỉ có ở tủy thận.9 Quá trình này bắt đầu từ sự hình thành các mảng Randall ở nhú thận, hoạt động như một điểm yếu cho quá trình vôi hóa tiến triển .9,10 Quan sát hiện tượng này trên kính hiển vi ánh sáng được gọi là bệnh canxi hóa thận vi thể (ở đây gọi là bệnh canxi hóa thận).8,11 Sự vôi hóa ngoài tử cung tự phát có thể được giải thích một phần là do muối canxi và phốt phát kết tủa từ chất lỏng siêu bão hòa khi sản phẩm canxi phốt phát (CaPP) vượt quá tích số tan. Các nghiên cứu trước đây cho thấy rằng nồng độ phốt phát trong huyết thanh và CaPP tăng có tương quan thuận với hàm lượng canxi trong thận,12,13 và nồng độ canxi trong huyết thanh tăng là một yếu tố nguy cơ độc lập đối với bệnh canxi hóa thận ở bệnh nhân CKD ở người.11 Bệnh canxi hóa thận phổ biến ở người và mèo mắc bệnh CKD.14, 15 Sự lắng đọng canxi ở thận đã được tìm thấy trên mô học ở Lớn hơn hoặc bằng 50 phần trăm số mèo có Hiệp hội Lợi ích Thận Quốc tế (IRIS) Giai đoạn 2 đến 4, so với 21 phần trăm ở những con mèo không bị thiếu azotemia.15 In vivo ở chuột, hàm lượng canxi trong thận có tương quan nghịch với độ thanh thải creatinine, cho thấy tác động có hại đến chức năng thận.13,16
Mèo mắc bệnh CKD có nguy cơ cao mắc chứng tăng calci huyết toàn phần trong huyết tương, với tỷ lệ mắc bệnh ngày càng tăng khi tăng ure máu.17 Ở những con mèo mắc bệnh CKD ăn chế độ ăn hạn chế phốt phát (PRD), việc tăng nồng độ phốt phát trong huyết tương và tổng lượng canxi (tCa) có liên quan đến sự tiến triển của bệnh CKD. 18 Tuy nhiên, vẫn còn phải xác định xem rối loạn cân bằng nội môi canxi và phốt phát có đóng vai trò trong sinh bệnh học bệnh canxi hóa thận hay không. Hơn nữa, tác động của bệnh canxi hóa thận liên quan đến CKD ở mèo vẫn chưa được nghiên cứu. Mục tiêu nghiên cứu của chúng tôi là: (a) khám phá các yếu tố rủi ro đối với bệnh canxi hóa thận ở mèo CKD và (b) đánh giá mối liên quan của bệnh canxi hóa thận với những thay đổi về thông số CKD-MBD, tiến triển của CKD và tỷ lệ tử vong do mọi nguyên nhân.

Cistache tubulosa
PHƯƠNG PHÁP
1. Lựa chọn trường hợp
Hồ sơ của 2 thực hành lấy ý kiến đầu tiên có trụ sở tại Luân Đôn từ ngày 1 tháng 1 năm 1992 đến ngày 31 tháng 12 năm 2017 đã được xem xét và những con mèo CKD thiếu azotemia đã trải qua các cuộc khám nghiệm tử thi hoàn chỉnh đã được xác định. Chẩn đoán CKD thiếu máu được định nghĩa là nồng độ creatinine huyết tương Lớn hơn hoặc bằng 2 mg/dL với trọng lượng riêng nước tiểu (USG)<1.035, or plasma creatinine concentration ≥2 mg/dL on 2 consecutive occasions 2-4 weeks apart without evidence of a pre-renal cause. All cats with a CKD diagnosis were offered a PRD. A variety of PRD was used throughout the study (Feline Low Protein Diet [wet]; Masterfoods, Bruck, Austria; Waltham Veterinary Diet, Feline Low Phosphorus Low Protein [dry and wet]; Effem, Minden, Germany [dry] and Masterfoods, Bruck, Austria [wet]; Feline Veterinary Diet Renal [dry and wet], Royal Canin SAS, Aimargues, France [dry] and Masterfoods, Bruck, Austria [wet]) with a phosphorus content of 0.7-1.1 g/Mcal and calcium-to phosphorus ratio (Ca:P) of 1.3-2.1. Cats not accepting a PRD continued on their maintenance diets.
Inclusion required a formalin-fixed paraffin-embedded (FFPE) kidney block for histopathological evaluation. Cats were excluded if they had clinically suspected hyperthyroidism and their plasma total thyroxine (TT4) concentration was >40 nmol/L, họ đang được điều trị y tế cho bệnh cường giáp, có bằng chứng về một bệnh đồng thời khác hoặc đang được điều trị bằng corticosteroid, furosemide hoặc bisphosphonates. Những con mèo mắc IRIS CKD giai đoạn 4 khi được chẩn đoán và những con mèo không được tái khám sau khi chẩn đoán CKD cũng bị loại trừ. Những con mèo nhận amlodipine besylate để điều trị tăng huyết áp toàn thân cũng được đưa vào.
2. Dữ liệu lâm sàng
Các mẫu máu, nước tiểu và khám nghiệm tử thi được thu thập với sự đồng ý của chủ sở hữu và sự chấp thuận của Ủy ban Phúc lợi và Đạo đức của Trường Cao đẳng Thú y Hoàng gia (URN20131258E). Các mẫu máu được thu thập bằng cách chọc tĩnh mạch cổ vào các ống chứa axit heparin và ethylenediaminetetraacetic (EDTA) và nước tiểu được lấy bằng chọc dò bàng quang. Mẫu được bảo quản ở 4 C trong thời gian<6 hours before centrifugation and separation. Heparinized plasma was analyzed biochemically at an external laboratory (IDEXX laboratories, Wetherby, UK). Inhouse urinalyses, including USG measurement by refractometry, dipstick chemical analysis, and microscopic urine sediment examination, were performed on the day of collection. Urinary tract infection was confirmed by bacterial culture (Royal Veterinary College Diagnostic Laboratory Services, Hatfield, UK).
Systolic blood pressure (SBP) measurements were made as previously described by Doppler.19 Indirect ophthalmoscopy was performed using a retinal camera (ClearView, Optibrand, Fort Collins, Colorado) in cats with an average SBP >160 mm Hg. Systemic hypertension was defined as an average SBP >160 mm Hg in conjunction with ocular pathology consistent with hypertensive damage, or SBP >170 mm Hg trong 2 lần liên tiếp.
Clinical records were reviewed to extract the following: age, sex, breed, body weight, SBP, tCa, ionized calcium (iCa), plasma creatinine, urea, phosphate, potassium, sodium, chloride, total protein, albumin, and TT4 concentrations, plasma alanine aminotransferase (ALT) and alkaline phosphatase (ALP) activities, PCV, USG, and urine culture results. The proportion of PRD recorded as being fed at every visit (until death) from each cat with PRD prescribed after CKD diagnosis was reviewed from our clinical records. Owners were asked at each visit to estimate the proportion of PRD by volume of the total quantity of food fed. A time-averaged proportion of PRD fed by volume of the total ration was calculated from this estimate for each cat. Where the proportion fed was missing from the record at a particular visit, the proportion stated at the previous visit was imputed, except if it was the visit at which euthanasia was recommended and the cat had deteriorated clinically from the previous visit. Cats were categorized according to the time-averaged ingestion of PRD, where PRD comprised ≥50%, >10 phần trăm ,<50%, or none of their food intake for their CKD duration.

bổ sung nước tiểu
3. Dữ liệu mô bệnh học
Các cuộc kiểm tra khám nghiệm tử thi đã được cung cấp cho tất cả các khách hàng khi mèo của họ bị chết và nhận được sự đồng ý từ những người đồng ý. Khi khám nghiệm tử thi, mỗi quả thận được mổ xẻ theo chiều dọc và chiều ngang và cố định (10 phần trăm formalin đệm trung tính). Các mô thận cố định bằng formalin (bao gồm cả vỏ và tủy) được nhúng parafin để đánh giá mô bệnh học trong tương lai. Một phần 4-μm của mô FFPE được nhuộm bằng von Kossa để xác định sự lắng đọng hydroxyapatite.20 Các phần thận dọc theo chiều dọc được nhuộm màu được chụp ảnh, làm mù dữ liệu ca bệnh, sử dụng kính hiển vi kỹ thuật số (Leica DM4000, Wetzlar, Đức) để đánh giá bệnh canxi hóa thận bằng kính hiển vi (Hình 1). ImageJ (Phiên bản 2.1.0, Viện Y tế Quốc gia, Bethesda, Maryland) đã được sử dụng để định lượng bệnh canxi hóa thận từ các hình ảnh đại diện được chụp tại vùng tủy. Canxi hóa thận được phân loại theo tỷ lệ trung bình của mô nhuộm màu tích cực từ 5 hình ảnh tủy được chụp ở độ phóng đại 10 lần. Họ đã được xếp loại như sau:<0.06% = grade 0, 0.06% to 1% = grade 1, and >1 phần trăm=lớp 2 (Hình 1). Hệ thống phân loại này, được xác định trước trước khi phân tích thống kê, cung cấp một định lượng khách quan về mức độ nghiêm trọng của bệnh canxi hóa thận (0.06 phần trăm và 1 phần trăm tương ứng với 1 10 5 cm2 và 1,4 10 4 cm2 tương ứng). Phần FFPE liền kề từ mỗi hộp được nhuộm màu đỏ Alizarin (ở pH 4,2), cho phép phân biệt tinh thể CaP và CaOx.20

HÌNH 1 Quả thận, nhuộm von Kossa, độ phóng đại x10. Một ví dụ về từng cấp độ canxi hóa thận (0-2) được trình bày như sau: (A) và (B) mèo số. 7 với bệnh canxi hóa thận cấp 0 (0.004 phần trăm); (C) và (D) con mèo không. 34 ca nhiễm canxi thận độ 1 (0,327 % ); (E) và (F) con mèo không. 39 người mắc bệnh canxi hóa thận độ 2 (5,51 phần trăm ). Màu dương tính của Von Kossa được viền bằng màu đen trong ảnh gốc (A, C và E) hoặc màu đỏ tươi sau khi xử lý bằng ImageJ (B, D và F; 8-màu bit; ngưỡng {{16} }) để định lượng tỷ lệ diện tích canxi hóa thận trong mỗi trường hợp (n=51)
4. Chụp cắt lớp vi tính (micro-CT) đối với bệnh canxi hóa thận vĩ mô
Các khối thận FFPE được quét để phát hiện bệnh canxi hóa thận vĩ mô bằng cách sử dụng máy chụp cắt lớp vi tính (CT) (Skyscan 1172, Bruker, Kontich, Bỉ) bằng một máy ảnh nhỏ (4000 x 2672 pixel) không có bộ lọc. Hình ảnh thu được bằng cách sử dụng các tham số quét sau: kích thước voxel đẳng hướng 5 μm mỗi pixel, điện áp nguồn 50 kV, dòng điện nguồn 200 μA, thời gian phơi sáng 670 ms và quét xoay hình ảnh 180 với bước xoay 0,4. Hình ảnh chiếu được tái tạo thành ảnh chụp cắt lớp bằng NRecon 1.7.5.9 (Bruker, Kontich, Bỉ) và định vị lại bằng Dataviewer 1.5.6.6 (Bruker, Kontich, Bỉ). Ảnh chụp cắt lớp được phân tích bằng phần mềm phân tích Bruker CT-Analyzer (CTAn) 1.20.3 (Bruker, Kontich, Bỉ) và các hình ảnh hóa 3-chiều (3D) kết xuất khối được tạo bằng CTVox 3.3 (Bruker Kontich, Bỉ). Tóm lại, đối với mỗi khối, thể tích mô được tính bằng cách nhân độ sâu với diện tích trung bình từ 5 chụp cắt lớp cách nhau ở những khoảng cách bằng nhau trong toàn bộ mẫu; thể tích canxi hóa thận được tính toán bằng công cụ phân tích 3D trong CTAn. Tỷ lệ thể tích mô thận trên mô thận (VN: KT) được tính theo công thức:
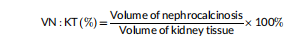
5. Phân tích thống kê
Các phân tích thống kê được thực hiện bằng phần mềm R (Phiên bản 4.1.1 GUI 1.77 High Sierra build, R Foundation for Statistical Computing, Vienna, Austria). Tỷ lệ lỗi loại I được đặt ở mức 0,05. Các biến liên tục được đánh giá về tính quy phạm bằng cách kiểm tra trực quan các biểu đồ và sử dụng phép thử Shapiro-Wilk. Thử nghiệm của Levene được sử dụng để kiểm tra xem các nhóm có phương sai bằng nhau hay không. Hầu hết dữ liệu thường không được phân phối và do đó, dữ liệu số được trình bày dưới dạng trung vị (phân vị thứ 25, 75) để đảm bảo tính nhất quán. Dữ liệu phân loại được trình bày dưới dạng phần trăm.
5.1 Các yếu tố nguy cơ mắc bệnh canxi hóa thận
Các biến cơ sở được so sánh giữa các nhóm bằng cách 1-phân tích phương sai (ANOVA), sau đó là kiểm tra hậu kiểm Tukey hoặc kiểm định hậu kiểm của Kruskal-Wallis và Dunn đối với các biến liên tục có phân phối bình thường hoặc sai lệch, tương ứng. Tỷ lệ kết quả phân loại được so sánh bằng cách sử dụng thử nghiệm chính xác của Fisher.
Các yếu tố nguy cơ gây bệnh canxi hóa thận vi thể ban đầu được đánh giá bằng cách sử dụng phương pháp hồi quy logistic thông thường. Tuổi, trọng lượng cơ thể, tCa, creatinine, urê, phốt phát, kali, natri, clorua, tổng protein, albumin, ALT, ALP, PCV, USG và thời gian sống sót của CKD được nhập dưới dạng các biến liên tục, trong khi đó giới tính và tỷ lệ PRD đã ăn vào ( "Không ăn PRD" so với "Ăn 10 phần trăm –50 phần trăm PRD" so với "Ăn nhiều hơn hoặc bằng 50 phần trăm PRD") đã được nhập dưới dạng các biến phân loại cho các phân tích đơn biến. Các biến liên quan đến bệnh canxi hóa thận ở P < 0,10 và với dữ liệu có sẵn cho ít nhất một nửa số mèo (n > 25), đã được nhập vào một mô hình đa biến. Loại bỏ ngược thủ công đã được áp dụng để có được mô hình cuối cùng với P <0,05. Phiên bản thông thường của phép thử Hosmer-Lemeshow được sử dụng để đánh giá mức độ phù hợp của mô hình cuối cùng và sự hiện diện của tính đồng tuyến tính giữa các yếu tố rủi ro độc lập quan trọng (P < 0,05) được đánh giá bằng hệ số lạm phát phương sai. Phần còn lại cho các ngoại lệ và các quan sát có ảnh hưởng đã được kiểm tra bằng kiểm tra trực quan biểu đồ Quantile-Quantile. Mối quan hệ tuyến tính giữa yếu tố dự đoán liên tục và logit được đánh giá bằng cách phân loại các biến thành các khoảng "thấp", "trung bình" và "cao" bằng nhau trong phân tích hồi quy logistic và đánh giá xu hướng tăng hoặc giảm của hệ số. Kết quả được báo cáo là tỷ lệ chênh lệch (OR; khoảng tin cậy 95 phần trăm [CI]).
5.2 Sự thay đổi các thông số CKD-MBD theo thời gian về bệnh canxi hóa thận
Các mô hình hiệu ứng hỗn hợp tuyến tính đã được sử dụng để đánh giá sự thay đổi của các biến số lâm sàng liên tục theo thời gian. Dữ liệu theo chiều dọc từ tất cả các lần thăm khám có sẵn trong 365 ngày đầu tiên sau khi chẩn đoán CKD được bao gồm cho những điều sau: trọng lượng cơ thể, tCa, creatinine, urê, phốt phát, kali, natri, clorua, tổng protein, albumin, ALT, ALP và PCV. Nhóm ("cấp 0" so với "cấp 1" so với "cấp 2"), thời gian (tính theo tháng [30,4 ngày]) và tương tác giữa nhóm và thời gian được coi là hiệu ứng cố định. Số trường hợp của mỗi con mèo và thời gian được lồng trong từng con mèo được đưa vào dưới dạng 2 hiệu ứng ngẫu nhiên không tương quan. Phần dư được coi là độc lập trong mô hình và tính quy phạm đã được kiểm tra. Không có nỗ lực nào được thực hiện để quy kết dữ liệu bị thiếu. Kết quả được báo cáo là hệ số ( ) ± SE.
5.3 Mối liên hệ giữa bệnh canxi hóa thận và các yếu tố khác với tỷ lệ sống sót
Ngày chẩn đoán CKD tăng azotemia được xác định là cơ sở, trong khi cái chết do mọi nguyên nhân là sự kiện được quan tâm. Thời gian sống sót được mô tả bằng đường cong Kaplan-Meier và được so sánh giữa các nhóm sử dụng bài kiểm tra thứ hạng log và Kruskal-Wallis với bài kiểm tra sau đại học của Dunn vì tất cả mèo đều đạt điểm cuối nghiên cứu. Các biến cơ sở liên quan đến tỷ lệ sống sót đã được khám phá bằng cách sử dụng phân tích rủi ro theo tỷ lệ Cox. Phần dư Martingale được sử dụng để đánh giá giả định về tính tuyến tính của các biến liên tục trong mô hình Cox. Phần dư cho các ngoại lệ và các quan sát có ảnh hưởng đã được kiểm tra bằng kiểm tra trực quan biểu đồ Quantile-Quantile. Các biến liên tục được chuyển đổi thành các biến phân loại dựa trên tertiles (tuổi, natri) nếu giả định về các mối nguy theo tỷ lệ, như được đánh giá bằng kiểm tra đường cong Kaplan-Meier và đánh giá tính độc lập giữa từng biến và thời gian không được đáp ứng. Các biến liên quan đến tỷ lệ sống sót với P <.10 trong các phân tích đơn biến đã được đưa vào mô hình Cox đa biến. Mô hình hồi quy Cox cuối cùng được rút ra bằng cách loại bỏ ngược thủ công với P < 0,05. Kết quả được báo cáo là tỷ lệ rủi ro (HR; 95 phần trăm CI).
5.4 von Kossa với tương quan nhuộm màu đỏ Alizarin và bệnh canxi hóa thận vĩ mô
Đối với mỗi trường hợp, các khu vực nhiễm canxi thận theo tỷ lệ trong tủy thận ở độ phóng đại X 2,5, được nhuộm bởi von Kossa và Alizarin red riêng biệt, đã được tính toán. Mối quan hệ giữa 2 kỹ thuật nhuộm này đối với bệnh canxi hóa thận vi thể được đánh giá bằng tương quan Spearman. Trong một nhóm nhỏ gồm 49 trường hợp, bệnh canxi hóa thận vĩ mô được đánh giá bằng micro-CT. Mối tương quan của Spearman được sử dụng để đánh giá mối quan hệ giữa thể tích canxi hóa thận theo tỷ lệ (micro-CT) và diện tích nhiễm canxi thận tỷ lệ (von Kossa, tổng quan X 0.14- X 0.36 độ phóng đại).
chiết xuất hạt dẻ cười
CUỘC THẢO LUẬN
Kết quả của chúng tôi chỉ ra rằng nồng độ tCa huyết tương ban đầu cao hơn và lượng PRD uống vào không phụ thuộc vào các yếu tố nguy cơ gây bệnh thận. Mèo bị nhiễm canxi thận cấp 0 có liên quan đến việc tăng nồng độ creatinine, urê và phốt phát trong huyết tương trong 365 ngày đầu tiên sau khi chẩn đoán CKD tăng azotemia. Nhóm mèo này cũng có thời gian sống sót ngắn hơn đáng kể so với những con mèo bị nhiễm canxi thận nặng hơn (độ 1 và 2). Một mối liên hệ tích cực độc lập đáng kể giữa hạn chế phốt phát trong chế độ ăn uống và tỷ lệ sống sót đã được quan sát.
Khoáng hóa thận là một quá trình phức tạp và nhiều mặt và cơ chế bệnh sinh của nó liên quan đến CKD vẫn chưa rõ ràng. Tuy nhiên, ngày càng có nhiều bằng chứng cho thấy rối loạn chuyển hóa khoáng chất, đặc biệt là canxi và phốt phát, có khả năng góp phần gây ra bệnh canxi hóa thận.11,12 Trong nghiên cứu của chúng tôi, tCa huyết tương cao hơn khi chẩn đoán CKD, ngay cả với tCa trong khoảng thời gian tham chiếu, là một nguy cơ độc lập gây bệnh canxi hóa thận. nhân tố; chỉ có 1 (2 phần trăm) con mèo bị tăng canxi máu toàn phần lúc ban đầu. Phát hiện này cho thấy rằng những xáo trộn nhẹ trong cân bằng nội môi canxi có thể thúc đẩy quá trình khoáng hóa thận ở mèo CKD. Phù hợp với những phát hiện của chúng tôi, một nghiên cứu CKD ở người cho thấy nồng độ tCa trong huyết thanh là một yếu tố nguy cơ gây ra bệnh canxi hóa thận độc lập.11 Hơn nữa, mối liên quan giữa chứng tăng canxi máu toàn phần và bệnh canxi hóa thận đã được tìm thấy ở bệnh nhân người sau ghép thận,21 và bệnh nhân bị bệnh canxi hóa thận vĩ mô bằng hình ảnh CT có nồng độ tCa và iCa cao hơn so với những người không có.22 Tuy nhiên, một nghiên cứu mô bệnh học ở người không tìm thấy mối liên quan giữa nồng độ tCa huyết thanh với hàm lượng canxi trong thận và sự lắng đọng canxi ở ống thận.12 Sự khác biệt về sự tham gia của canxi trong bệnh canxi hóa thận giữa các nghiên cứu là do nghiên cứu tính không đồng nhất của dân số, cỡ mẫu và phương pháp phát hiện vôi hóa thận.
Trong nghiên cứu của chúng tôi, việc nuốt phải PRD được xác định là một yếu tố nguy cơ gây bệnh canxi hóa thận độc lập ở mèo CKD. Hạn chế phốt phát trong chế độ ăn uống ảnh hưởng đáng kể đến sự điều chỉnh khoáng chất và nội tiết tố trong CKD-MBD, bao gồm giảm FGF23 và PTH. Bắt đầu PRD.18 Hàm lượng phốt phát trong chế độ ăn thấp hơn và tỷ lệ Ca:P trong chế độ ăn uống cao hơn, khi so sánh với các loại thức ăn có sẵn trên thị trường dành cho mèo trưởng thành khỏe mạnh,25 có khả năng tăng cường hấp thu canxi ở ruột và tăng nồng độ canxi trong huyết tương.26 Ở bệnh nhân người, chứng tăng canxi niệu là tình trạng phổ biến yếu tố nguy cơ nhiễm canxi thận.27 Do đó, người ta cho rằng bệnh canxi thận có thể được thúc đẩy bởi sự gia tăng nồng độ tCa trong huyết tương và tăng cường bài tiết canxi qua nước tiểu sau khi chuyển sang PRD ở mèo CKD. Tuy nhiên, không thể thu được bằng chứng trực tiếp ủng hộ giả thuyết này trong nghiên cứu của chúng tôi và các nghiên cứu tiền cứu đo điện giải trong nước tiểu là bắt buộc.
Kết quả của chúng tôi cho thấy rằng bệnh canxi hóa thận không liên quan tích cực với sự tiến triển của CKD và tỷ lệ tử vong do mọi nguyên nhân. Phát hiện này rất hấp dẫn vì nó hơi trái ngược với một nghiên cứu trước đây ở người cho thấy vai trò bất lợi của bệnh canxi hóa thận đối với chức năng thận bằng cách xác định mối tương quan thuận giữa hàm lượng canxi trong thận và nồng độ creatinine huyết thanh.12 Bệnh canxi hóa thận được xác định bằng hình ảnh (CT, siêu âm, hoặc chụp X quang) cũng có liên quan đến việc tăng nguy cơ mắc bệnh thận giai đoạn cuối ở bệnh nhân người.28 Một nghiên cứu trên mèo CKD cho thấy quá trình khoáng hóa thận có liên quan đến viêm kẽ và xơ hóa nghiêm trọng hơn, cho thấy vai trò của nó trong việc thúc đẩy tiến triển của CKD.15 Tuy nhiên, gần đây các nghiên cứu đoàn hệ liên quan đến bệnh nhân người được chụp CT thận cho thấy thiếu sự liên quan giữa chức năng thận và vôi hóa thận.22,29 Quan sát này phù hợp với kết quả của chúng tôi và ủng hộ giả thuyết của chúng tôi rằng bệnh canxi hóa thận, ở một mức độ nhất định, có thể không gây ra tác động có hại trực tiếp chức năng thận và góp phần vào sự tiến triển của CKD. Tuy nhiên, cần có các nghiên cứu trong tương lai để hiểu rõ hơn về tác động của bệnh canxi hóa thận đối với tình trạng suy giảm CKD ở mèo.
Mặc dù ăn phải PRD là một yếu tố nguy cơ độc lập gây ra bệnh canxi hóa thận, phân tích tỷ lệ sống sót của chúng tôi cho thấy rằng việc hạn chế phốt phát trong chế độ ăn uống (khi ăn vào lớn hơn hoặc bằng 50% PRD) có liên quan đến MST lâu hơn và tăng tỷ lệ sống sót lên đến 3- gấp đối với mèo CKD khi so sánh với mèo ăn chế độ ăn duy trì (Bảng 4 và Hình 4). Những phát hiện này hỗ trợ cho các nghiên cứu trước đây đã tìm thấy lợi ích sống sót do hạn chế phốt phát trong chế độ ăn uống ở mèo CKD.30-32 Ngoài ra, kết quả từ phân tích phụ của chúng tôi (Bảng S2 và S3) cho thấy mèo CKD tiếp tục được cho ăn chế độ ăn duy trì có nồng độ creatinine, urê và phốt phát trong huyết tương tăng nhiều hơn và giảm PCV và trọng lượng cơ thể trong năm đầu tiên sau khi chẩn đoán CKD, củng cố thêm bằng chứng hiện tại về tác dụng có lợi của việc hạn chế phốt phát trong chế độ ăn uống để giảm bớt sự tiến triển của bệnh.23,24,32, 33 Tăng phosphat máu có liên quan đến suy giảm chức năng thận,34 và chất kết dính phốt phát đã được chứng minh là bảo vệ chống lại sự tiến triển của CKD.35,36
Nồng độ phosphate trong huyết tương và PCV là những yếu tố dự đoán độc lập về tỷ lệ tử vong do mọi nguyên nhân. Chứng tăng phosphat máu và thiếu máu có liên quan đến CKD tiến triển hơn và tiên lượng xấu hơn ở mèo và người.37-42 Sự ứ đọng phosphat xảy ra khi tốc độ lọc cầu thận (GFR) giảm nhưng trong giai đoạn đầu của CKD, nồng độ phosphat trong huyết tương thường được duy trì trong phạm vi sinh lý các giới hạn do cơ chế điều hòa nội tiết tố thích ứng, bao gồm tăng sản xuất FGF23 và PTH và giảm sản xuất calcitriol.6,43 Do đó, nồng độ phốt phát trong huyết tương cao hơn khi chẩn đoán CKD có thể gợi ý về cân bằng nội môi phốt phát bị rối loạn nghiêm trọng hơn và có nguy cơ tử vong cao hơn . Phù hợp với kết quả của chúng tôi, một nghiên cứu trước đây đã phát hiện ra rằng nồng độ phốt phát trong huyết thanh cao hơn có liên quan độc lập với tỷ lệ sống sót ở 773 con mèo bị CKD.42 Cơ chế bệnh sinh của bệnh thiếu máu ở CKD là do nhiều yếu tố nhưng giảm sản xuất erythropoietin là yếu tố góp phần chính. phát hiện, các nghiên cứu khác cũng tìm thấy mối liên quan giữa PCV thấp hơn và tăng tỷ lệ tử vong ở mèo CKD,38,39,45 nhưng không phải tất cả.42 Điều thú vị là cả nồng độ creatinine huyết tương và giai đoạn IRIS đều không phải là yếu tố dự báo tử vong trong nghiên cứu hiện tại, điều này không nhất quán với các nghiên cứu trước đây.38,39,42,45,46 Nồng độ creatinine trong huyết tương phản ánh GFR và là một dấu ấn sinh học thay thế thường được sử dụng để đánh giá chức năng thận.47 Sự khác biệt có thể được giải thích bằng cách loại trừ mèo CKD giai đoạn IRIS trong nghiên cứu của chúng tôi và cỡ mẫu tương đối nhỏ, chỉ có 17 con mèo CKD giai đoạn 3 của IRIS. Ngoài ra, 29 phần trăm (n=15) mèo mắc CKD tăng azotemia trong nghiên cứu của chúng tôi đã không được quản lý chế độ ăn uống đối với CKD, điều này có thể ảnh hưởng đến kết quả và cản trở việc đánh giá chính xác giá trị tiên đoán của nồng độ creatinine huyết tương và có khả năng các biến số khác tại thời điểm chẩn đoán CKD đối với tỷ lệ sống sót trong nghiên cứu của chúng tôi.
Việc phát hiện sự lắng đọng canxi được thực hiện bằng cả phương pháp von Kossa sử dụng bạc nitrat và nhuộm màu đỏ Alizarin. Nguyên tắc của phương pháp von Kossa dựa trên sự liên kết của các ion bạc với các anion, chẳng hạn như phốt phát, oxalat và cacbonat, từ các mô bị vôi hóa và quá trình khử muối bạc, dẫn đến quan sát thấy màu đen của kim loại bạc.20,48,49 Nhuộm màu đỏ Alizarin là một kỹ thuật khác được sử dụng để chứng minh các tinh thể canxi.50 Nó liên kết trực tiếp với các ion canxi và có thể được sử dụng để phân biệt CaOx với CaP vì CaOx chỉ có thể được nhuộm bằng Alizarin Red ở độ pH 7 chứ không phải ở độ pH 4,2, với phương pháp thứ hai được sử dụng trong nghiên cứu của chúng tôi.51,52 Chúng tôi đã quan sát thấy mối tương quan chặt chẽ giữa 2 phương pháp nhuộm canxi hóa thận này, cho thấy rằng các khoáng chất chủ yếu bao gồm CaP. Quan sát này rất thú vị vì phần lớn sỏi niệu trên đường tiết niệu ở mèo có chứa CaOx.53 Có thể sự kết tủa CaP là điều kiện tiên quyết cho bệnh canxi hóa thận, sỏi thận hoặc cả hai ở mèo, một quá trình giống như sự hình thành các mảng Randall ở người. 8 Quá trình quét Micro-CT được thực hiện trên các mẫu thận FFPE để xác định xem một phiến kính nhuộm von Kossa có phải là đại diện của bệnh canxi hóa thận hay không. Chúng tôi đã tìm thấy mối tương quan vừa phải giữa bệnh canxi hóa thận vi mô và vĩ mô, hỗ trợ thêm cho các kỹ thuật và phương pháp định lượng được sử dụng để phân loại mức độ nghiêm trọng của bệnh canxi hóa thận trong nghiên cứu của chúng tôi, nhưng gợi ý, như có thể mong đợi, rằng một phần mô thận đưa ra ước tính gần đúng về mức độ nghiêm trọng của bệnh canxi hóa thận. bệnh canxi hóa thận vĩ mô được đánh giá bằng hình ảnh 3D.

viên nang cistache
Nghiên cứu hồi cứu của chúng tôi có một số hạn chế. Bệnh canxi hóa thận được xác định từ các mẫu thận được thu thập khi khám nghiệm tử thi và không biết vôi hóa thận phát triển ở những con mèo này vào thời điểm nào. Bệnh canxi hóa thận có thể đã phát triển trước khi chẩn đoán CKD. Chỉ những con mèo được khám nghiệm tử thi mới được đưa vào nghiên cứu. Do đó, sự sai lệch trong lựa chọn có thể đã xảy ra mặc dù các cuộc khám nghiệm tử thi đã được cung cấp cho tất cả các khách hàng khi mèo của họ bị tiêu diệt tại các phòng khám của chúng tôi. Một loạt các chế độ ăn duy trì đã được cho ăn trước khi chuyển sang PRD. Mặc dù nồng độ khoáng chất chính xác trong các chế độ ăn này rất khó xác định, nhưng theo báo cáo, giá trị trung bình của hàm lượng phốt pho và Ca:P lần lượt là 3 g/Mcal và 1,3 trong số 82 loại thức ăn cho mèo có bán trên thị trường.25 Do đó, điều này là hợp lý để giả định rằng những con mèo chấp nhận PRD sau khi chẩn đoán CKD nhận được lượng phốt phát trong chế độ ăn uống thấp hơn và chế độ ăn kiêng Ca:P cao hơn so với những con tiếp tục được cho ăn chế độ ăn duy trì. Do việc phân bổ nhóm PRD không được chọn ngẫu nhiên (tất cả mèo đều được cung cấp PRD như một phần trong chiến lược quản lý CKD của chúng trong nghiên cứu của chúng tôi vì lý do đạo đức), nên có thể xảy ra sai lệch lựa chọn, mặc dù không có sự khác biệt về các biến số lâm sàng được xác định giữa 3 nhóm tại đường cơ sở. Do đó, các tác động của PRD đối với sự tiến triển và tỷ lệ tử vong của CKD nên được giải thích một cách thận trọng vì lý do không rõ tại sao mèo không ăn PRD có thể liên quan đến khả năng sống sót kém hơn của chúng. Ngoài ra, nhiều loại PRD, với sự khác biệt về hàm lượng phốt pho và Ca: P, đã được cung cấp trong suốt thời gian nghiên cứu và không thể suy ra rằng kết quả từ nghiên cứu của chúng tôi có thể được khái quát hóa cho tất cả các PRD có bán trên thị trường bởi vì mặc dù các đặc tính chung của thận lâm sàng chế độ ăn uống là tương tự nhau, sự khác biệt trong công thức chế độ ăn uống tồn tại. Một nghiên cứu theo chiều dọc trong tương lai là cần thiết để điều tra thêm về tác động nhân quả của việc hạn chế phốt phát trong chế độ ăn uống đối với bệnh thận. Thật thú vị, mức độ vôi hóa vĩ mô có thể được đánh giá bằng cách sử dụng phương pháp quét micro-CT trong nghiên cứu của chúng tôi. Tuy nhiên, thể tích mô thận FFPE có thể đã được đánh giá quá cao do sự can thiệp của sáp parafin. Mặc dù đã thu được các phép đo nhiều diện tích bề mặt mô ở các khoảng độ sâu đều đặn để đưa ra ước tính tốt nhất có thể về thể tích mô, tỷ lệ VN: KT có thể đã bị đánh giá thấp. Tuy nhiên, khả năng này được coi là có tác động tương đối nhỏ đến mối tương quan giữa bệnh canxi hóa thận vi mô và vĩ mô được báo cáo. Cuối cùng, bệnh canxi hóa thận có liên quan đến chứng cường cận giáp ở bệnh nhân người.29 Mối liên quan này rất có thể là do nồng độ canxi trong huyết tương và nước tiểu tăng lên, bài tiết phốt phát qua nước tiểu và tái hấp thu canxi ở thận do PTH kích thích, dẫn đến vôi hóa thận.54, 55 Yếu tố tăng trưởng nguyên bào sợi-23 cũng được cho là có liên quan đến bệnh canxi hóa thận.56 Thật không may, dữ liệu về FGF23, PTH và chất điện giải trong nước tiểu không có sẵn trong nghiên cứu của chúng tôi; do đó, không thể điều tra sự liên quan của họ trong bệnh canxi hóa thận. Hạn chế này ngăn cản việc đánh giá thêm về khả năng đóng góp của chứng tăng calci niệu hoặc chứng tăng phosphat niệu đối với bệnh canxi hóa thận. Tình trạng canxi ở những con mèo trong nghiên cứu của chúng tôi được đánh giá bằng tCa vì phép đo iCa hoạt tính sinh học không có sẵn ở hầu hết các con mèo. Các nghiên cứu bổ sung, bao gồm các phép đo FGF23, PTH, iCa trong huyết tương, và canxi và phốt phát trong nước tiểu, được đảm bảo để xác định liệu các yếu tố này có đóng vai trò quan trọng hơn trong bệnh canxi hóa thận hay không.
Nói chung, chúng tôi đã chỉ ra rằng nồng độ tCa trong huyết tương cao hơn khi chẩn đoán CKD và hạn chế phốt phát trong chế độ ăn uống là những yếu tố nguy cơ độc lập đối với bệnh canxi hóa thận mặc dù không thể xác định được nguyên nhân. Vôi hóa ngoài xương là một quá trình nhiều mặt và phức tạp, được điều chỉnh tích cực bởi nhiều chất cảm ứng và ức chế khác nhau.57,58 Vai trò của các chất ức chế vôi hóa nội sinh, chẳng hạn như magiê, fetuin-A và pyrophosphate, đối với bệnh canxi hóa thận vẫn còn được khám phá ở mèo CKD. Hơn nữa, ở mèo, bệnh canxi hóa thận dường như không liên quan đến tốc độ tiến triển của bệnh và nguy cơ tử vong do mọi nguyên nhân trong nghiên cứu của chúng tôi. Tuy nhiên, việc uống PRD lớn hơn hoặc bằng 50 phần trăm có thể làm giảm nguy cơ tử vong do mọi nguyên nhân và kéo dài thời gian sống sót ở mèo CKD. Những quan sát mâu thuẫn này đòi hỏi phải nghiên cứu thêm. Ở mèo, CKD là một hội chứng không đồng nhất với tốc độ tiến triển rất khác nhau, rất có thể do nhiều yếu tố gây ra. Kết quả của chúng tôi cho thấy sự rối loạn trong cân bằng nội môi phốt phát góp phần vào sự tiến triển nhanh chóng của CKD mặc dù bệnh canxi hóa thận không rõ ràng ở những con mèo này. Các nghiên cứu triển vọng trong tương lai đánh giá sự phát triển và tiến triển của bệnh canxi hóa thận ở mèo mắc bệnh CKD tăng azotemia được đảm bảo và có thể dẫn đến một khuôn khổ mới cho các phương pháp chẩn đoán và điều trị trong việc quản lý bệnh CKD-MBD ở mèo.
NGƯỜI GIỚI THIỆU
1. Nồng độ của Finch NC, Geddes RF, Syme HM, Elliott J. Yếu tố tăng trưởng nguyên bào sợi 23 (FGF-23) ở mèo mắc bệnh thận mãn tính không nhiễm trùng huyết giai đoạn đầu (CKD) và ở mèo lão khoa khỏe mạnh. J Vet Intern Med. 2013;27:227-233.
2. Geddes RF, Finch NC, Elliott J, Syme HM. Yếu tố tăng trưởng nguyên bào sợi 23 trong bệnh thận mãn tính ở mèo. J Vet Intern Med. 2013;27(2): 234-241.
3. Locatelli F, Cannata-Andía J, Drüek T, et al. Quản lý rối loạn chuyển hóa canxi và phốt phát trong suy thận mãn tính, nhấn mạnh vào việc kiểm soát chứng tăng photphat máu. Cấy ghép quay số Nephrol. 2002;17(5):723-731.
4. Larsson T, Nisbeth U, Ljunggren Ö, et al. Nồng độ tuần hoàn của FGF-23 tăng lên khi chức năng thận suy giảm ở bệnh nhân mắc bệnh thận mãn tính, nhưng không thay đổi để đáp ứng với sự thay đổi lượng phốt phát hấp thụ ở những người tình nguyện khỏe mạnh. Thận Int. 2003;64(6):2272-2279.
5. Bergwitz C, Jüppner H. Điều chỉnh cân bằng nội môi phốt phát bằng PTH, vitamin D và FGF23. Annu Rev Med. 2010;61(1):91-104.
6. Geddes RF, Finch NC, Syme HM, Elliott J. Vai trò của phốt pho trong sinh lý bệnh của bệnh thận mãn tính. J Vet Emerg Crit Care. 2013;23(2):122-133.
7. Moe S, Drüeke T, Cunningham J, et al. Định nghĩa, đánh giá và phân loại chứng loạn dưỡng xương do thận: tuyên bố về vị trí của bệnh thận: cải thiện kết cục toàn cầu (KDIGO). Thận Int. 2006; 69(11):1945-1953.
8. Priante G, Ceol M, Terrin L, et al. Hiểu về sinh lý bệnh của Nephrocalcinosis. Trong: L dài, ed. Những cập nhật và tiến bộ trong bệnh sỏi thận – Sinh lý bệnh, Di truyền và Phương thức điều trị. Luân Đôn, Vương quốc Anh: IntechOpen; 2017:3-52. https://www.intechopen.com/books/updates-and-advances-in-nepholithiasis-pathophysiology genes-and- Treatment-modalities/under Hiểu-the Pathophysiology-of-nephrocalcinosis
9. Sayer JA, Carr G, Simmons NL. Nephrocalcinosis: những hiểu biết phân tử về sự kết tủa canxi trong thận. Khoa học lâm sàng. 2004;106(6): 549-561.
10. Moe OW. Sỏi thận: sinh lý bệnh và quản lý y tế. lưỡi giáo. 2006;367(9507):333-344.
11. Evenepoel P, Daenen K, Bammens B, et al. Nhiễm canxi thận vi thể ở bệnh nhân mắc bệnh thận mãn tính. Cấy ghép quay số Nephrol. 2015;30(5):843-848.
12. Gimenez LF, Solez K, Walker WG. Mối liên quan giữa hàm lượng canxi thận và suy thận trong 246 sinh thiết thận ở người. Thận Int. 1987;31(1):93-99.
13. Nagano N, Miyata S, Obana S, et al. Sevelamer hydrochloride, một chất kết dính phốt phát, bảo vệ chống suy giảm chức năng thận ở chuột bị suy thận mãn tính tiến triển. Cấy ghép quay số Nephrol. 2003;18(10):2014-2023.
14. Kuzela DC, Huffer WE, Conger JD, et al. Vôi hóa mô mềm ở bệnh nhân lọc máu mãn tính. Tôi là J Pathol. 1977;86(2):403-424.
15. Chakrabarti S, Syme HM, Brown CA, Elliott J. Phép đo mô hình bệnh thận mãn tính ở mèo và mối tương quan với các dấu hiệu rối loạn chức năng thận. Bác sĩ thú y Pathol. 2013;50(1):147-155.
16. Jara A, Chacon C, Ibaceta M, et al. Ảnh hưởng của amoni clorua và phốt pho trong chế độ ăn uống ở chuột azotaemia. Phần II-phì đại thận và lắng đọng canxi. Cấy ghép quay số Nephrol. 2004;19(8):1993-1998.
17. van den Broek DHN, Chang YM, Elliott J, Jepson RE. Bệnh thận mãn tính ở mèo và nguy cơ tăng canxi máu toàn phần. J Vet Intern Med. 2017;31(2):465-475.
18. Tang PK, Geddes RF, Chang YM, Jepson RE, Bijsmans E, Elliott J. Các yếu tố rủi ro liên quan đến rối loạn cân bằng nội môi canxi sau khi bắt đầu chế độ ăn hạn chế phốt phát ở mèo mắc bệnh thận mãn tính. J Vet Intern Med. 2021;35:321-332.
19. Syme HM, Barber PJ, Markwell PJ, Elliott J. Tỷ lệ tăng huyết áp tâm thu ở mèo bị suy thận mãn tính khi đánh giá ban đầu. J Am Vet Med PGS. 2002;220(12):1799-1804.
20. Kiernan JA. Phương pháp cho các ion vô cơ. Trong: Kiernan JA, chủ biên. Phương pháp mô học và mô học: Lý thuyết và thực hành. tái bản lần thứ 4. Bloxham, Oxfordshire: Scion Publishing Ltd; 2007:337-353.
21. Evenepoel P, Lerut E, Naesens M, et al. Nội địa hóa, nguyên nhân và tác động của lắng đọng canxi photphat trong mô ghép thận. Am J Ghép. 2009;9(11):2470-2478.
22. Ejlsmark-Svensson H, Bislev LS, Rolighed L, Sikjaer T, Rejnmark L. Các yếu tố dự đoán chức năng thận và vôi hóa trong bệnh cường cận giáp nguyên phát: một nghiên cứu bệnh chứng lồng ghép. Chuyển hóa nội tiết J Clin. 2018;103(9):3574-3583.
23. Geddes RF, Elliott J, Syme HM. Ảnh hưởng của việc cho ăn chế độ ăn có thận đối với nồng độ yếu tố tăng trưởng nguyên bào sợi 23 trong huyết tương ở mèo mắc bệnh thận mãn tính tăng azotemia ổn định. J Vet Intern Med. 2013;27(6):1354-1361.
24. Thợ cắt tóc PJ, Rawlings JM, Markwell PJ, et al. Ảnh hưởng của việc hạn chế phốt phát trong chế độ ăn uống đối với chứng cường cận giáp thứ phát ở thận ở mèo. J. Thực hành động vật nhỏ. 1999;40(2):62-70.
25. Summers SC, Stockman J, Larsen JA, Zhang L, Rodriguez AS. Đánh giá hàm lượng phốt pho, canxi và magiê trong các loại thực phẩm thương mại có sẵn dành cho mèo khỏe mạnh. J Vet Intern Med. 2020;34(1):266-273.
26. Masuyama R, Nakaya Y, Katsumata S, et al. Tỷ lệ canxi và phốt pho trong chế độ ăn uống điều chỉnh quá trình khoáng hóa và luân chuyển xương ở chuột loại bỏ thụ thể vitamin D bằng cách ảnh hưởng đến sự hấp thụ canxi và phốt pho ở ruột. Công cụ khai thác xương J Res. 2003;18(7):1217-1226.
27. Rönnefarth G, Misselwitz J. Bệnh canxi hóa thận ở trẻ em: một cuộc khảo sát hồi cứu. Pediatr Nephrol. 2000;14:1016-1021.
28. Tang X, Bergstralh EJ, Mehta RA, Vrtiska TJ, Milliner DS, Lieske JC. Nhiễm canxi thận là một yếu tố nguy cơ dẫn đến suy thận ở bệnh nhân tăng oxy máu nguyên phát. Thận Int. 2015;87(3):623-631.
29. Starup-Linde J, Waldhauer E, Rolighed L, Mosekilde L, Vestergaard P. Sỏi thận và vôi hóa ở bệnh nhân cường cận giáp nguyên phát: mối liên quan với các biến số sinh hóa. Eur J Nội tiết. 2012;166(6):1093-1100.
30. Elliott J, Rawlings JM, Markwell PJ, Thợ cắt tóc PJ. Sự sống sót của những con mèo bị suy thận mãn tính xảy ra tự nhiên: ảnh hưởng của việc quản lý chế độ ăn uống. J Thực hành động vật nhỏ. 2000;41:235-242.
31. Plantinga EA, Everts H, Kastelein AMC, Beynen AC. Một nghiên cứu hồi cứu về sự sống sót của những con mèo bị suy thận mãn tính mắc phải đã đưa ra các chế độ ăn thương mại khác nhau. Cựu chiến binh Rec. 2005;157(7):185-187.
32. Ross SJ, Osborne CA, Kirk CA, Lowry SR, Koehler LA, Polzin DJ. Đánh giá lâm sàng về điều chỉnh chế độ ăn uống để điều trị bệnh thận mãn tính tự phát ở mèo. J Am Vet Med PGS. 2006;229(6):949-957.
33. Lou LM, Caverni A, Gimeno JA, et al. Can thiệp chế độ ăn uống tập trung vào lượng phốt phát ở bệnh nhân chạy thận nhân tạo bị tăng phốt phát trong máu. Phòng khám Nephrol. 2012;77(6):476-483.
34. Voormolen N, Noordzij M, Grootendorst DC, et al. Phosphate huyết tương cao là một yếu tố nguy cơ gây suy giảm chức năng thận và tử vong ở bệnh nhân tiền lọc máu. Cấy ghép quay số Nephrol. 2007;22(10):2909-2916.
35. Nemoto Y, Kumagai T, Ishizawa K, et al. Liên kết phốt phát bằng oxyhydroxide sucroferric cải thiện tổn thương thận trong mô hình thận còn sót lại. Đại diện khoa học 2019;9(1):1-11.
36. Wang Q, Ishizawa K, Li J, et al. Hạt nano chứa phốt phát trong nước tiểu góp phần gây viêm và tổn thương thận trong mô hình chuột tăng huyết áp nhạy cảm với muối. Cộng Biol. 2020;3(1):1-12.
37. Chakrabarti C, Syme HM, Elliott J. Các biến số lâm sàng dự đoán sự tiến triển của chứng tăng nitơ huyết ở mèo mắc bệnh thận mãn tính. J Vet Intern Med. 2012;26(2):275-281.
38. Geddes RF, Elliott J, Syme HM. Mối quan hệ giữa nồng độ yếu tố tăng trưởng nguyên bào sợi huyết tương-23 và thời gian sống sót ở mèo mắc bệnh thận mãn tính. J Vet Intern Med. 2015;29(6):1494-1501.
39. Kuwahara Y, Ohba Y, Kitoh K, Kuwahara N, Kitagawa H. Hiệp hội dữ liệu phòng thí nghiệm và tử vong trong vòng một tháng ở mèo bị suy thận mãn tính. J Thực hành động vật nhỏ. 2006;47(8):446-450.
40. Kestenbaum B, Sampson JN, Rudser KD, et al. Nồng độ phốt phát huyết thanh và nguy cơ tử vong ở những người mắc bệnh thận mãn tính. J Am Sóc Nephrol. 2005;16(2):520-528.
41. Keith DS, Nichols GA, Gullion CM, Brown JB, Smith DH. Theo dõi dọc và kết quả trong số những người mắc bệnh thận mãn tính trong một tổ chức chăm sóc được quản lý lớn. Arch thực tập Med. 2004;164:659-663.
42. Boyd LM, Langston C, Thompson K, Zivin K, Imanishi M. Survival I mắc bệnh thận mãn tính tự nhiên (2000–2002). J Vet Intern Med. 2008;22:1111-1117.
43. Slatopolsky E. Vai trò của chuyển hóa canxi, phốt pho, s và vitamin D trong sự phát triển của bệnh cường cận giáp thứ phát. Cấy ghép quay số Nephrol. 1998;13(Bổ sung 3):3-8.
44. Chalhoub S, Langston CE, Eatroff A. Thiếu máu do bệnh thận. Nó là gì, phải làm gì và có gì mới. J Feline Med Surg. 2011;13(9):629-640.
45. King J, Tasker S, Gunn-Moore D, et al. Các yếu tố tiên lượng ở mèo mắc bệnh thận mãn tính. J Vet Intern Med. 2007;21:906-916.
46. Syme HM, Markwell PJ, Pfeiffer D, Elliott J. Sự sống sót của những con mèo bị suy thận mãn tính tự nhiên có liên quan đến mức độ nghiêm trọng của protein niệu. J Vet Intern Med. 2006;20:528-535.
47. Finch N. Đo tốc độ lọc cầu thận ở mèo: phương pháp và ưu điểm so với các dấu hiệu thông thường của chức năng thận. J Feline Med Surg. 2014;16(9):736-748.
48. McGee-Russell SM. Phương pháp mô hóa học cho canxi. J Histochem Cytochem. 1958;6(1):22-42.
49. Bonewald LF, Harris SE, Rosser J, et al. Chỉ riêng nhuộm Von Kossa I không đủ để khẳng định rằng khoáng hóa trong ống nghiệm đại diện cho sự hình thành xương. Calcif Tissue Int. 2003;72(5):537-547.
50. Puchtler H, Meloan SN, Terry MS. Về lịch sử và cơ chế nhuộm alizarin và alizarin S đỏ đối với canxi. J Histochem Cytochem. 1969;17:110-124.
51. Proia AD, Brinn NT. Xác định các tinh thể canxi oxalat bằng cách sử dụng thuốc nhuộm alizarin red S. Phòng thí nghiệm Arch Pathol Med. 1985;109(2):186-189.
52. Lewin-Smith MR, Kalasinsky VF, Mullick FG. Xác định mô hóa học của cellulose vi tinh thể, canxi oxalate và hoạt thạch trong các phần mô. Phòng thí nghiệm Arch Pathol Med. 2011;135(8):963.
53. Kyles AE, Hardie EM, BG bằng gỗ, et al. Các bất thường về lâm sàng, bệnh học, X quang và siêu âm ở mèo bị sỏi niệu quản: 163 trường hợp (1984–2002). JAMA. 2005;226(6):932-936.
54. Lila AR, Sarathi V, Jagtap V, Bandgar T, Menon PS, Shah NS. Biểu hiện thận của cường cận giáp nguyên phát. Ind J Chuyển hóa nội tiết. 2012;16(2):258-262.
55. Rejnmark L, Vestergaard P, Mosekilde L. Sỏi thận và vôi hóa thận trong cường cận giáp nguyên phát. Chuyển hóa nội tiết J Clin. 2011;96(8):2377-2385.
56. Takasugi S, Shioyama M, Kitade M, Nagata M, Yamaji T. Sự tham gia của estrogen trong bệnh canxi hóa thận do phốt pho gây ra thông qua yếu tố tăng trưởng nguyên bào sợi 23. Sci Rep. 2020;10(1):1-11.
57. Shanahan C, Crouthamel M, Kapustin A, et al. Vôi hóa động mạch trong bệnh thận mãn tính: vai trò chính của canxi và phốt phát. Thông tư Res. 2011;109(6):697-711.
58. Babler A, Schmitz C, Büscher A, et al. Bệnh lý vi mạch và vôi hóa mô mềm trong giấy phép được điều chỉnh bởi fetuin-a, pyrophosphate và magiê. XIN MỘT. 2020;15(2):e0228938.
Pak-Kan Tang1|Rosanne E. Jepson2|Yu-Mei Chang3|Rebecca F. Geddes2|Mark Hopkinson1|Jonathan Elliott1
1 Khoa Khoa học Y sinh So sánh, Đại học Thú y Hoàng gia, Đại học London, London, Vương quốc Anh
2 Khoa Khoa học Lâm sàng và Dịch vụ, Đại học Thú y Hoàng gia, Đại học London, London, Vương quốc Anh
3 Văn phòng Hỗ trợ Nghiên cứu, Trường Cao đẳng Thú y Hoàng gia, Đại học London, London, Vương quốc Anh






