Trừu tượng:Các thành phần dễ bay hơi được chưng cất trong nước của Cistanche tubulosa (Nhân sâm sa mạc) đã được nghiên cứu về mặt hóa học và sinh học. Dựa trên thời gian lưu và sự phân mảnh khối lượng của sắc ký đồ GC-MS thu được, 106 thành phần riêng lẻ đại diện cho ≈ 99,29 phần trăm tổng số thành phần dễ bay hơi đã được xác định. Các hợp chất chính (66,57 phần trăm tổng thành phần) được xác định là hexanal (15,98 phần trăm), trans-sabine axetat (12,22 phần trăm), tất cảo-aromadendren (9,30 phần trăm ), axit nonanoic (6,66 phần trăm ), 3Z-hexenyl-2-metyl butanoat (6.09 phần trăm ), valeranon (5,25 phần trăm ), (E , E)- -Farnesene (3,18 phần trăm ), -pinene (3.06 phần trăm ), linalool isoval Cả (3.03 phần trăm ) và -humulene (1,8 phần trăm ). Ước tính hoạt tính chống oxy hóa của EO cho thấy hiệu quả đầy hứa hẹn ở nồng độ 80 g/mL, nó có tác dụng ức chế 62,40, 863,29 và 62,72% so với TBHQ cho thấy mức ức chế 78,62, 77,56 và 79,23% khi sử dụng DPPH, ABTS và -caroten/axit linoleic tương ứng. Hoạt tính chống oxy hóa được phát âm ở mức 80 g/mL so với các nồng độ khác. Các thành phần dễ bay hơi cho thấy hoạt tính ức chế vi khuẩn gram dương nằm trong khoảng từ 2,23 mg/100 mL (đối với tụ cầu vàng ) đến 15,68 mg/100 mL (đối với Bacillus cereus) so với ciprofloxacin cho thấy hoạt tính ức chế là 0,185 và 0,182 mg/100 mL , tương ứng. Hơn nữa, MIC của các chất dễ bay hơi đối với vi khuẩn gram âm nằm trong khoảng từ 18,35 (Escherichia coli) đến 31,61 mg/100 mL (viêm phổi do Klebsiella) so với ciprofloxacin tương ứng là 0,184 đến 0,188 mg/mL. Ngoài ra, hoạt tính kháng nấm chống lại nấm candida albicans khá hứa hẹn (4,36 mg/mL).
Theo các nghiên cứu có liên quan,hột cálà một loại thảo mộc phổ biến được mệnh danh là “thần dược kéo dài tuổi thọ”. Thành phần chính của nó làcistanoside, có tác dụng khác nhau nhưchống oxy hóa, chống viêm, Vàxúc tiến chức năng miễn dịch. Cơ chế giữa cistanche vàLàm trắng danằm trong tác dụng chống oxy hóa củaglycoside cistanche. Melanin trong da người được tạo ra bởi quá trình oxy hóa tyrosine được xúc tác bởityrosinaza, và phản ứng oxy hóa cần có sự tham gia của oxy nên các gốc oxy tự do trong cơ thể trở thành nhân tố quan trọng ảnh hưởng đến quá trình sản sinh melanin. Cistanche chứa cistanoside, một chất chống oxy hóa và có thể làm giảm sự hình thành các gốc tự do trong cơ thể, do đóức chế sản xuất melamin.

Để biết thêm thông tin:
david.deng@wecistanche.com WhatApp:86 13632399501
từ khóa:Cistanche tubulosa; cấu tử dễ bay hơi; chống oxy hóa; kháng khuẩn; Orobanchaceae. . © 2021 Ấn phẩm ACG. Đã đăng ký Bản quyền.
1. Giới thiệu
Cistanche tubulosa, họ Orobanchaceae, là một loài thực vật ký sinh lâu năm, mọc ở những vùng khô cằn của châu Á và châu Phi, nó đã được phát hiện ở Trung Quốc, Ấn Độ, Nhật Bản, Ả Rập Saudi (sa mạc Sakaka, Aljouf, KSA) [1]. Nó có nhiều tên phổ biến khác nhau trong y học Trung Quốc là Lục bình sa mạc, Nhân sâm sa mạc và Rou Cong Rong, thân cây mọng nước và nhiều thịt với hàm lượng nước cao [1-6]. Cistanche quen thuộc với các thành phần dễ bay hơi và không bay hơi có thể bao gồm lignan, glycoside phenylethanoid, oligo và polysacarit, alkaloid và iridoid. Do sự đa dạng lớn về hàm lượng hóa chất thực vật và các hoạt động sinh học, Cistanche đã đạt được giá trị dược liệu cao trong các loại thuốc dân gian và truyền thống của Trung Quốc. Do đó, nó đã được sử dụng như một loại thuốc kích thích tình dục trong trường hợp liệt dương và vô sinh, thuốc nhuận tràng trong táo bón do tuổi già, và được phát hiện là có tác dụng bảo vệ thần kinh, đặc biệt là trong các trường hợp mắc bệnh Alzheimer, Parkinson và trầm cảm, chống lão hóa, chống ung thư, chống kết tập tiểu cầu, kháng nấm và kháng khuẩn, bảo vệ gan, kích thích miễn dịch, chống oxy hóa, hỗ trợ thận và chống ung thư trong ung thư biểu mô thực quản đại trực tràng [1, 7-13]. Nó cũng được sử dụng trong điều trị chứng đau đầu gối và lưng, cải thiện khả năng miễn dịch và các hoạt động nhận thức, và như một thuốc chống trầm cảm [14-17]. Nó đã được phát hiện là có tác dụng hạ đường huyết theo báo cáo của Shimoda và cộng sự [18]. Cuộc khảo sát tài liệu tuyên bố việc sử dụng Cistanche an toàn như một loại cây không độc hại về lâu dài [19]. Mặc dù C. tubulosa được cho là có giá trị y học cao, đặc biệt là trong y học cổ truyền Trung Quốc, các thành phần dễ bay hơi của chúng hiếm khi được nghiên cứu và thành phần hóa học của chúng chưa được mô tả đầy đủ. Cuộc điều tra trước đây đã tiết lộ đặc điểm của 38 thành phần từ tinh dầu C. salsa và 25 hợp chất từ dầu C. Deserticola, với ba thành phần chính được gọi là metyl 14-metyl pentadecanoat (13,60 phần trăm ), etyl palmitat (12,4 phần trăm ) và 2,5,6-trimetylolêtan (7,61 phần trăm ). Cuộc khảo sát cũng cho thấy việc xác định 21 hợp chất chỉ từ dầu dễ bay hơi C. tubulosa [1, 20-22]. Hơn nữa, hoạt động sinh học của các thành phần dễ bay hơi chưa được nghiên cứu đầy đủ. Do đó, chúng tôi mong muốn xác định thành phần hóa học của các thành phần dễ bay hơi của hoa C. tubulosa và ước tính các hoạt động chống oxy hóa và kháng khuẩn của chúng.
2. Vật liệu và phương pháp
2.1. Nguyên liệu thực vật
Cistanche tubulosa (Schenk) Hook. f. (Orobanchaceae) được thu thập vào tháng 3 năm 2019 từ sa mạc Sakaka, Aljouf, KSA. Ông Hamdan Al-Hassan, M.Sc. (Trung tâm nghiên cứu lạc đà và phạm vi), Aljouf, KSA. Một mẫu chứng từ (59-CPJU) đã được lưu trữ trong phòng tiêu bản của Khoa Dược lý, Cao đẳng Dược, Đại học Jouf.
2.2. Khai thác các thành phần dễ bay hơi
Hoa của C. tubulosa được thu hái vào ngày 2 tháng 3019 và rửa cẩn thận bằng nước chảy, đồng thời chiết xuất các thành phần dễ bay hơi bằng phương pháp chưng cất thủy động chuẩn với thiết bị Clevenger. 500 g hoa tươi được cắt thành từng miếng nhỏ và chưng cất bằng phương pháp thủy điện trong 5 giờ cho đến khi không còn sản lượng nữa. phần chưng cất được tách ra khỏi pha nước bằng phễu chiết thể tích 500 mL. NaCl được sử dụng để trục xuất phần còn lại của các thành phần dễ bay hơi khỏi lớp nước bằng cơ chế loại bỏ muối. Pha nước được lắc nhiều lần với CH2Cl2 để thu được tất cả các sản phẩm chưng cất. Dịch chiết được gộp lại sau đó được lọc qua giấy lọc Whatman (Số 40) sau khi được cho qua Na2SO4 khan để khử nước. Sản phẩm được tính bằng 0,36 phần trăm tổng số chất bay hơi. Các cấu tử thu được là chất lỏng màu vàng nhạt, có mùi dễ chịu. Nó được đóng gói trong một lọ mờ đục khô ráo, sạch sẽ và đậy kín và giữ trong bóng tối ở 4 độ để phân tích.
2.3. Sắc ký khí và Sắc ký khí-Khối phổ (GC-MS)
Model 6890 của máy sắc ký khí Agilent được cung cấp với cột mao quản silica cố định pha 120 m × 0,25 mm id (df=0.25 μm) HP-5MS (Agilent, Folsom , CA) và máy dò ion hóa ngọn lửa (FID) đã được áp dụng để phân tích chiết xuất dễ bay hơi. Nhiệt độ của lò được điều chỉnh từ 60 đến 240 độ với tốc độ 3 độ / phút. và giữ trong 50 phút. Khí mang của tỷ lệ cấp liệu helium tuyến tính là 20 cm/giây. Nhiệt độ của kim phun và máy dò là 250 độ.

Các thành phần dễ bay hơi được phân tích bằng Agilent Technologies model 7890B GC được giao tiếp với máy dò khối lượng Agilent 7000D GC/TQ (GC/MS) và bộ lấy mẫu tự động Agilent 7693A. Ion hóa ở 70 eV, cột HP-5MS (id 120m x 0,25 mm). Toàn bộ quá trình được tiến hành ở vận tốc không đổi 30 cm/s của pha động (He) và nhiệt độ không đổi ở 250 ºC cho cả kim phun và đầu dò. Nhiệt độ lò được lập trình từ 60 đến 240 ºC với tốc độ 3 ºC/phút và được giữ trong 50 phút.
Việc tiêm mẫu đồng thời với dung dịch chứa chuỗi n-hydrocacbon tương đồng (C8-C26) trong cùng điều kiện được thực hiện để xác định các giá trị chỉ số của Kovat. Việc xác định các chất bay hơi bị cô lập được thực hiện bằng cách khớp với dữ liệu thư viện khối phổ của NIST, so sánh các chỉ số của Kovat với chỉ số của các thành phần xác thực và dữ liệu đã công bố. Định lượng được thực hiện theo tích phân diện tích pic.
2.4. Hoạt động chống oxy hóa
2.4.1. Xét nghiệm nhặt gốc tự do DPPH
Hoạt tính chống oxy hóa tiềm năng của các thành phần dễ bay hơi thu được được đánh giá bằng phương pháp DPPH tiêu chuẩn và tert-butylhydroquinone (TBHQ) được sử dụng làm thuốc chống oxy hóa tiêu chuẩn. Phép đo độ hấp thụ được thực hiện ở bước sóng tối đa 517 nm trên máy đo quang phổ UV (HP 8452, UVVIS), tất cả các phép thử được tiến hành ba lần và tính trung bình của các kết quả [23, 24].
2.4.2. -Xét nghiệm tẩy trắng Caroten
Phương pháp -caroten/axit linoleic tiêu chuẩn được áp dụng để xác định hoạt tính chống oxy hóa của các thành phần dễ bay hơi của C. tubulosa như đã mô tả trước đây, so với chất chống oxy hóa tiêu chuẩn tert-butylhydroquinone (TBHQ). Tất cả các thử nghiệm được đo ba lần ở bước sóng tối đa 470nm trong hơn 60 phút bắt đầu từ 0 phút và giá trị trung bình của các kết quả được tính [23, 24].
2.4.3. Xét nghiệm gốc tự do ABTS
ABTS [2,2`-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid), được áp dụng để xác định chất chống oxy hóa của các thành phần dễ bay hơi của C. tubulosa như được mô tả trong tài liệu [25], khi so sánh với chất chống oxy hóa tiêu chuẩn tert-butylhydroquinone (TBHQ). Tất cả các thử nghiệm được đo ba lần ở bước sóng tối đa 734 nm trong 60 phút bắt đầu từ 0 phút và giá trị trung bình của các kết quả được tính [26]. Phương trình sau đây được áp dụng để tính toán hiệu ứng nhặt gốc tự do trong tất cả các phương pháp
phần trăm ức chế=A (kiểm soát) - A (thử nghiệm hoặc tiêu chuẩn) / A (kiểm soát) × 100,
Ở đâu, Độ hấp thụ =

2.5. Xét nghiệm kháng khuẩn
2.5.1. Chuẩn bị huyền phù vi sinh vật
Chín chủng vi sinh vật gây bệnh được coi là nguồn gốc chính của một số bệnh và ngộ độc thực phẩm đã được chọn để làm xét nghiệm kháng sinh đồ bao gồm S. aureus, B. cereus E. fecal và L. monocytogenes được sử dụng như vi khuẩn G plus ve, E. coli , P. aeruginosa, K. pneumonia, và Salmonella typhimurium là vi khuẩn G-ve. Ngoài ra, C. albicans được sử dụng làm chủng nấm. Phương pháp định lượng nồng độ ức chế tối thiểu (MIC) được áp dụng để ước tính khả năng kháng khuẩn của các thành phần dễ bay hơi của C. tubulosa. Huyền phù vi khuẩn và nấm được chuẩn bị trong môi trường canh thang thích hợp cho từng loại (Muller Hinton Sabaroud Dextrose tương ứng cho vi khuẩn và nấm). Việc ủ từng chủng với môi trường thích hợp được thực hiện trong 24 giờ ở 37 độ đối với vi khuẩn và 28 độ đối với nấm. Sau thời gian ủ và pha loãng nối tiếp các huyền phù đã chuẩn bị, một số độ pha loãng nhất định được chọn theo tiêu chuẩn 0.5 Mc-Farlandscale cho xét nghiệm. Ciprofloxacin và fluconazole tiêu chuẩn đã được điều chế với hàm lượng 100µg/mL và được sử dụng tương ứng như thuốc kháng khuẩn và kháng nấm [28-30].
2.5.2. Phương pháp nồng độ ức chế tối thiểu (MIC)
Phương pháp định lượng đĩa pha loãng microtiter được áp dụng, trong đó phương pháp nồng độ ức chế tối thiểu (MIC) được áp dụng để đánh giá hoạt tính kháng khuẩn của các thành phần dễ bay hơi C. tubulosa, chống lại một số vi sinh vật như đã đề cập. Một giếng vi đĩa {{0}} vô trùng đã được sử dụng, trong đó 100µL vi sinh vật tương ứng ở nồng độ (0,5 Mc-Farland, khoảng 1×108cfu/mL) được trộn riêng với dịch chưng cất thu được ở các nồng độ khác nhau (100 phần trăm , tiếp theo là pha loãng nối tiếp hai lần). Ciprofloxacin và fluconazole lần lượt được áp dụng làm tiêu chuẩn kháng khuẩn và kháng nấm dương tính, trong khi DMSO được áp dụng làm đối chứng âm tính. Tấm vi mạch với các thành phần hỗn hợp trong mỗi giếng được ủ trong 24 giờ ở ≈37 độ đối với vi khuẩn và 28 độ đối với nấm. Các đĩa sau đó được hiển thị cho bất kỳ kết tủa tăng trưởng nào của các sinh vật được thử nghiệm. Tất cả các thí nghiệm được tiến hành ba lần và MIC được tính là nồng độ thấp nhất có tác dụng ức chế hoặc cản trở sự phát triển của vi sinh vật được thử nghiệm [27].
3. Kết quả và thảo luận
3.1. Phân tích các thành phần dễ bay hơi
Trong nghiên cứu của chúng tôi, quá trình chưng cất thủy điện hoa C. tubulosa tạo ra 0.36% sản phẩm chưng cất màu vàng nhạt, có mùi thơm dịu và 106 thành phần dễ bay hơi (bảng 1) chiếm 99,29% hàm lượng dễ bay hơi. Các thành phần này được phân loại thành 5 monoterpen, 15 sesquiterpen, 62 hợp chất oxy hóa nhẹ đại diện cho các hợp chất nhóm lớn nhất và 24 hợp chất oxy hóa nặng. Các thành phần chính của cấu tử dễ bay hơi được xác định là hexanal (15,98 phần trăm ), trans-sabine axetat (12,22 phần trăm ), also-aromadendrene (9,30 phần trăm ), axit nonanoic (6,66 phần trăm ), 3Z-hexenyl-2-metyl butanoat (6,09 phần trăm ), valeranone (5,25 phần trăm ), (E, E)- -Farnesene (3,18 phần trăm ), -pinene (3,06 phần trăm ), linalool isoval Cả (3,03 phần trăm ), -humulene (1,8 phần trăm ), Jasminol (1,58 phần trăm ), 4-hydroxy benzaldehyde (1,56 phần trăm ), Geosmin (1,44 phần trăm ), 3Z- hexenyl iso butanoate (1,39 phần trăm ) và geranyl axeton (1,38 phần trăm ). Nhưng trong các kết quả nghiên cứu tài liệu trước đây, được xuất bản bởi Jiang và Tu 2009, chỉ có 21 thành phần dễ bay hơi được xác định trong tinh dầu C. tubulosa, 38 thành phần cũng được đặc trưng bởi tinh dầu C. salsa, trong khi 25 hợp chất được xác định từ tinh dầu C. tubulosa. dầu của C. Deserticola, với ba thành phần chính (metyl 14-metyl pentadecanoat; 13,60 phần trăm , etyl palmitat; 12,40 phần trăm và 2,5,6-trimetylolêtan; 7,61 phần trăm ) [22, 28]. Việc xác định các chất bay hơi bị cô lập đã được thực hiện một cách tạm thời bằng cách khớp với dữ liệu thư viện khối phổ của NIST, được xác nhận thêm bằng cách so sánh các chỉ số của Kovat với chỉ số của các thành phần xác thực cũng như với dữ liệu đã xuất bản [29-31]. Người ta thấy rằng KI tính toán của các hợp chất đã xác định nằm trong phạm vi KI của những hợp chất được công bố trong tài liệu. Ví dụ: KI được tính toán và công bố cho trans-Sabinyl axetat (1287& 1273-1289), aromadendrene (1444& 1430-1450), valeranone (1678, 1668-1679), alloaromadendrene (1459& {{79} }), -Farnesene (1508& 1505-1520), hexenyl-2-metyl butanoat (1230& 1210-1231), -humulene (1455& 1452-1570), -pinen (971& { {91}}) [32-36]. Theo các giá trị KI đã đề cập, các hợp chất được xác định phù hợp với các hợp chất được báo cáo trong tài liệu [37-40].



3.2. Kết quả xét nghiệm chất chống oxy hóa
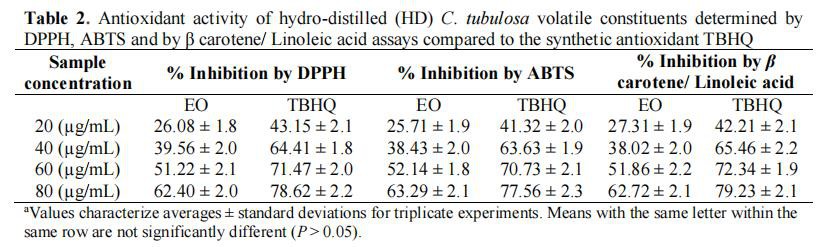
Các xét nghiệm DPPH, ABTS và -caroten đã được áp dụng để nghiên cứu hoạt tính chống oxy hóa của các thành phần dễ bay hơi C. tubulosa, kết quả cho thấy hoạt tính chống oxy hóa đáng tin cậy của các chất bay hơi được thử nghiệm (Bảng 2). Nghiên cứu hiện tại chỉ ra rằng khả năng loại bỏ các thành phần dễ bay hơi của C. tubulosa ở các nồng độ khác nhau (g/mL) nằm trong khoảng từ 26,08% đến 62,40% đối với xét nghiệm DPPH, trong khi từ 25,71 đến 63,29% và 27,31 đến 62,72% ở ({{ 14}}) g/mL đối với các hệ thống thử nghiệm ABTS và -caroten, tương ứng, so với thuốc chống oxy hóa TBHQ tiêu chuẩn, cho thấy 43,15 đến 78,62 phần trăm , 41,32 đến 77,56 phần trăm và 42,21 đến 79,23 phần trăm tại (20-80 ) ug/mL tương ứng cho các hệ thống thử nghiệm DPPH, ABTS và -caroten. Hoạt tính chống oxy hóa đầy hứa hẹn có thể là do sự hiện diện của hỗn hợp phức hợp có hoạt tính cao trong sản phẩm chưng cất như allo-aromadendrene (9,3 phần trăm ), valeranone (5,25 phần trăm ), (E, E)- -Farnesene (3,18 phần trăm ) và -pinene (3,06 phần trăm ) được cho là có tác động rõ rệt đến hoạt động chống oxy hóa. Theo khảo sát tài liệu, hoạt động sinh học mục tiêu của các thành phần dễ bay hơi có thể là do hỗn hợp các thành phần terpenoid và phenolic hiện có, được biết là có hoạt tính kháng khuẩn và chống oxy hóa và có thể tăng cường hoặc hiệp đồng các hoạt động mục tiêu [32].
3.3. Kết quả xét nghiệm kháng sinh
Phương pháp MIC (nồng độ ức chế tối thiểu) được áp dụng để kiểm tra hoạt tính kháng khuẩn của các thành phần dễ bay hơi của C. tubulosa đối với chín vi sinh vật gây bệnh có nguồn gốc động vật đã được nghiên cứu. Sản phẩm chưng cất thể hiện hoạt tính mạnh đối với S. aureus với MIC 2,23 mg/100mL và tác dụng trung bình đối với C. albicans (MIC= 4.36 mg/100mL), bảng 3.

4. Kết luận
Các thành phần dễ bay hơi của C. tubulosa hay thường được gọi là Nhân sâm sa mạc được cấu tạo chủ yếu từ hexanal (15,98 phần trăm ), trans-sabine axetat (12,22 phần trăm ), cho phép aromadendrene (9,30 phần trăm ), axit nonanoic (6,66 phần trăm ), 3Z-hexenyl{ {11}}metyl butanoate (6,09 phần trăm ), valeranone (5,25 phần trăm ), (E, E)- -Farnesene (3,18 phần trăm ), -pinene (3,06 phần trăm ), linalool isoval Cả (3,03 phần trăm ) và - humulene (1,8 phần trăm ), được đặc trưng bởi thời gian lưu và kiểu phân mảnh của từng loại, trong sắc ký đồ GC-MS, cũng như so sánh với tài liệu. Các thành phần này cho thấy tác dụng chống oxy hóa đầy hứa hẹn ở nồng độ 80 g/mL và các kết quả tương đối giống nhau khi sử dụng ba phương pháp thử nghiệm. Nó cũng thể hiện hoạt tính kháng khuẩn và kháng nấm mạnh đối với S. aureus L. monocytogenes và C. albicans so với ciprofloxacin và fluconazole.

Sự nhìn nhận
Các tác giả gửi lời cảm ơn tới Trưởng khoa Nghiên cứu Khoa học tại Đại học Jouf đã tài trợ cho công trình này thông qua khoản tài trợ nghiên cứu số (DSR2020-04-453) và tới Dự án hỗ trợ các nhà nghiên cứu của Đại học Taif số (TURSP-2020/56), Đại học Taif, Taif, Ả Rập Saudi.
Xung đột lợi ích
Các tác giả tuyên bố không có xung đột lợi ích.
Người giới thiệu
[1] Y. Giang và P.-F. Tú (2009). Phân tích thành phần hóa học trong loài Cistanche, J. Chrom. A. 1216(11), 1970-1979.
[2] L. Zhiming, L. Huinuan, G. Long, G. Jingwen và T. Chi-Meng (2016). Herba Cistanche (Rou Cong Rong): Một trong những món quà dược phẩm tốt nhất của y học cổ truyền Trung Quốc, Front. dược phẩm. 7, 41.
[3] C. Gu, X. Yang, và L. Huang (2016). Cistanches Herba: một đánh giá dược lý thần kinh, Mặt trận. dược phẩm. 7, 289.
[4] EM Abdallah (2017). Đánh giá khả năng kháng khuẩn của cuống hoa của Cistanche violacea, một loại cây ký sinh trùng được thu thập từ vùng khô hạn ở Qassim, Ả Rập Saudi, Pharma. sinh học. đánh giá. 4(6), 239-244.
[5] K. Zwe-Ling, J. Athira, K. Fan-Chi, H. Jia-Ling và C. Shu-Chun (2018). Tác dụng của chiết xuất Cistanche tubulosa đối với chức năng sinh sản của con đực ở chuột mắc bệnh tiểu đường do streptozotocin–nicotinamide gây ra, Chất dinh dưỡng 10(10), 1562.
[6] W. Lin-lin, D. Hui, Y. He-shui, L. Qing-hai, Z. Li-juan và S. Xin-bo (2015). Cistanches Herba: thành phần hóa học và tác dụng dược lý, Chin. thảo mộc. y tế. 7(2), 135-142.
[7] F. Changshuang, L. Jinyu, A. Adila, X. Lijie, Y. Yi, C. Qiuyan, L. Jie, W. Xinhui và L. Jinyao (2019). Các glycoside phenylethanoid của Cistanche tubulosa gây ra quá trình chết theo chương trình trong các tế bào Eca‑109 thông qua con đường phụ thuộc vào ty thể, Oncol. Hãy để. 17(1), 303-313.
[8] Q. Xu, W. Fan, S.-F. Ye, Y.-B. Công, W. Qin, S.-Y. Chen và J. Cai (2016). Cistanche tubulosa bảo vệ các tế bào thần kinh dopaminergic thông qua quy định về quá trình chết theo chương trình và yếu tố dinh dưỡng thần kinh có nguồn gốc từ tế bào thần kinh đệm: in vivo và in vitro, Front. Lão hóa thần kinh. 8, 295.
[9] N. Wang, S. Ji, H. Zhang, S. Mei, L. Qiao và X. Jin (2017). Herba Cistanches: chống lão hóa, bệnh lão hóa. 8(6), 740.
[10] A. Bougandoura, B. D'Abrosca, S. Ameddah, M. Scognamiglio, R. Mekkiou, A. Fiorentino, S. Benayache và F. Benayache (2016). Thành phần hóa học và hoạt tính chống viêm trong ống nghiệm của chiết xuất Cistanche violacea Desf.(Orobanchaceae), Fitoterapia 109, 248-253.
[11] Z. Jiang, J. Wang, X. Li và X. Zhang (2016). Echinacoside và Cistanche tubulosa (Schenk) R. wight cải thiện tổn thương tinh hoàn và tinh trùng do bisphenol A gây ra ở chuột thông qua các enzym steroidogen điều hòa trục tuyến sinh dục, J. Ethnopharmacol. 193, 321-328.
[12] CJ Wu, MY Chien, NH Lin, YC Lin, WY Chen, CH Chen và JTC Tzen (2019). Echinacoside được phân lập từ Cistanche tubulosa được cho là kích thích tiết hormone tăng trưởng thông qua kích hoạt thụ thể ghrelin, Phân tử 24(4),720.
[13] X. Wang và Y. Guo (2017). Xác định đồng thời nhanh sáu thành phần hiệu quả trong Cistanche tubulosa bằng phương pháp quang phổ cận hồng ngoại, Molecules 22(5), 843.
[14] AE Al-Snafi (2020). Các chất chuyển hóa hoạt tính sinh học và dược lý của Cistanche tubulosa-Một đánh giá. IOSR J. Pharm. 10(1), 37-46.
[15] D. Wang, H. Wang và L. Gu (2017). Các hoạt động cải thiện nhận thức và chống trầm cảm của loại thảo mộc truyền thống Trung Quốc Cistanche, Evid. Căn cứ phức tạp. thay thế. y tế. 2017, 3925903.
[16] AE Al-Snafi (2016). Tác dụng miễn dịch của cây thuốc: Đánh giá (phần 2), Immun. nội tiết. Metab. Đại lý Med. hóa. 16(2), 100-121.
[17] AS Al-Menhali, SA Jameela, AA Latiff, MA Elrayess, M. Alsayrafi và M. Jaganjac (2017). Cistanche tubulosa gây ra quá trình chết theo chương trình qua trung gian các loài oxy phản ứng của các tế bào ung thư ruột kết nguyên phát và di căn ở người, J. Applied Pharm. Khoa học. 7(5), 039-045.
[18] H. Shimoda, J. Tanaka, Y. Takahara, K. Takemoto, SJ Shan và MH Su (2009). Tác dụng hạ đường huyết của chiết xuất Cistanche tubulosa, một loại thuốc thô truyền thống của Trung Quốc, ở chuột, Amer. J. Chín. y tế. 37(6), 1125-1138.
[19] XY Wang, R. Xu, J. Chen, JY Song, SG Newmaster, JP Han, Z. Zhang và SL Chen (2018). Phát hiện các sản phẩm thuốc Cistanches herba (Rou Cong Rong) bằng cách sử dụng chữ ký nucleotide dành riêng cho loài, Mặt trận. Khoa học thực vật 9, 1643.
[20] NS Du, SH Qu, XD Re, JT Ni, HQ Zhang và HJ Yan (1988). Nghiên cứu thành phần tinh dầu từ Cistanche salsa G, Youji Huax. 8, 522-525.
[21] C. Formisano, D. Rigano, F. Senatore, M. SJ Simmonds, A. Bisio, M. Bruno và S.Rosselli (2008). Thành phần tinh dầu và đặc tính chống ăn mòn của Bellardia Chicago (L.) All. (sin. Bartsia trixago L.)(Scrophulariaceae), Biochem. Hệ thống. sinh thái. 36(5-6), 454-457.
[22] SJ Roudbaraki và D. Nori-Shargh (2016). Phân tích thành phần dễ bay hơi của Orobanche alba Stephan từ Iran, Current Anal. hóa. 12(5), 496-499.
[23] A.Baran, E. Karakılıç, Ö. Faiz và F. Özen (2020). Tổng hợp các metallicophthalocyanine chứa kẽm và coban có chứa chalcone; điều tra các đặc tính quang hóa, quét gốc DPPH và chelat kim loại của chúng, Org.Commun.. 13(2), 65-78.
[24] A. Musa, NS Al-musical và MS Abdel-Bakky (2016). Đánh giá hóa học và dược lý của chiết xuất etanolic của Bassia epiphora, Der Pharm Chem. 8(12), 169-178.
[25] MM Ramadan, MM Ali, KZ Ghanem và AH El-Ghorab (2015). Tinh dầu từ cây thơm Ai Cập là chất chống oxy hóa và chất chống ung thư mới trong các dòng tế bào ung thư ở người, Gras. y Aceit 66(2), e080.
[26] ZQ He, XY Shen, ZY Cheng, RL Wang, PX Lai và X. Xing (2020). Thành phần hóa học, hoạt tính kháng khuẩn, chống oxy hóa và gây độc tế bào của tinh dầu Dianella ensifolia, Rec. tự nhiên sản xuất. 14(2), 160-165.
[27] A. Hamed, B. Mahmoud, M. Samy, EM Mostafa, A. Wanas, M. Radwan, M. Elsohly và M. Kamel (2019). Các nghiên cứu về hóa chất thực vật và kháng khuẩn của lá Sprague Markhamia platycalyx (Baker), Trop. J.Pharm. độ phân giải 18, 2623-263.
[28] MM Ghoneim, A. Musa, AA El-Hela và KM Elokely (2018). Đánh giá và hiểu biết về cơ sở phân tử của hoạt động Staphylococcus aureus kháng methicillin của các chất chuyển hóa thứ cấp được phân lập từ Lamium amplexicaule, Pharmacog. tạp chí. 14(55), S3-S7.
[29] MA Abdelgawad, AM Mohamed, A. Musa, EM Mostafa và HM Awad (2018). Tổng hợp, phân tách sắc ký và tiến hóa kháng khuẩn của azoquinoline-8-ol mới, J. Pharm. Khoa học. độ phân giải 10(6), 1314-1318.
[30] A. Musa (2019). Thành phần hóa học, đánh giá kháng khuẩn và chống viêm của các chất chiết xuất khác nhau của suaeda vera fork. đang phát triển ở Ả Rập Saudi, Int. J.Pharm. độ phân giải 11(4), 962-967.
[31] RP Adams (2017). Xác định các thành phần tinh dầu bằng sắc ký khí/khối phổ, ed. 4.1., Tập đoàn xuất bản quyến rũ Carol Stream.
[32] BFMT Andrade, LN Barbosa, IS Probst và AF Júnior (2014). Hoạt động kháng khuẩn của tinh dầu, J. Essent. Dầu Res. 26(1), 34-40.
[33] V. Babushok, P. Linstrom và I. Zenkevich (2011). Chỉ số lưu giữ đối với các hợp chất được báo cáo thường xuyên của tinh dầu thực vật, J. Phys. và Hóa học. Tham khảo Dữ liệu 40(4), 043101.
[34] J. Alencar, A. Craveiro và FdA Matos (1984). Các chỉ số của Kovats như một quy trình lựa chọn trước trong thư viện khối phổ tìm kiếm các chất dễ bay hơi, J. Nat. sản xuất. 47(5), 890-892.
[35] MY Tian, XG Zhao, XH Wu, Y. Hong, Q. Chen, XL Liu và Y. Zhou (2020). Thành phần hóa học, hoạt tính kháng khuẩn và gây độc tế bào của tinh dầu Ficus tikoua Bur, Rec.Nat.Prod. 14, 219-224.
[36] A. Judzentiene, F. Tomi và J. Casanova (2009). Phân tích tinh dầu Artemisia absinthium L. từ Litva bằng CC, GC (RI), GC-MS và 13C NMR, Nat. sản xuất. Giao tiếp. 4(8), 1934578X0900400820.
[37] PH Ribeiro, LM Santos, C. AG. Camara, FS Born và CW Fagg (2016). Thành phần hóa học theo mùa của các loại tinh dầu của hai loài eugenia và đặc tính diệt nấm của chúng, Quim. Nova. 39, 38-43.
[38] J. Calva, JM Castillo, N. Bec, J. Ramirez, JM Andrade, C. Larroque và C. Armijos (2019). Thành phần hóa học, sự phân bố đồng phân đối quang và hoạt tính AChE-BChE của tinh dầu Myrteola phyllodes (Benth) Landrum từ Ecuador, Rec. tự nhiên sản xuất. 13, 355-362.
[39] EM Mostafa (2020). Khám phá aurora B và chất ức chế kinase 4 phụ thuộc cyclin được phân lập từ scorzonera tortuosissima Boiss. và các nghiên cứu lắp ghép của họ, Pharmacog. tạp chí. 16 (96), 258-263.
[40] J. Yan, XB Liu, W.‑W. Zhu, X. Zhong, Q. Sun và Y.‑Z. Lương (2015). Chỉ số lưu giữ để xác định các hợp chất thơm bằng GC: Phát triển và ứng dụng cơ sở dữ liệu chỉ số lưu giữ, Sắc ký 78(1-2), 89-108.
Để biết thêm thông tin: david.deng@wecistanche.com WhatApp:86 13632399501















