Hội nghị tranh cãi KDIGO về bệnh thận: Bệnh thận trong khối u ác tính huyết học và gánh nặng của ung thư sau khi ghép thận
Mar 06, 2022
Jolanta Małyszko, Aristotelis Bamias, Farhad R. Danesh, Alicja Debska-´Slizien, Maurizio Gallieni, Morie A. Gertz, Jan T. Kielstein, Petra Tesarova, Germaine Wong, Michael Cheung,
David C. Wheeler, Wolfgang C. Winkelmayer, và Camillo Porta; cho những người tham gia hội nghị
1 Khoa Thận, Lọc máu và Nội khoa, Đại học Y Warsaw, Ba Lan;
2Second Propaedeutic Khoa Nội khoa, Đại học Quốc gia và Kapodistrian của Athens, Hy Lạp;
3 Khoa Thận, Trung tâm Ung thư MD Anderson của Đại học Texas, Houston, Texas, Hoa Kỳ;
4 Khoa Cận thận, Ghép tạng và Nội khoa, Đại học Y Gdansk, Gdansk, Ba Lan;
5 Đơn vị lọc máu và lọc máu, Khoa Y sinh và Lâm sàng Luigi Sacco, Đại học Di Milano, Milan, Ý;
6 Phân khu Huyết học, Khoa Y, Phòng khám Mayo, Rochester, Minnesota, Hoa Kỳ;
7 Phòng khám Y khoa V, Thận học, Thấp khớp, Lọc máu, Bệnh viện Giảng dạy Học thuật Braunschweig, Braunschweig, Đức;
8 Khoa Ung thư, Khoa Y 1, Đại học Charles và Bệnh viện Đại học Tổng hợp, Praha, Cộng hòa Séc;
9CentreforKidneyNghiên cứu, Bệnh viện Nhi đồng Westmead, Westmead, New South Wales, Úc;
10 Trường Y tế Công cộng Sydney, Đại học Sydney, New South Wales, Úc;
11KDIGO, Brussels, Bỉ;
12 Khoa Thận, Đại học London, London, Vương quốc Anh;
13George Institute for Global Health, Sydney, Australia;
14 Viện Y tế Thận học Selzman, Bộ phận Thận học, Khoa Y, Đại học Y khoa Baylor, Houston, Texas, Hoa Kỳ;
15 Khoa Nội và Trị liệu, Đại học Pavia và Khoa Ung thư Dịch, IRCCS Istituti Clinic Scienti fi ci Maugeri, Pavia, Ý
Vui lòng liên lạc để biết thêm thông tin:emily.li@wecistanche.com

Cistanche tubulosa ngăn ngừa bệnh thận
Mối quan hệ hai chiều giữa ung thư vàbệnh thận mãn tính(CKD) rất phức tạp. Bệnh nhân ung thư, đặc biệt là những bệnh nhân có khối u ác tính về huyết học như đa u tủy và ung thư hạch bạch huyết, có nhiều nguy cơ bị tổn thương thận cấp tính và suy thận. Mặt khác, bằng chứng mới nổi từ các phân tích đăng ký quan sát lớn đã liên tục cho thấy rằng nguy cơ ung thư tăng ít nhất 2- đến 3- lần ở những người ghép thận và nguy cơ gia tăng được quan sát không chỉ xảy ra ở những người những người đã được ghép thận nhưng cả những người đang chạy thận nhân tạo và mắc bệnh suy thận giai đoạn nhẹ đến trung bình. Sự tương tác giữa ung thư và CKD đã đặt ra những thách thức lớn về điều trị và lâm sàng trong việc quản lý những bệnh nhân này. Với tầm quan trọng của vấn đề và sự không chắc chắn, cũng như những tranh cãi hiện tại trong các bằng chứng hiện có, Bệnh thận: Cải thiện kết quả toàn cầu (KDIGO) đã tập hợp một hội đồng toàn cầu gồm các chuyên gia lâm sàng và khoa học đa ngành cho một hội nghị tranh cãi về bệnh thận để xác định các vấn đề quản lý chính trong thận học liên quan đến bệnh nhân ác tính. Báo cáo này bao gồm những tranh cãi đã được thảo luận về bệnh ở các khối u ác tính huyết học, cũng như ung thư saughép thận. Tổng quan về các ưu tiên nghiên cứu trong tương lai cũng được thảo luận.
Ung thư đang được công nhận là một biến chứng lớn ở bệnh nhân mắc bệnh thận mãn tính (CKD). Mức độ của nguy cơ gia tăng thay đổi tùy theo mức độ nghiêm trọng của CKD, với nguy cơ lớn nhất trong sốngười ghép thận. Bằng chứng thuyết phục từ các phân tích quan sát dọc đã cho thấy nguy cơ vượt quá nguy cơ ung thư và tử vong liên quan đến ung thư ở những người ghép thận cao hơn ít nhất 2- lần so với dân số nói chung phù hợp với giới tính và tuổi.1,2 Cụ thể, nguy cơ cao mắc các bệnh ung thư liên quan đến vi rút như bệnh tăng sinh bạch huyết và sarcoma Kaposi gấp 10- lần.1 Bệnh ác tính về huyết học hoặc ung thư cũng liên quan đến nhiều vấn đề về thận, chẳng hạn như CKD, chấn thương thận cấp tính (AKI), rối loạn điện giải, viêm cầu thận và ban xuất huyết giảm tiểu cầu huyết khối. Cả CKD và AKI đều có thể do các quá trình liên quan đến bệnh ác tính hoặc các phương pháp điều trị bệnh gây ra.
Ở những bệnh nhân có khối u ác tính về huyết học, CKD có thể do tổn thương trực tiếp bởi tế bào ung thư hoặc tổn thương gián tiếp thông qua cơ chế trung gian miễn dịch, chẳng hạn như xảy ra với bệnh thận màng.4 AKI ở bệnh nhân ác tính có thể do thâm nhiễm lympho ở thận, bệnh thận hình thành nhiều u tủy và các bệnh gammopat đơn dòng, và hội chứng ly giải khối u (TLS), và những bệnh này xảy ra chủ yếu ở các khối u ác tính với gánh nặng khối u cao và sự đảo lộn tế bào nhanh chóng. CKD.7 Nguy cơ AKI có thể tăng lên bởi một số yếu tố: mất nước do nôn mửa, tiêu chảy, tắc nghẽn đường tiết niệu, rối loạn dịch và điện giải, dùng thuốc cản quang, thuốc chống viêm không steroid, kháng sinh độc với thận và độc tính trên thận của hóa trị liệu hoặc thuốc nhắm mục tiêu.4–6 Tỷ lệ mắc AKI ở bệnh nhân có bệnh lý ác tính huyết học cấp độ kích thích cao tới 68,5 phần trăm sử dụng tiêu chí RIFLE (rủi ro, thương tích, thất bại, mất chức năng, giai đoạn cuốibệnh thận [ESKD]), with >90% các trường hợp do giảm tưới máu, hoại tử ống thận cấp tính, TLS, độc tố thận, hoặc tăng bạch cầu lympho bào thực quản.
Cải thiện kết quả ung thư thông qua chẩn đoán tốt hơn và các liệu pháp cá nhân hóa chẳng hạn như các loại thuốc nhắm mục tiêu miễn dịch và gen chọn lọc đã dẫn đến một số lượng ngày càng tăng những người sống sót sau ung thư9, những người có nguy cơ mắc bệnh thận cao hơn. Chăm sóc bệnh nhân ung thư ngày càng trở nên chuyên biệt và liên ngành, hiện đang đòi hỏi sự hợp tác giữa các chuyên gia về thận học, y học cấy ghép, ung thư y tế, chăm sóc nguy kịch, dược học / dược lâm sàng và chăm sóc giảm nhẹ, ngoài các bác sĩ phẫu thuật và bác sĩ tiết niệu. Để xác định các vấn đề quản lý chính trong khoa thận liên quan đến bệnh nhân ác tính, KDIGO (Bệnh thận: Cải thiện Kết quả Toàn cầu) đã tập hợp một hội đồng toàn cầu gồm chuyên môn khoa học và lâm sàng đa ngành để triệu tập một hội nghị tranh cãi về bệnh thận ở Milan, Ý, vào tháng 12 năm 2018. Báo cáo này đề cập đến các vấn đề liên quan đến thận trong các khối u ác tính huyết học và thảo luận về gánh nặng củaung thư thậnngười ghép tạng.
BỆNH KIDNEY TRONG HEMATOLOGY
Nhận biết và ngăn ngừa hội chứng ly giải khối u
TLS là một trường hợp cấp cứu về bệnh ung thư máu do chết tế bào khối u tự phát hoặc do hóa trị. Nó có thể được phân loại như một dạng phòng thí nghiệm hoặc dạng lâm sàng, trong đó rối loạn chuyển hóa có thể lấn át khả năng cân bằng nội môi và gây ra những hậu quả nghiêm trọng về mặt lâm sàng. Sự phát triển của các loại thuốc ung thư học mới đã vượt qua các cuộc điều tra liên quan đến TLS, và do đó tỷ lệ mắc và tỷ lệ hiện mắc của TLS không được xác định rõ ràng. Nguy cơ TLS bị ảnh hưởng bởi loại khối u, gánh nặng khối u, đặc điểm của bệnh nhân và loại liệu pháp. Định nghĩa thường được sử dụng của TLS10 chứa thành phần chấn thương thận đã lỗi thời cần được cập nhật để phản ánh định nghĩa KDIGO AKI hiện tại.11
Để đánh giá nguy cơ TLS, nên đo các chất điện giải (natri, kali, phốt pho, magiê và canxi), mức lọc cầu thận ước tính (eGFR), và axit uric ở tất cả bệnh nhân lúc ban đầu. Tần suất của các phép đo trong phòng thí nghiệm phụ thuộc vào hồ sơ rủi ro. Vai trò dự đoán của acid uric ban đầu đối với TLS hiện vẫn chưa được biết rõ. Với sự sẵn có mở rộng của một số tiểu thuyết nhắm mục tiêu các tác nhân dựa trên tế bào miễn dịch và phân tử, chẳng hạn như kháng thể đơn dòng, chất ức chế kinase phụ thuộc cyclin, chất ức chế proteasome, tác nhân pro-apoptotic và tế bào thụ thể kháng nguyên chimeric (CAR) –T, phổ của các khối u có nguy cơ mắc bệnh TLS đang ngày càng mở rộng và hiện nay bao gồm bệnh bạch cầu lymphocytic mãn tính, bệnh bạch cầu dòng tủy mãn tính, bệnh đa u tủy và một số khối u đặc.
Thuốc ức chế men xanthine oxidase (XOI) là nhóm thuốc được lựa chọn để ngăn ngừa TLS, mặc dù liều lượng và mức mục tiêu của axit uric chưa được xác định (Bảng 114–16) .17 Đối với bệnh nhân TLS bình thường.chức năng thận, allopurinol là XOI ưu tiên. Febuxostat là một giải pháp thay thế để giảm axit uric; trong thử nghiệm FLORENCE, bắt đầu dùng 1 liều cố định febuxostat 2 ngày trước khi bắt đầu hóa trị và chỉ tiếp tục trong 7 đến 9 ngày đã đạt được sự kiểm soát axit uric huyết thanh vượt trội đáng kể so với allopurinol, với tính năng bảo toàn và an toàn chức năng thận tương đương. Đối với các phương pháp điều trị lâu hơn (như với bệnh gút), hồ sơ an toàn của febuxostat vẫn không chắc chắn. Dùng febuxostat trong thời gian ngắn có thể là một lựa chọn thay thế tốt, đặc biệt khi cân nhắc rằng có thể đạt được đáp ứng nhanh với acid uric huyết thanh. Mặc dù febuxostat hiện nay là thuốc thông thường và giá thành đã giảm, nhưng nó vẫn đắt hơn allopurinol, khiến giá thành ở nhiều vùng trở thành một yếu tố. Ngoài ra, rasburicase là một phương pháp điều trị rất hiệu quả đối với TLS, mặc dù liều lượng và tần suất tối ưu của nó chưa được biết, đồng thời tính khả dụng và chi phí có thể bị cấm. Các báo cáo gần đây chỉ ra rằng rasburicase liều đơn có hiệu quả trong việc ngăn ngừa và quản lý TLS, 20 có thể mở rộng khả năng tiếp cận. Liệu pháp tuần tự của rasburicase và XOI đã được chứng minh là có hiệu quả. 21
Bằng chứng liên quan đến việc ngăn ngừa TLS còn hạn chế. Trong các thử nghiệm về bệnh bạch cầu cấp tính, tỷ lệ TLS được báo cáo là 42% và 53% với alvocidib (với cytarabine và mitoxantrone tuần tự) và 15% với dinaciclib. Venetoclax có nguy cơ liên quan cao nhất đối với việc gây ra TLS trong bệnh bạch cầu lymphocytic mãn tính (8,3% và 8,9% trong 2 thử nghiệm), trong khi tỷ lệ mắc TLS là # 5% với brentuximab vedotin (đối với u lympho tế bào lớn đồng sản), carfilzomib và lenalidomide (đối với đa u tủy ), dasatinib (đối với bệnh bạch cầu nguyên bào lympho cấp tính), và oprozomib (đối với các khối u ác tính huyết học khác nhau) .22 Mặc dù vai trò dự đoán của axit uric ban đầu đối với TLS vẫn còn đang được tranh luận, các hướng dẫn về TLS ở trẻ em và người lớn cho thấy nguy cơ phát triển TLS và thận các sự kiện tăng lên lần lượt 1. 75- và 2. 21- lần đối với mỗi lần tăng mg / dl axit uric huyết thanh.

Các vấn đề liên quan đến đa u tủy
Điều trị ngoài cơ thể để kiểm soát bệnh thận đa u tủy xương.
Nếu các phương pháp điều trị ngoài cơ thể được sử dụng, mức độ của chuỗi ánh sáng không chứa trong huyết thanh (FLC) sẽ cần được theo dõi. Nồng độ FLC cao có liên quan đến khả năng sống sót tổng thể và không có biến cố thấp hơn, 24 trong khi giảm FLC nhanh chóng dẫn đến cải thiện khả năng sống sót của thận và tổng thể.25 Các biện pháp hỗ trợ và hóa trị luôn phải được bắt đầu càng sớm càng tốt, trước khi thay huyết tương điều trị (TPE) hoặc chạy thận nhân tạo cắt cao (HCO-HD). Vẫn chưa biết liệu TPE có cải thiện kết quả thận hay tổng thể ở bệnh nhân đa u tủy có FLC cao hay không (Bảng 1). Hầu hết các thử nghiệm điều tra TPE trong bệnh thận bó bột là từ thời kỳ tiền bortezomib, và không rõ liệu các tác nhân mới hơn có dẫn đến nồng độ FLC tích phân thấp hơn theo thời gian hay không. Trong một thử nghiệm được công bố vào năm 1988 bao gồm 29 người tham gia, TPE đã chứng minh hiệu quả trong việc loại bỏ các chuỗi nhẹ khỏi tuần hoàn và cải thiện kết quả.26 Tuy nhiên, trong một nhóm bệnh nhân lớn hơn đang hóa trị trước khi giới thiệu bortezomib (n ¼ 104), TPE không cải thiện được điểm cuối tổng hợp tử vong, phụ thuộc vào lọc máu, hoặc tốc độ lọc cầu thận<30 ml/min="" per="" 1.73="" m2="" at="" 6="" months.27="" anecdotal="" data="" with="" high-volume="" selective="" plasma="" exchange="" are="" encouraging.28="" extracorporeal="" elimination="" of="" flc="" is="" not="" indicated="" in="" patients="" with="" normal="" kidney="" function.="" hyperviscosity="" syndrome="" is="" an="" indication="" for="" tpe,="" irrespective="" of="" other="" treatment="">
Vai trò của nồng độ FLC đối với việc bắt đầu hoặc ngừng điều trị ngoài cơ thể vẫn chưa được biết rõ. HCO-HD có thể loại bỏ hiệu quả các chuỗi nhẹ29 và đã được chứng minh là loại bỏ các tác nhân gây độc tế bào30 và thuốc giảm đau.31 Dữ liệu từ các thử nghiệm không kiểm soát cho thấy rằng việc sử dụng HCO-HD có thể dẫn đến cải thiện điểm cuối của thận. Tuy nhiên, trong một nghiên cứu trên những bệnh nhân bị bệnh thận do u tủy được điều trị bằng phác đồ hóa trị dựa trên bortezomib, việc sử dụng HCO-HD so với chạy thận nhân tạo thông thường không dẫn đến sự khác biệt có ý nghĩa thống kê về tính độc lập chạy thận nhân tạo ở thời điểm 3 tháng.34 Trong thời gian {{ 9}} năm theo dõi 90 bệnh nhân tham gia thử nghiệm EuLITE nhãn mở, giai đoạn 2, ngẫu nhiên có đối chứng, 35 98 và 82 tác dụng phụ nghiêm trọng đã được báo cáo trong HCO-HD và chạy thận nhân tạo dòng chảy cao (HF- HD) các nhóm, tương ứng. Các tác dụng phụ nghiêm trọng thường gặp nhất là nhiễm trùng, các biến cố tim mạch và huyết khối, và các biến cố liên quan đến hệ cơ xương. Trong 90 ngày đầu tiên, 26 trường hợp nhiễm trùng (bao gồm 14 phổi) được báo cáo trong nhóm HCO-HD, và 13 trường hợp nhiễm trùng (bao gồm 3 phổi) đã được báo cáo trong nhóm HF-HD.35 Kết hợp những kết quả này không hỗ trợ cho việc bắt đầu HCO -HD giai đoạn 3 nghiên cứu. Với nhu cầu cải thiện các chiến lược điều trị trong bệnh thận do u tủy, việc kết hợp các kỹ thuật loại bỏ FLC hiệu quả với hóa trị hiệu quả nhưng có thể dung nạp được cần được nghiên cứu thêm.
Một báo cáo năm 2012 từ các mô hình động vật đã xác định được peptit vòng tuần hoàn của chất ức chế cạnh tranh can thiệp vào sự liên kết của các chuỗi nhẹ với protein Tamm-Horsfall, có thể mở đường cho việc loại bỏ nhu cầu đào thải ngoài cơ thể. Tuy nhiên, các nghiên cứu trên người vẫn chưa được tiến hành.
Quản lý các bệnh xương liên quan đến đa u tủy. Although bisphosphonates are contraindicated in patients with advanced kidney disease, single-dose (30 mg) pamidronate for hypercalcemia does not require dose adjustment if eGFR is >30 ml / phút trên 1,73 m2. Dữ liệu nghiên cứu kéo dài 12 tháng cho thấy pamidronate cũng có thể được sử dụng cho bệnh nhân chạy thận nhân tạo.37
Lựa chọn giữa liệu pháp bisphosphonate hoặc denosumab.Đối với bệnh đa u tủy mới được chẩn đoán, denosumab không thua kém axit zoledronic trong thời gian xảy ra các biến cố liên quan đến xương và có độc tính trên thận thấp hơn.38 Tuy nhiên, có một số dữ liệu hạn chế hỗ trợ cho sự không thua kém về độ an toàn của denosumab so với alendronat ở bệnh nhân chạy thận nhân tạo, đặc biệt liên quan đến nguy cơ hạ calci huyết nặng.39 Dữ liệu giai thoại cho thấy điều này cũng đúng đối với thẩm phân phúc mạc.40 Liệu bisphosphonate có liên quan đến các nguy cơ bất lợi hay không (Bảng 1).
Managing calcineurin inhibitors In recipients of allogeneic stem cell transplants, tacrolimus is associated with a lower likelihood of AKI relative to cyclosporine. Drug blood levels should be measured at regular intervals. It is unknown if lowering calcineurin inhibitor levels to reduce the risk of AKI elevates the risk of graft-versus-host disease. However, cyclosporine levels >195 mg / l vào ngày thứ 10 sau cấy ghép có liên quan đến việc giảm đáng kể khả năng mắc bệnh ghép vật chủ cấp tính sau khi cấy ghép tế bào gốc tạo máu toàn thể.41 Không rõ liệu có bất kỳ vai trò nào đối với sinh thiết thận ở bệnh nhân AKI. dùng thuốc ức chế calcineurin.
Vì các chất ức chế calcineurin có thể gây ra bệnh vi mạch huyết khối liên quan đến cấy ghép, các trường hợp tăng huyết áp, giảm tiểu cầu và tăng lactate dehydrogenase nên nghi ngờ bệnh vi mạch huyết khối.
Vai trò của sinh thiết thận đối với liệu pháp phục hồi thận trong bệnh thận bó bột
Sinh thiết thận được khuyến nghị đặc biệt để xác nhận bệnh thận bó bột trong AKI sau khi bắt đầu hóa trị. Không nên trì hoãn liệu pháp trong khi chờ đợi kết quả sinh thiết. Bất kỳ lo ngại nào về việc tăng nguy cơ chảy máu ở nhóm bệnh nhân này đều không được tài liệu ủng hộ.42
Tỷ lệ bệnh thận không nguyên bào ở những bệnh nhân nghi ngờ mắc bệnh thận bó bột là không rõ. Điều tra xem có các dấu ấn sinh học có thể được sử dụng để dự đoán xác suất phát triển bệnh thận bó bột hay không có thể là điều đáng giá. Nhóm công tác về u tủy quốc tế năm 2014 đã cập nhật các tiêu chí chẩn đoán đa u tủy đã xác định bệnh thận bó bột chuỗi nhẹ là sự kiện xác định u tủy và các dấu ấn sinh học đã được xác nhận của bệnh ác tính.43
Xác định bệnh nhân nào mắc bệnh gammopnal đơn dòng có ý nghĩa về thận nên được điều trị
Tất cả bệnh nhân mắc bệnh gammopnal đơn dòng có ý nghĩa thận (MGRS) và là mục tiêu của hóa trị liệu (ví dụ, bệnh amyloidosis chuỗi nhẹ Ig, bệnh lắng đọng chuỗi nhẹ, bệnh cầu thận C3, hội chứng tăng sinh bạch huyết sau ghép, immunotactoid, v.v.) nên được điều trị. Trong một báo cáo đồng thuận từ Nhóm nghiên cứu bệnh thận và bệnh đơn dòng quốc tế (IKMG), 44 MGRS được xác định lại là một rối loạn tăng sinh dòng vô tính tạo ra Ig đơn dòng độc cho thận và không đáp ứng các tiêu chuẩn huyết học đã xác định trước đó để điều trị một bệnh ác tính cụ thể. Chẩn đoán bệnh liên quan đến MGRS được thiết lập bằng sinh thiết thận và các nghiên cứu miễn dịch huỳnh quang để xác định các lắng đọng Ig đơn bộ (mặc dù những lắng đọng này rất ít ở những bệnh nhân mắc bệnh cầu thận C3 hoặc bệnh vi mạch huyết khối). Theo đó, IKMG khuyến cáo thực hiện sinh thiết thận trong các trường hợp nghi ngờ mắc MGRS; Điện di protein huyết thanh và nước tiểu và cố định miễn dịch, cũng như phân tích các FLC huyết thanh, cũng nên được thực hiện để xác định Ig đơn dòng có trách nhiệm. Cuối cùng, chọc hút tủy xương và sinh thiết nên được tiến hành để xác định dòng tăng sinh bạch huyết. Phương pháp đo tế bào dòng chảy có thể hữu ích trong việc xác định các dòng vô tính nhỏ. Các xét nghiệm di truyền bổ sung và nghiên cứu lai huỳnh quang FL tại chỗ rất hữu ích cho việc xác định dòng vô tính và đưa ra các khuyến nghị điều trị. Tuy nhiên, các cạm bẫy vẫn tồn tại ở mỗi bước chẩn đoán, và mức độ nghi ngờ lâm sàng cao vẫn được yêu cầu khi chẩn đoán MGRS.45 Chỉ định và thời gian bắt đầu điều trị vẫn còn tranh cãi (Bảng 1), mặc dù bất kỳ quyết định nào cũng nên được chia sẻ giữa các bác sĩ huyết học, bác sĩ thận học và bệnh nhân theo kiểu đa khoa.

Hóa trị để điều trị bệnh gammopnal đơn dòng có ý nghĩa về thận
Điều trị MGRS thường bao gồm một chất ức chế proteasome, mặc dù sự kết hợp tối ưu của các chất này vẫn chưa được biết.
Ứng cử để ghép thận ở bệnh nhân u tủy và bệnh amyloidosis đang lọc máu Các báo cáo giai đoạn47 gợi ý rằng việc ghép thận có thể được xem xét sau khi bệnh thuyên giảm hoàn toàn u tủy48 và có thể được theo đuổi sau khi thuyên giảm hoàn toàn bệnh amyloidosis về mặt huyết học. Tuy nhiên, thời gian thuyên giảm tối ưu trước khi cấy ghép vẫn chưa được biết (Bảng 1). Không có rối loạn chức năng cơ quan ngoài thượng thận do amyloid được coi là điều kiện tiên quyết để cấy ghép. Peptide natri lợi niệu loại N-pro-B như một dấu hiệu của suy tim chỉ được sử dụng hạn chế trong bệnh thận mạn tính tiến triển.
Liều lượng thuốc gây độc tế bào ở bệnh nhân CKD G3b-G5D
Các nghiên cứu về liều lượng ở bệnh nhân CKD G3b-G5D không phải là một phần của quá trình phê duyệt điều trị theo quy định ở Hoa Kỳ hoặc Châu Âu. Do đó, thiếu dữ liệu để xác định liều lượng tối ưu của hầu hết các thuốc gây độc tế bào ở bệnh nhân CKD G3b – G5D.49 Các cơ quan quản lý cần giải quyết vấn đề này và một chiến lược có thể là thực hiện các nghiên cứu sau khi đưa thuốc ra thị trường là bắt buộc (Bảng 1).
Vai trò của thiết bị hấp thụ mới đối với bệnh nhân huyết học / ung thư
Không có lợi ích nào được chứng minh của việc sử dụng thiết bị hấp phụ mới ở bệnh nhân huyết học / ung thư.50 Không biết liệu thiết bị hấp phụ có mang lại lợi ích so với các phương pháp trị liệu kháng interleukin -6 hay không hoặc nếu có bất kỳ dấu hiệu nào cho việc sử dụng thiết bị hấp phụ mới trong giai đoạn 3 của AKI với nhu cầu điều trị thay thế thận.
Thuốc giảm đau để kiểm soát cơn đau lâu dài ở bệnh nhân CKD bị đau liên quan đến ung thư
Điều trị thích hợp cơn đau ở bệnh nhân ung thư vẫn còn là một vấn đề chưa được giải quyết. Không có cơ sở chứng minh việc tránh dùng opioid ở những bệnh nhân có khối u ác tính. Các thuốc chống viêm không steroid phải được sử dụng thận trọng ở những bệnh nhân mắc bệnh thận mạn tính tiến triển hoặc có nguy cơ cao mắc bệnh này. Tỷ lệ lợi ích trên nguy cơ của gabapentin và pregabalin nên được đánh giá trên cơ sở từng cá nhân. Tất cả các thành phần của hướng dẫn của Tổ chức Y tế Thế giới cần được xem xét.
Xác định bệnh nhân ung thư huyết học nào bị CKD có thể được điều trị bằng các tác nhân kích thích erythropoietin
Ở bệnh nhân ung thư huyết học, tình trạng sắt nên được tối ưu hóa trước khi bắt đầu điều trị bằng tác nhân kích thích erythropoietin (ESA). Dữ liệu về tác dụng phụ tiềm ẩn của ESA ở bệnh nhân có khối u rắn không thể áp dụng cho bệnh nhân huyết học. Nên cân nhắc giữa rủi ro đối với hoạt động thúc đẩy khối u của erythropoietin so với lợi ích. Tương tự, nồng độ hemoglobin mục tiêu không rõ ràng. Các ESA đường uống mới hơn chưa được đánh giá trong quần thể bệnh nhân này.
Ra quyết định bắt đầu hoặc chấm dứt liệu pháp thay thế thận
Kỳ vọng về những gì lọc máu có thể đạt được một cách hợp lý ở bệnh nhân ung thư huyết học thường cao không thực tế ở bệnh nhân và người chăm sóc của họ52; Do đó, ước tính tiên lượng tổng thể dựa trên tình trạng toàn diện của từng bệnh nhân (bao gồm tuổi tác, tình trạng hoạt động, sức khỏe yếu, suy dinh dưỡng, bệnh đi kèm và thuốc phối hợp) là bắt buộc. Cần có phương pháp tiếp cận nhóm liên ngành và cải thiện giao tiếp giữa bác sĩ huyết học / bác sĩ ung thư và bác sĩ thận học để tạo điều kiện thuận lợi cho cuộc thảo luận về việc có nên bắt đầu điều trị thay thế thận hay không. Khi đó, trao đổi thông tin đồng cảm với bệnh nhân bằng cách sử dụng phương pháp ra quyết định chung có thể dẫn đến một quyết định sáng suốt, tôn trọng quyền tự chủ của bệnh nhân và phù hợp với mục tiêu và giá trị cá nhân của bệnh nhân.
Các yếu tố dự đoán về khả năng sống sót ngắn hạn sau khi bắt đầu điều trị thay thế thận không có sẵn cho bệnh nhân ung thư huyết học. Không bắt đầu liệu pháp thay thế thận là một cách tiếp cận hợp lệ, vì kết quả có thể tương tự như liệu pháp lọc máu với chất lượng cuộc sống tốt hơn. Nhìn chung, các chỉ thị nâng cao chưa được sử dụng nhiều, và có thể việc tư vấn về các chỉ thị nâng cao có thể là một chiến lược hiệu quả để tránh phải ra quyết định trong những trường hợp khẩn cấp.
Đối với những bệnh nhân không bắt đầu lọc máu hoặc ngừng lọc máu, nên xem xét và cung cấp dịch vụ chăm sóc giảm nhẹ. Một phương pháp khả thi khác là trải qua thời gian thử nghiệm liệu pháp thay thế thận trong phòng chăm sóc đặc biệt.
UNG THƯ TRONG BỆNH NHÂN CHUYỂN HÓA KIDNEY Dịch tễ học
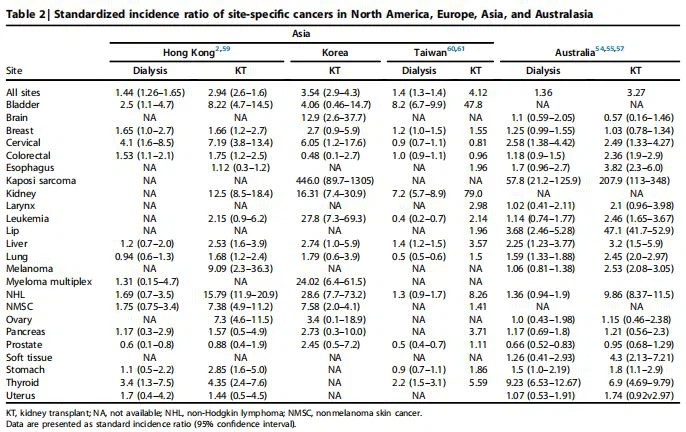
Dữ liệu đăng ký mạnh mẽ và thuyết phục chỉ ra rằng nguy cơ ung thư tổng thể ởngười ghép thậnđược tăng ít nhất 2- lên 2. 5- lần so với dân số chung phù hợp với tuổi và giới tính (Bảng 21,2,54–64). 1,54–56 Bệnh nhân có nguy cơ gia tăng là những người mắc bệnh ung thư liên quan đến vi rút như sarcoma Kaposi (20- lần), ung thư cổ tử cung (5- đến 10- lần) và bệnh tăng sinh bạch huyết sau cấy ghép. 1,54 Khác khối u ác tính cơ quan đặc như ung thư đại trực tràng và ung thư phổi (khoảng 2- đến 3- lần) làm tăng tỷ lệ mắc bệnh khiêm tốn so với dân số chung phù hợp với tuổi và giới tính. 1,54 Các bệnh ung thư khác, chẳng hạn như vú và tuyến tiền liệt, không gây ra rủi ro vượt mức cho những người được cấy ghép. Vì nguy cơ ung thư gia tăng cũng đã được chứng minh ở những bệnh nhân lọc máu và những người bị CKD mức độ sớm đến trung bình, gánh nặng ung thư gia tăng ở các cơ sở CKD có thể không liên quan đến ức chế miễn dịch đơn thuần mà còn có thể do các tình trạng liên quan đến CKD, chẳng hạn như urê huyết và viêm gia tinh mãn tính. 57,59,62
Ung thư là nguyên nhân gây tử vong hàng đầu ở những người được ghép tạng.2 Dữ liệu cho thấy nguy cơ tử vong trong dân số ghép tạng tăng ít nhất 2- đến 3- lần so với dân số chung phù hợp về độ tuổi và giới tính. 63 Nguyên nhân của việc gia tăng nguy cơ chưa rõ ràng nhưng có thể là do tỷ lệ mắc ung thư tăng, sự khác biệt về sinh học khối u trong bối cảnh ức chế miễn dịch, và / hoặc sự khác biệt trong cách tiếp cận hóa trị liệu, đặc biệt là giữa những người nhận với các bệnh đi kèm. Nguy cơ gia tăng ung thư và tử vong liên quan đến ung thư được quan sát thấy trong các quần thể cấy ghép chủ yếu là do ung thư liên quan đến vi rút, chẳng hạn như bệnh tăng sinh bạch huyết sau ghép (vi rút Epstein-Barr), sarcoma Kaposi, u lympho tràn dịch nguyên phát (herpesvirus 8 ở người), da , ung thư hầu họng, amidan, ung thư hậu môn sinh dục (cổ tử cung, âm đạo, âm hộ, hậu môn, dương vật [virus u nhú ở người]), ung thư biểu mô tế bào Merkel (Merkel cell polyomavirus) và ung thư biểu mô tế bào gan (virus viêm gan B và C).
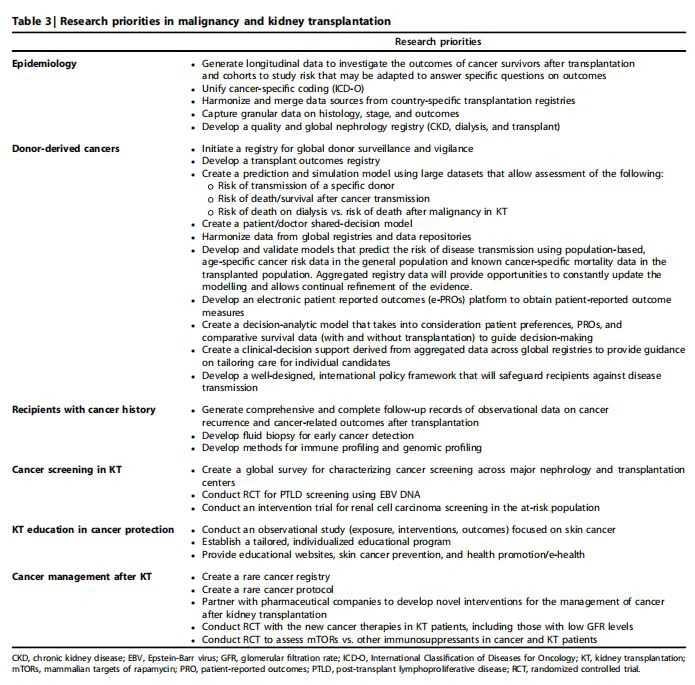
Dữ liệu dịch tễ học về tỷ lệ mắc và kết quả của những người ghép tạng bị ung thư được dựa trên các phân tích đăng ký quan sát. Việc báo cáo cho các cơ quan đăng ký này chủ yếu là tự nguyện và các câu hỏi liên quan đến tính đầy đủ của chúng đã được đưa ra.60 Các mối quan tâm cụ thể liên quan đến kết quả được xác định như thế nào; dữ liệu có được báo cáo chính xác và đầy đủ hay không; thiếu các chi tiết liên quan đến mô học, giai đoạn và các kết quả lâu dài hơn; thiếu một tiêu chuẩn tham chiếu mạnh mẽ — ví dụ, liên kết dữ liệu với các cơ quan đăng ký ung thư nơi việc thu thập dữ liệu là bắt buộc; và thiếu một hệ thống mã hóa chung xác định kết quả ung thư. Hầu hết các cơ quan đăng ký người nhận cấy ghép được phát triển ở các nước có thu nhập cao. Điều quan trọng là phải hỗ trợ sự phát triển của các cơ quan đăng ký ghép tạng và lọc máu xuyên suốt và mạnh mẽ ở các nước có thu nhập thấp đến trung bình. Các cơ hội và ưu tiên nghiên cứu được liệt kê trong Bảng 3.
Sự lây truyền ung thư của người hiến tặng ở những người nhận cấy ghép
Hiếm khi lây truyền ung thư từ người hiến tặng. Tỷ lệ lây truyền bệnh ước tính (từ cả người hiến tặng còn sống và đã qua đời) khác nhau giữa 1 và 2 trường hợp trên 1 0, 000 người ghép tạng, mặc dù những ước tính này phụ thuộc vào độ lệch báo cáo58 và có thể mô tả thấp hơn bệnh thực tế tỷ lệ mắc bệnh. Nguy cơ lây truyền bệnh phụ thuộc vào loại ung thư, từ dưới 0,1% trong số các bệnh ung thư không xâm lấn tại chỗ đến hơn 10% trong số các bệnh ung thư ác tính như u ác tính.2 Mặc dù việc lây truyền bệnh là không thường xuyên nhưng nó có thể gây tàn phá sự kiện cho bệnh nhân, gia đình họ và nhóm cấy ghép vì tiên lượng của những người nhận bị bệnh do người hiến tặng nói chung là xấu.65 Các trường hợp tử vong liên quan đến bệnh do người hiến tặng thường xuyên được báo cáo trên các phương tiện truyền thông, điều này làm dấy lên lo ngại và lo sợ trong cộng đồng .
Cấy ghép ở những bệnh nhân có tiền sử ung thư
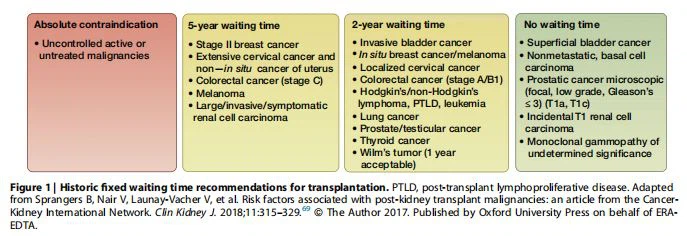
Các khuyến nghị về khả năng đủ điều kiện cấy ghép ở những bệnh nhân bị ung thư trước đó chỉ rõ rằng các ứng viên tiềm năng phải thuyên giảm hoàn toàn sau khi điều trị ung thư triệt để, không có bằng chứng về bệnh đang hoạt động. Tuy nhiên, thời gian chờ được khuyến nghị trước khi niêm yết khác nhau đáng kể giữa các hướng dẫn.66 Có ít bằng chứng chất lượng để hướng dẫn việc ra quyết định. Thời gian chờ đợi từ khi thuyên giảm hoàn toàn đến khi được liệt kê phụ thuộc vào nguy cơ bệnh tái phát và khả năng sống sót sau đó. Các đánh giá có hệ thống gần đây về các nghiên cứu quan sát đã chỉ ra rằng nguy cơ tử vong do ung thư cụ thể vượt quá ở những người nhận có tiền sử ung thư cao hơn ít nhất 3- lần so với những người không có tiền sử ung thư.67 Dữ liệu mới nổi cho thấy thời gian chờ đợi là không yếu tố quyết định tái phát bệnh sau khi cấy ghép68; tuy nhiên, những dữ liệu này cần được diễn giải một cách thận trọng vì chúng có thể chịu tác động của thiên vị lựa chọn và thời đại.
Do các đặc điểm của bệnh nhân thay đổi và sự ra đời của các liệu pháp mới như liệu pháp nhắm mục tiêu, thuốc ức chế điểm kiểm soát hoặc kết hợp cả hai để quản lý ung thư, các tiêu chí để liệt kê không nên cố định, như đã từng được thực hiện trước đây (Hình 1) .69 Thay vào đó, các tiêu chí phải năng động và được cá nhân hóa và cần cân nhắc đến sở thích của bệnh nhân và sự đánh đổi tiềm năng giữa chất lượng cuộc sống và lợi ích sống sót khi cấy ghép, xác suất tử vong sớm trong khi chạy thận, và nguy cơ tái phát bệnh và tử vong do ung thư sau khi cấy ghép.
Tầm soát ung thư ở những người ghép thận
Sàng lọc cấy ghép tạo cơ hội để phát hiện và điều trị các tổn thương tiền ác tính. Các hướng dẫn sàng lọc hiện tại trong quần thể ghép tạng phần lớn được ngoại suy và áp dụng từ dân số chung, và không có bằng chứng dựa trên thử nghiệm để hỗ trợ chúng. khác với những người dân chung. Một nghiên cứu gần đây về tầm soát ung thư đại trực tràng bằng các xét nghiệm chẩn đoán miễn dịch phân một lần ở bệnh nhân CKD (bao gồm cả những người ghép thận) đã cho thấy hiệu quả thuận lợi, nhưng các biến chứng chính do nội soi đi làm là cao.72 Cũng có sự khác biệt đáng kể trong thực hành sàng lọc trên các các trung tâm cấy ghép trên toàn thế giới. Các chương trình sàng lọc dựa trên dân số đối với ung thư cổ tử cung, đại trực tràng, ung thư vú và tuyến tiền liệt được phổ biến ở hầu hết các quốc gia có thu nhập cao. Do nguy cơ gia tăng của các loại ung thư khác, chẳng hạn như ung thư thận, bệnh tăng sinh hệ bạch huyết sau cấy ghép, và ung thư phổi và da, việc tầm soát định kỳ các loại ung thư này được thực hiện ở nhiều trung tâm trên toàn thế giới. Tuy nhiên, bằng chứng để hỗ trợ tần suất, phương thức và dân số mục tiêu để sàng lọc là không chắc chắn.
kết quả xét nghiệm đại tràng cao.72 Ngoài ra còn có sự khác biệt đáng kể trong thực hành sàng lọc ở các trung tâm cấy ghép lớn trên toàn thế giới. Các chương trình sàng lọc dựa trên dân số đối với ung thư cổ tử cung, đại trực tràng, ung thư vú và tuyến tiền liệt được phổ biến ở hầu hết các quốc gia có thu nhập cao. Do nguy cơ gia tăng của các loại ung thư khác, chẳng hạn như ung thư thận, bệnh tăng sinh hệ bạch huyết sau cấy ghép, và ung thư phổi và da, việc tầm soát định kỳ các loại ung thư này được thực hiện ở nhiều trung tâm trên toàn thế giới. Tuy nhiên, bằng chứng để hỗ trợ tần suất, phương thức và dân số mục tiêu để sàng lọc là không chắc chắn.
Bất chấp các khuyến nghị tầm soát hiện tại, tỷ lệ hấp thu để kiểm tra vú và cổ tử cung định kỳ ở dân số được cấy ghép vẫn còn thấp.73 Lý do cho việc hấp thu thấp là do nhiều yếu tố. Công việc định tính đã chỉ ra rằng bệnh nhân nhận thức được tính nhạy cảm của họ với nguy cơ ung thư cao hơn nhưng cũng ưu tiên các vấn đề khác liên quan đến bệnh thận và bệnh lý của họ.74 Họ cũng lo ngại về những tác hại tiềm ẩn và chi phí liên quan đến việc xét nghiệm thông thường.75,76 Chất lượng cần có bằng chứng liên quan đến việc tầm soát định kỳ các loại ung thư khác. Một số gợi ý để mở rộng cơ sở bằng chứng được liệt kê trong Bảng 3.
Giáo dục bệnh nhân
Các chiến lược giáo dục để ngăn ngừa ung thư giữa những người nhận ghép tạng tồn tại đối với ung thư da nhưng không áp dụng đối với các loại ung thư nội tạng rắn khác. Giáo dục bệnh nhân nên bắt đầu sớm, nghĩa là trước hoặc trong khi xác định CKD tiến triển. Một chương trình giáo dục cũng nên tôn trọng quan điểm và sở thích của bệnh nhân. Các trang web về sức khỏe điện tử có thể cung cấp giáo dục kỹ lưỡng ở cấp độ đọc cơ bản.
Kiểm soát ung thư sau khi ghép thận
Việc quản lý ung thư sau khi ghép thận rất phức tạp. Đối với bệnh nhân phát triển ung thư saughép thận, cách tiếp cận truyền thống tập trung vào việc giảm ức chế miễn dịch tổng thể, với việc sử dụng các tác nhân hóa trị liệu do bác sĩ chuyên khoa ung thư quản lý. Liều lượng giảm ức chế miễn dịch sau khi cấy ghép có thể phụ thuộc vào loại, giai đoạn ung thư và nhiều yếu tố khác. Tuy nhiên, cách tiếp cận này cần được cân bằng cẩn thận với nguy cơ bị từ chối allograft. Thiếu dữ liệu dựa trên thử nghiệm tiềm năng để cung cấp thông tin về quản lý ức chế miễn dịch, bao gồm giảm liều và / hoặc ngừng ức chế miễn dịch, còn thiếu. Mục tiêu của động vật có vú của chất ức chế rapamycin (sirolimus và everolimus) có thể có vai trò đầy hứa hẹn trong việc kiểm soát ung thư sau khi cấy ghép (đặc biệt với ung thư da không tế bào biểu bì và sarcoma Kaposi), do tác dụng ức chế miễn dịch và chống ung thư đồng thời của chúng.
Các liệu pháp chống ung thư nhắm mục tiêu mới bao gồm thuốc ức chế điểm kiểm soát và các liệu pháp miễn dịch khác hiện đã có sẵn để điều trị các khối u ác tính huyết học và cơ quan rắn ở giai đoạn cao. Trên nhiều loại khối u, các tác nhân này có hiệu quả cao hơn các liệu pháp gây độc tế bào tiêu chuẩn. Tuy nhiên, phần lớn các thử nghiệm can thiệp đánh giá hiệu quả của các tác nhân mới đã loại trừ những người được cấy ghép. Hồ sơ an toàn và hiệu quả của các tác nhân này trong quần thể bị ức chế miễn dịch vẫn chưa được biết. Đặc biệt, có những báo cáo và hàng loạt trường hợp cho thấy việc sử dụng kháng nguyên liên kết với tế bào lympho T chống PD1, độc tế bào, và các chất điều biến miễn dịch khác ở những người nhận cấy ghép có thể dẫn đến đào thải allograft cấp tính. 80–83 Đây vẫn là một vấn đề gây tranh cãi vì ở đó là các báo cáo trường hợp khác trong đó việc sử dụng everolimus thay cho các chất ức chế calcineurin không ngăn chặn được sự đào thải allograft ở những bệnh nhân dùng ipilimumab hoặc pembrolizumab.
Sự phát triển của cơ quan đăng ký hợp tác toàn cầu về ung thư có thể cho phép chia sẻ dữ liệu và tạo cơ hội cho các đối tác trong ngành và sự tham gia của bệnh nhân trong các thử nghiệm lâm sàng về các liệu pháp chống ung thư mới.
PHẦN KẾT LUẬN
Những người tham gia hội nghị nhấn mạnh tầm quan trọng của sự hợp tác giữa các bác sĩ chuyên khoa thận, huyết học / ung thư, và các chuyên gia cấy ghép, cũng như các dược sĩ, trong việc chăm sóc sức khỏe và thử nghiệm lâm sàng.
Bất chấp tần suất xuất hiện của nó, AKI là một thành phần của TLS để dự phòng và điều trị tối ưu cũng như việc sử dụng khác biệt giữa XOI và rasburicase vẫn chưa được biết đến. Thiếu dữ liệu về liều lượng và độc tính của các loại thuốc cũ và mới được sử dụng cho các bệnh huyết học và ung thư đã dẫn đến tổn thương thận cấp và mãn tính. Các công ty dược phẩm nên đầu tư các nghiên cứu sau khi đưa ra thị trường không phù hợp để cải thiện khả năng giảm tác dụng phụ trên thận mà không ảnh hưởng đến hiệu quả điều trị. Đa u tủy là một trong những bệnh lý huyết học chủ yếu dẫn đến tình trạng lệ thuộc lọc máu mãn tính. Phương pháp tiếp cận chiết xuất thực và dược lý phải được tối ưu hóa để giảm tổn thương thận và nhu cầu lọc máu. Mặc dù việc lây truyền ung thư từ những người hiến thận là rất hiếm, nhưng điều bắt buộc là tất cả những người hiến thận đã chết và còn sống phải được sàng lọc các khối u ác tính. Đối với những ứng viên cấy ghép tiềm năng có tiền sử ung thư, nên chờ đợi thời gian sau khi ung thư thuyên giảm. Việc sàng lọc ung thư sau cấy ghép nên được điều chỉnh cho phù hợp với từng bệnh nhân. Việc tầm soát ung thư thận, bệnh tăng sinh bạch huyết sau ghép tạng, ung thư phổi và da nên được thực hiện tại các trung tâm cấy ghép trên toàn thế giới. Ở những người ghép thận được chẩn đoán mắc bệnh ung thư, việc điều trị ít hiệu quả hơn so với dân số chung. Thực hành lâm sàng Cur thuê dựa trên bằng chứng từ các nghiên cứu quan sát và phân tích đăng ký, nhưng quá trình thu thập dữ liệu và chất lượng của nó đòi hỏi phải cải thiện. Cần nghiên cứu sâu hơn về cơ chế bệnh sinh ung thư, công dụng của việc tầm soát ung thư và tác dụng của các phác đồ ức chế miễn dịch khác nhau.
RUỘT THỪA
Những người tham gia hội nghị khác
Ali K. Abu-Alfa, Lebanon; Hatem Amer, Hoa Kỳ; Gernot Beutel, Đức; Jeremy R.Chapman, Úc; Xiaohong Chen, Trung Quốc; Jerzy Chudek, Ba Lan; Laura Cosmai, Ý; Romano Danesi, Ý; Filippo De Stefano, Ý; Kunitoshi Iseki, Nhật Bản; Edgar A. Jaimes, Hoa Kỳ; Kenar D. Jhaveri, Hoa Kỳ; Artur Jurczyszyn, Ba Lan; RümeyzaTuran Kazancioglu, Thổ Nhĩ Kỳ; Abhijat Kitchlu, Canada; Christian Kollmannsberger, Canada; Amit Lahoti, Hoa Kỳ; Yang Li, Trung Quốc; Manuel Macía, Tây Ban Nha; Takeshi Matsubara, Nhật Bản; Dionysios Mitropoulos, Hy Lạp; Eisei Noiri, Nhật Bản; Mark A. Perazella, Hoa Kỳ; Pierre Ronco, Pháp; Mitchell H. Rosner, Hoa Kỳ; Maria Jose SolerRomeo, Tây Ban Nha; Ben Sprangers, Bỉ; Walter M. Stadler, Hoa Kỳ; Paul E. Stevens, Vương quốc Anh; Vladimír Tesar, Cộng hòa Séc; Verônica Torres da Costa eSilva, Brazil; David H. Vesole, Hoa Kỳ; Anitha Vijayan, Hoa Kỳ; Ond rej Viklický, Cộng hòa Séc; Biruh T. Workeneh, Hoa Kỳ; Motoko Yanagita, Nhật Bản; Elena Zakharova, Liên bang Nga.

NGƯỜI GIỚI THIỆU
1. Vajdic CM, McDonald SP, McCredie MR, et al. Tỷ lệ mắc bệnh ung thư trước và sau khi ghép thận. JAMA. 2006; 296: 2823–2831.
2. Au E, Wong G, Chapman JR. Ung thư ở người ghép thận. Nat Rev Nephrol. 2018; 14: 508–520.
3. Malyszko J, Kozlowski L, Kozlowska K, et al. Ung thư và thận: những liên lạc viên nguy hiểm hay cái giá phải trả cho sự tiến bộ của y học? 2017; 8: 66601–66619.
4. Jhaveri KD, Shah HH, Calderon K, và cộng sự. Các bệnh cầu thận được thấy cùng với ung thư và hóa trị: một bài tổng quan tường thuật. Thận Int. 2013; 84: 34–44.
5. Pierson-Marchandise M, Gras V, Morgan J, et al. Các loại thuốc chủ yếu thường gây ra chấn thương thận cấp tính: một nghiên cứu trường hợp không xảy ra trên cơ sở dữ liệu cảnh giác dược. Br J Clin Pharmacol. 2017; 83: 1341–1349.
6. Lâm AQ, Humphreys BD. Thận một lần: AKI ở bệnh nhân ung thư.Clin J Am Soc Nephrol. 2012; 7: 1692–1700.
7. Renaghan AD, Jaimes EA, Malyszko J, et al. Tổn thương thận cấp tính và CKD liên quan đến ghép tế bào gốc tạo máu. Clin J Am SocNephrol. Năm 2020; 15: 289–297.
8. Canet E, Zafrani L, Lambert J, và cộng sự. Tổn thương thận cấp ở bệnh nhân có khối u ác tính huyết học cấp độ cao mới được chẩn đoán: ảnh hưởng đến sự thuyên giảm và khả năng sống sót. PLoS Một. 2013; 8: e55870.
9. Torre LA, Siegel RL, Ward EM, Jemal A. Tỷ lệ và xu hướng tỷ lệ tử vong và tỷ lệ tử vong do ung thư toàn cầu — một bản cập nhật. Dấu ấn sinh học ung thư Epidemiol Trước đó. 2016; 25: 16–27.
10. Cairo MS, Bishop M. Hội chứng ly giải khối u: các chiến lược điều trị mới và phân loại. Br J Haematol. 2004; 127: 3–11.
11. Kellum JA, Lameire N, Nhóm Công việc Hướng dẫn KDIGO AKI. Chẩn đoán, đánh giá và xử trí chấn thương thận cấp tính: tóm tắt KDIGO (phần 1). Chăm sóc Crit. 2013; 17: 204.
12. Howard SC, Jones DP, Pui CH. Hội chứng ly giải khối u. N Engl J Med.2011; 364: 1844–1854.
13. McBride A, Tri fi lio S, Baxter N, và cộng sự. Quản lý hội chứng ly giải khối u trong thời đại của các liệu pháp điều trị ung thư mới. J Adv Pract Oncol. 2017; 8: 705–720.
14. Voelker R. Một cảnh báo khác cho febuxostat. JAMA. 2019; 321: 1245.
15. Bridoux F, Chevret S, Fermand JP. Chạy thận nhân tạo ở ngưỡng cắt cao trong bệnh thận do u tủy đúc: cần điều tra thêm. Lancet Haematol.2019; 6: e347.
16. Mazali FC, Johnson RJ, Mazzali M. Sử dụng thuốc hạ acid uric hạn chế bệnh thận do cyclosporin thực nghiệm. Nephron Exp Nephrol. 2012; 120: e12 – e19.
17. Bellos I, Kontzoglou K, Psyrri A, Pergialiotis V. Dùng Febuxostat để phòng ngừa hội chứng ly giải khối u: một phân tích tổng hợp. J Clin Pharm Ther. 2019; 44: 525–533.
18. Spina M, Nagy Z, Ribera JM, et al. FLORENCE: nghiên cứu ngẫu nhiên, mù đôi, quan trọng giai đoạn III về febuxostat so với allopurinol để phòng ngừa hội chứng ly giải khối u (TLS) ở những bệnh nhân có khối u ác tính huyết học có nguy cơ TLS từ trung bình đến cao. Ann Oncol. 2015; 26: 2155–2161.
19. Vadhan-Raj S, Fayad LE, Fanale MA, et al. Một thử nghiệm ngẫu nhiên giữa rasburicase liều duy nhất so với liều dùng hàng ngày ở những bệnh nhân có nguy cơ mắc hội chứng ly giải khối u. Ann Oncol. 2012; 23: 1640–1645.
20. Nauffal M, Redd R, Ni J, và cộng sự. Liều 6- mg rasburicase đơn lẻ: trải nghiệm tại một trung tâm y tế hàn lâm lớn. J Oncol Pharm Pract.2019; 25: 1349–1356.
21. Cortes J, Moore JO, Maziarz RT, và cộng sự. Kiểm soát acid uric huyết tương ở người lớn có nguy cơ mắc hội chứng ly giải khối u: hiệu quả và độ an toàn của rasburicase đơn độc và rasburicase, tiếp theo là allopurinol so với allopurinol đơn thuần - kết quả của một nghiên cứu đa trung tâm ở giai đoạn III. J Clin Oncol. 2010; 28: 4207–4213.
22. Howard SC, Tri fi lio S, Gregory TK, et al. Hội chứng ly giải khối u trong thời đại của các tác nhân mới và được nhắm mục tiêu ở những bệnh nhân có khối u ác tính về huyết học: một đánh giá có hệ thống. Ann Hematol.2016; 95: 563–573.
23. Coif fi er B, Altman A, Pui CH, et al. Hướng dẫn quản lý hội chứng ly giải khối u ở trẻ em và người lớn: một đánh giá dựa trên bằng chứng. J Clin Oncol. 2008; 26: 2767–2778.
24. Snozek CL, Katzmann JA, Kyle RA, và cộng sự. Giá trị tiên lượng của tỷ lệ chuỗi ánh sáng không có huyết thanh trong u tủy mới được chẩn đoán: được đề xuất đưa vào hệ thống phân loại quốc tế. Bệnh bạch cầu. 2008; 22: 1933–1937.
25. van Rhee F, Bolejack V, Hollmig K, và cộng sự. Nồng độ chuỗi ánh sáng không có trong huyết thanh cao và sự giảm nhanh chóng của chúng khi đáp ứng với liệu pháp điều trị là một dạng phụ đa u tủy tích cực với tiên lượng xấu. Máu. 2007; 110: 827– 832.
26. Zucchelli P, Pasquali S, Cagnoli L, Ferrari G. Thử nghiệm trao đổi huyết tương có kiểm soát trong suy thận cấp do đa u tủy. Thận Int. Năm 1988; 33: 1175–1180.
27. Clark WF, Stewart AK, Rock GA, et al. Trao đổi huyết tương khi u tủy biểu hiện như một suy thận cấp: một thử nghiệm ngẫu nhiên, có đối chứng. Ann Intern Med. 2005; 143: 777–784.
28. Kanda M, Sanada S, Kowata H, et al. Cải thiện thận với trao đổi huyết tương chọn lọc phân tử ở bệnh nhân đa u tủy loại Bence-Jones. Quay số Apher. 2016; 20: 420–422.
29. Mene P, Giammarioli E, Fo fi C, và cộng sự. Loại bỏ chuỗi ánh sáng tự do trong huyết thanh bằng cách thẩm thấu HFR ở bệnh nhân đa u tủy và chấn thương thận cấp tính: một loạt trường hợp. Máy ép máu thận Res. 2018; 43: 1263–1272.
30. Eden G, Kühn-Velten WN, Hafer C, Kielstein JT. Tăng cường thải trừ cyclophosphamide bằng thẩm tách máu liều cao: dược động học liều duy nhất ở bệnh nhân bị bệnh thận bó bột. Đại diện Vụ án BMJ 2018; bcr -2017-221735.
31. Arelin V, Schmidt JJ, Kayser N, và cộng sự. Loại bỏ methadone bằng cách lọc máu kéo dài sử dụng máy lọc máu có độ cắt cao: tác động đối với việc điều trị quá liều và kiểm soát cơn đau ở bệnh nhân được cắt bỏ chuỗi nhẹ. Clin Nephrol. 2016; 85: 353–357.
32. Gerth HU, Pohlen M, Görlich D, và cộng sự. Tác động của lọc máu cắt lớp cao đối với sự phục hồi của thận ở bệnh nhân đa u tủy phụ thuộc vào lọc máu: kết quả từ một nghiên cứu bệnh chứng. PLoS Một. 2016; 11. e0154993.
33. Buus NH, Rantanen JM, Krag SP, et al. Chạy thận nhân tạo bằng phương pháp cắt cao
bộ lọc trong bệnh thận đúc chuỗi nhẹ. Máu Purif. 2015; 40: 223–231.
34. Bridoux F, Carron PL, Pegourie B, et al. Ảnh hưởng của thẩm tách máu liều cao so với chạy thận nhân tạo thông thường đối với tính độc lập của quá trình chạy thận nhân tạo ở những bệnh nhân mắc bệnh thận bó bột do u tủy: một thử nghiệm lâm sàng ngẫu nhiên. JAMA. 2017; 318: 2099–2110.
35. Hutchison CA, Cockwell P, Moroz V, và cộng sự. Giới hạn cao so với chạy thận nhân tạo thông lượng cao đối với bệnh thận do u tủy đúc ở bệnh nhân được hóa trị liệu dựa trên bortezomib (EuLITE): một thử nghiệm ngẫu nhiên có đối chứng giai đoạn 2. Lancet Haematol. 2019; 6: e217 – e228.
Ying WZ, Wang PX, Sanders PW. Vai trò quan trọng của tín hiệu apoptosis-
