Sử dụng hợp chất phenolic từ thảm thực vật ô liu Nước ở gà thịt: Ảnh hưởng đến hệ vi sinh vật đường ruột và thời hạn sử dụng của philê vú Phần 3
Mar 12, 2022
Xin vui lòng liên hệoscar.xiao@wecistanche.comđể biết thêm thông tin
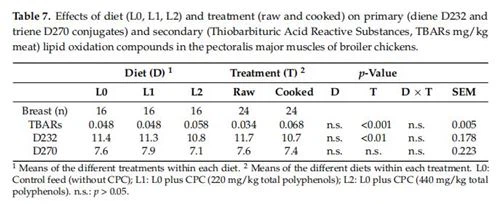
2.7.Lipid Oxi hóa
Quá trình oxy hóa lipid đã được nghiên cứu thông qua phép đo thứ cấp (TBAR) và sơ cấp (D232 và D270)Quá trình oxy hóahợp chất (Bảng 7). Không có sự khác biệt đáng kể nào được ghi nhận giữa ba nhóm thử nghiệm, mặc dù điều đáng chú ý là có sự gia tăng nhẹ giá trị TBAR của gà ở nhóm L2 so với ở nhóm L1 và L 0, trong khi D232 cho thấy xu hướng ngược lại. Hai chỉ số phân tích này có mối tương quan đáng kể (TBARs so với D232 r =-0. 5, tr<0.001 and="" tbars="" vs.="" d270r=""><0.05). the="" cooking="" treatment="" caused="" decreases="" in="" the="" primary="" oxidation="" products=""><0.01), which="" were="" followed="" by="" increases="" in="" the="" secondary="" ones="" (p=""><0.001). no="" interactions="" between="" diet="" and="" cooking="" were="" observed.="" on="" the="" contrary,="" [31]and="" [45]="" observed="" a="" significant="" reduction="" in="" tbars="" in="" the="" breasts="" from="" chickens="" whose="" diets="" were="" supplemented="" with="" either="" olive="" cake="" or="" omww.="" similarly,="" [46]="" observed="" a="" reduction="" in="" tbars="" in="" the="" quadriceps="" femoris="" of="" chickens="" whose="" diets="" were="" enriched="" with="" omww="" permeate="" and="" the="">

Vui lòng bấm vào đây để biết thêm
Oke và cộng sự. [16] đã thêm các thể tích khác nhau của chiết xuất lá ô liu (5, 10 và 15 mL / lít) vào nước uống cung cấp cho gà thịt chủng Abor mẫu Anh, quan sát thấy tác động đáng kể đến việc giảm nồng độ malondialdehyde (MDA) trong máu. Ibrahim và cộng sự. [42], quan sát thấy sự giảm đáng kể nồng độ MDA trong ức gà thu được bằng cách bổ sung vào chế độ ăn với mức độ tăng dần của bã ô liu khô lên men hoặc lên men bằng enzym. Không giống như các nghiên cứu khác, tác dụng bảo vệ chống lại quá trình oxy hóa chất béo trong mô cơ không được quan sát thấy trong nghiên cứu hiện tại. Có nhiều yếu tố tạo ra sự thay đổi và khác biệt giữa các nghiên cứu. Ngoài giống vật nuôi và thời gian vỗ béo, các yếu tố khác như thành phần dinh dưỡng của khẩu phần, lượng thức ăn ăn vào, nhiệt độ môi trường cùng với các điều kiện căng thẳng khác có thể dẫn đến kết quả rất khác nhau mà thường khó so sánh. Không phải cuối cùng là loại ma trận mà chế độ ăn uống được làm giàu với phenol (bánh ô liu, bã ô liu, chiết xuất lá ô liu, chiết xuất nước thực vật, chỉ là một vài cái tên) do nồng độ của các hợp chất hoạt động và sự hiện diện của các chất bổ sung với tác dụng hiệp đồng hoặc bảo vệ có trong cùng chất nền, có thể ảnh hưởng đáng kể đến hoạt động chống oxy hóa cả in vivo và trong mô thịt sau khi giết mổ [47]. Những lợi ích sức khỏe tiềm ẩn từ việc tích hợp các chất phụ gia chống oxy hóa trong thịt tươi và các sản phẩm thịt không phải lúc nào cũng được chứng minh [48]. Ngược lại, nhiều hợp chất oxy hóa lipid và protein chính và phụ, chẳng hạn nhưhydroperoxit, epoxit,4- hydroxynonenal, malonaldehydeđược công nhận là chất gây ung thư tiềm ẩn hoặc có thể ảnh hưởng đến quá trình truyền tín hiệu tế bào như trường hợp của các hợp chất cacbonyl [49]. Trong trường hợp thịt tươi, khả năng tăng khả năng chống oxy hóa thông qua khẩu phần của động vật là một triển vọng rất gợi ý, đặc biệt là trong việc sử dụng các chất tự nhiên thay vì tổng hợp. Trên thực tế, không giống như các sản phẩm làm từ thịt mà công nghệ cung cấp các khả năng can thiệp khác nhau để tăng khả năng chống oxy hóa, ở thịt tươi, phương pháp thay thế duy nhất để can thiệp thông qua chế độ ăn của động vật là xử lý nhằm vào bề mặt của sản phẩm tuy nhiên phải phù hợp với pháp luật hiện hành. Số lượng phenol còn lại được đo trong thịt ức của nghiên cứu này không có khả năng gây ra lợi ích sức khỏe trực tiếp nhưng gián tiếp có thể gây ra. Chẳng hạn, việc nấu chín thịt làm mất đi sự bảo vệ của chất chống oxy hóa mô, do đó, sự làm giàu mô thịt bằng các hợp chất vẫn hoạt động ngay cả sau khi xử lý nhiệt, như trường hợp củaphenol, rất được quan tâm ứng dụng vì sự gia tăng thời hạn sử dụng và độ an toàn của chính sản phẩm. Lý do tại sao các hiệu ứng trong video lẫn video cũ đều không được quan sát như là hệ quả của thử nghiệm cho ăn với CPC, đáng được điều tra thử nghiệm thêm, đặc biệt là về sự tương tác giữapolyphenol trong chế độ ăn uốngvà hệ vi sinh vật đường ruột của gà mà nó tận dụng một phần đáng kể các hiệu ứng sinh hóa tiềm ẩn của phenol [9,10].

3. Vật liệu và phương pháp 3.1. Cơ sở thí nghiệm
Thử nghiệm được thực hiện trong chuồng gia cầm của Trang trại Thực nghiệm của Đại học Padova (Legnaro, Padova, Ý) sau 6 tháng ngừng hoạt động. Chuồng nuôi gia cầm được trang bị hệ thống làm mát, thông gió cưỡng bức, sưởi bằng bức xạ và hệ thống đèn có kiểm soát. Tổng cộng 12 chuồng có dây lưới (2,5 × 2,4 m; 6 m2) đã được sử dụng, mỗi chuồng được trang bị năm núm uống nước (khoảng cách: 20cm) và máng ăn hình tròn (đường kính: 30 cm) để phân phối thức ăn thủ công. Mỗi chuồng có sàn bê tông phủ lớp dăm bào (sâu 5 cm, 2,5 kg / m).
Ánh sáng được cung cấp 24 h / ngày trong 2 ngày đầu tiên sau khi gà đến chuồng gia cầm. Sau đó, số giờ ánh sáng giảm dần cho đến khi đạt được chu kỳ quang 18L: 6D, chu kỳ này được duy trì từ 12 ngày tuổi trở đi.

Cistanche có thể cải thiện khả năng miễn dịch
3.2. Động vật, Nhóm thí nghiệm và Bản ghi In Vivo
Nghiên cứu đã được phê duyệt bởi Ủy ban Đạo đức cho Thử nghiệm Động vật (Organismo per la Protezione del Benessere Animale; OPBA) của Đại học Padova (dự án 17/2016; Số 154392 ngày 10 tháng 5 năm 2016). Tất cả động vật đều được xử lý theo các nguyên tắc của Chỉ thị 2010/63 / EU [50] về việc bảo vệ động vật được sử dụng cho các mục đích thí nghiệm và khoa học khác. Các nhà nghiên cứu liên quan đến việc xử lý động vật là các chuyên gia về động vật (bằng Tiến sĩ hoặc Thạc sĩ về Khoa học Động vật) và / hoặc các bác sĩ thú y.
Tổng cộng 144 1- gà con một ngày tuổi (Ross 308) đã được vận chuyển bằng một chiếc xe tải thương mại, tuân thủ Quy định của Hội đồng (EC) số 1/2005 [51], đến các cơ sở thí nghiệm của trường Đại học. Tất cả gà con đã được tiêm phòng bệnh Marek, bệnh viêm phế quản truyền nhiễm và bệnh Newcastle tại trại giống. Gà con được cân riêng vào ngày chúng đến, được xác định bằng dấu chân, được phân bổ ngẫu nhiên trong số 12 chuồng (12 con / chuồng và 10 con / m²),và sau đó cân một lần mỗi tuần để đo trọng lượng sống của chúng cho đến khi giết mổ thương mại. Mức tiêu thụ thức ăn cho bút được đo hàng ngày trong suốt quá trình thử nghiệm. Ba chế độ ăn thương mại được thực hiện ở dạng vụn trong quá trình thử nghiệm (Martini SpA Longiano, Forli-Cesena, Ý): chế độ ăn P1 từ 0 đến 23 ngày, chế độ ăn P2 từ 24 đến 37 ngày và chế độ ăn P3 từ 38 ngày cho đến giết mổ ở 48 ngày (xem Tài liệu bổ sung cho dữ liệu phân tích, Bảng S1). Sản phẩm cô đặc phenolic thô (CPC) thu được như được mô tả bởi [12], một cách ngắn gọn, OVWs được xử lý bằng cách sử dụng các enzym có hoạt tính pectinase và hemicellulosic, sau đó chịu sự vi lọc, siêu lọc và thẩm thấu ngược. CPC được thêm vào khẩu phần ăn như sau :( i) L 0 Chế độ ăn kiểm soát (P3), (ii) L1 Chế độ ăn kiểm soát cộng với CPC (220 mg / kg thức ăn theo lý thuyết tổng phenol), (i) Chế độ ăn kiểm soát L2 cộng với CPC (440 mg / kg thức ăn theo lý thuyết tổng số phenol). Hàm lượng thực tế của các hợp chất phenolic riêng lẻ của CPC và của khẩu phần được báo cáo trong Bảng S2. Mỗi khẩu phần được lặp lại trong bốn chuồng (đồng nhất về trọng lượng sống ban đầu và sự thay đổi). CPC được cung cấp từ 24 ngày tuổi cho đến khi giết mổ thương mại ở 48 ngày (xem Tài liệu bổ sung về thành phần phenolic của CPC). Tất cả các con vật đều được cho ăn ad libitum trong suốt quá trình thử nghiệm và chế độ ăn bổ sung được chuẩn bị hàng tuần.
Để xác định thành phần của cộng đồng vi sinh vật đường ruột, người ta đã thu thập các miếng gạc cloacal (4 con / chuồng) ở 23,34 tuổi và 44 ngày tuổi cho tổng số 12 con (4 con trên mỗi chế độ ăn) đã được kiểm tra ba lần (36 miếng gạc) tổng số mẫu được thu thập).
3.3. Giết mổ thương mại, ghi chép chất lượng thịt và thân thịt
Ở 48 ngày tuổi, sau khi rút thức ăn và nước (tương ứng trong 7 giờ và 2 giờ), tất cả gà được giết mổ trong lò mổ thương mại. Gà được cân từng con trước khi nhốt. Tất cả gà từ chuồng được xếp vào lồng vận chuyển (chiều cao, 62,5cm × 16 0 cm × 25,0 cm; diện tích sàn, 1 m²). Việc bốc dỡ và vận chuyển từ các cơ sở thí nghiệm đến lò mổ thương mại và chuồng nuôi nhốt trước khi giết mổ mất khoảng 3 giờ. Gà được giết mổ theo quy trình tiêu chuẩn của lò mổ thương mại. Thân thịt được thu hồi sau 2 giờ làm lạnh ở 2 độ và được cân riêng để đo tỷ lệ gia công giết mổ [52].
Hai mươi bốn giờ sau khi giết mổ, thân thịt được mổ xẻ để lấy các cơ chính của ngực tách ra khỏi vú [53].
Trong quá trình thử nghiệm, đã ghi nhận mức thiệt hại 17,4% (25 con gà) do chết. Trong số 119 thân thịt, 72 thân thịt được chỉ định phân tích vi sinh trong thời hạn sử dụng (Phần 2.4 giải thích việc thiết lập thành phần hệ vi sinh vật có vú bằng các phương pháp phụ thuộc và không phụ thuộc vào nuôi cấy), trong khi 47 thân thịt còn lại được đông lạnh (-40 độ) và sau đó được sử dụng để đánh giá các chế phẩm gần nhau và tốc độ oxy hóa lipid của thịt sống và chín (đoạn 3.5).

3.4.Đánh giá thời hạn sử dụng
3.4.1.Chuẩn bị ức gà đóng gói
P cơ chính được đóng gói riêng lẻ trong các khay polyetylen mật độ thấp được bọc trong màng PVC dày 12 μm(Weigel,KOEX412,Gruppo Fabbri,Vignola,Modena,Ý) và được bảo quản ở 4 ± 1 độ. Trong tủ lạnh (Majolo "Plus 1 00 Seasoning Con-troller, Majolo, Cadoneghe, Padova, Ý). Tiếp xúc với ánh sáng được cố định từ 8: 00 đến 20:00 bằng đèn huỳnh quang 36 W [54]. Cài đặt bảo quản được thiết kế với mục đích bắt chước các điều kiện làm lạnh trong quá trình bán hàng. Các gói được lấy mẫu ngẫu nhiên ở 24,72,120, 180, 216 và 264 giờ từ ngày giết mổ
3.4.2. Phân tích cảm quan
Đánh giá cảm quan về vú tươi được thực hiện theo [37] sử dụng hệ thống cho điểm 3- điểm danh giá (1= không được chấp nhận, 2= có thể chấp nhận được, 3= chất lượng tốt). Chỉ số cảm quan tổng hợp (SI) được tính bằng [(2 × điểm mùi cộng 2 × điểm màu cộng với 1 × điểm kết cấu) / 5], với điểm 1,8 đóng vai trò là ngưỡng để xác định mẫu hư hỏng. Phân tích cảm quan được thực hiện bởi tám tham luận viên được đào tạo.
3.4.3 Phân tích vi sinh vật học của thịt vú trong thời hạn sử dụng
Các phân tích vi sinh được thực hiện theo các quy trình được mô tả bởi [38]. Các cơ chính của ngực (dài khoảng 2 cm x sâu 1 cm x rộng 2 cm) được cắt bỏ vô trùng dọc theo mỗi bên vú để thu được 25 mẫu đại diện cho mỗi bên vú. Các mẫu được trộn trong túi dạ dày với 225 mL nước đệm pepton và được phân tích sau các độ pha loãng thích hợp. Để tách chiết DNA, 1 mL của mỗi chất đồng nhất được thu thập trong ống Eppendorf 2 mL và ly tâm ở 13.500 × g trong 1 phút (máy ly tâm Eppendorf 5425, Hamburg, Đức). Sau đó, phần nổi phía trên được loại bỏ và viên đá được đông lạnh ở -80 độ. Một số chỉ tiêu vi sinh vật đã được nghiên cứu để mô tả động lực của quần thể vi sinh vật trong thời gian bảo quản như sau: Tổng số lượng sống sót (TVC) và tổng số lượng vi sinh vật sống (TPC) được đánh giá trên đĩa đếm đĩa Agar (Biokar Diagnostics, Beauvais, Pháp) , và các đĩa được ủ ở 30 độ trong 72 giờ hoặc ở 4 độ trong 10 ngày. Enterobacteriaceae được thống kê với Thạch đường mật đỏ Violet (Biokar Diagnostics, Beauvais, Pháp) ở 37 độ trong 24 giờ. Vi khuẩn lactic (LAB) được phân tích trên De Man, Rogosa và Sharpe Agar (Biokar Diagnostics, Beauvais, Pháp) trong điều kiện yếm khí ở 30 độ trong 48 giờ. Pseudomonas spp. số lượng được đánh giá trên Pseudomonas Agar Base bổ sung cetrimide, fucidine, và cephaloridine ở 25 độ trong 48 giờ (Oxoid Ltd., Basingstoke, Hampshire, UK). Số lượng vi khuẩn sinh H2S (giả định là Shewanella spp.) Được thực hiện trên thạch sắt (Lyngby, Laboratorios Conda, Torrejon de Ardoz, Tây Ban Nha) ở 25 độ trong 48 giờ. Kết quả được báo cáo là log10 CFU / g thịt.
3.4.4.pH và mất mát nhỏ giọt
Máy đo pH (Portamess 910, Knick, Berlin, Đức), được trang bị một điện cực cụ thể (Mettler Toledo, Milano, Ý), được sử dụng để đo các giá trị pH bằng cách đưa vào các cơ chính của ngực làm ba lần ở bên bụng của chúng. Tổn thất nhỏ giọt được đánh giá theo phương pháp được trình bày bởi [55] sử dụng phương pháp túi. Các lát cắt khoảng 2,5 cm từ bề mặt của ngực được đưa vào túi polyetylen và treo qua đêm ở 2 ± 1 độ C. Sự mất mát nhỏ giọt (phần trăm) được tính theo công thức sau: [(trọng lượng ban đầu - trọng lượng cuối cùng) / trọng lượng ban đầu ].
3.4.5. Nồng độ phenol trong chế độ ăn uống và trong cơ ngực
Việc chiết tách phenol được tiến hành trên 5g mẫu chế độ ăn đã xay nhỏ trộn với 5 0 mL dung dịch metanol / nước (80/20 (o / o) chứa 20mg / L butylated hydroxy-toluen (BHT), hỗn hợp được đồng nhất bằng máy phân tán dạng que (IKA, T50 Ultra-Turrax, Werke, Staufen, Đức) trong 1 phút ở tốc độ 7000 vòng / phút, được ly tâm ở 9327 × g trong 10 phút và phần nổi phía trên được thu hồi. Quy trình được lặp lại hai lần và dịch chiết thu được sau đó được cô đặc bằng thiết bị cô quay (Buchi Rotavapor, R -210, Thụy Sĩ) cho đến khi đạt thể tích cuối cùng là 20 mL. Một hộp mực SPE Bond Elut Jr-C18,1 g (Agilent Technologies, Santa Clara, CA, USA ), trước đó đã được kích hoạt với 10 mL metanol và 10 mL nước, được nạp 1 mL dịch chiết nước, quá trình rửa giải được thực hiện với 50 mL metanol. Sau khi loại bỏ dung môi trong chân không, dịch chiết phenol được hòa tan trong 1 mL dung dịch bao gồm metanol / nước (50:50 v / v) và được lọc qua bộ lọc ống tiêm polyvinylidene florua (PVDF) (0,2 mm). phân tích định tính và định lượng các hợp chất phenolic của dịch chiết được tiến hành theo [31] bởi
HPLC (Mod. 1100 Agilent Technologies, Santa Clara, CA, USA), được trang bị cột C18 (Spherisorb ODS -1 (250 mm × 4,6 mm) cỡ hạt 5 um, do Waters SpA (Milan, Ý) cung cấp) . Các hợp chất phenolic được phát hiện bằng cách sử dụng DAD đặt ở 280 nm. Việc định lượng polyphenol được xác định bằng cách sử dụng các đường chuẩn đơn cho mỗi hợp chất và kết quả được biểu thị bằng mg kg -1. Hydroxytyrosol (3, {{ 10}} DHPEA) được lấy từ Cabru SpA (Milan, Ý), tyrosol p-HPEA được mua từ Merck Life Science Srl (Milan, Ý) và verbascoside được lấy từ Extrasynthese (Genay, Pháp). Dạng dialdehyde của de-carboxymethyl oleuropein aglycone (3, 4- DHPEA-EDA) được chiết xuất từ dầu ô liu nguyên chất theo quy trình được báo cáo từ [56].
Tổng cộng 10gram thịt đã được trộn với 50 mL methanol và nước(80/20,o/ø)chứa axit formic {{0}}. 2 phần trăm và 20 mg / L BHT. Dung dịch được đồng nhất bằng dụng cụ phân tán dạng que (IKA, T50 Ultra-Turrax, Werke, Staufen, Đức) trong 1 phút ở tốc độ 7000 vòng / phút, được ly tâm ở 4146 × g trong 10 phút và phần nổi phía trên được thu hồi. Thao tác này được lặp lại hai lần và hai phần dịch chiết được thu thập và metanol được loại bỏ bằng thiết bị cô quay (Buchi Rotavapor, R -210, Thụy Sĩ). 20 mL dịch chiết được nạp vào hộp mực SPE Bond Elut HF Mega BE-C18,5g (Agilent Technologies, Santa Clara, CA, USA), trước đó đã được kích hoạt với 20 mL metanol và 20 mL nước; rửa giải được thực hiện với 50 mL metanol. Sau khi loại bỏ dung môi trong chân không, dịch chiết phenol được thu hồi với 0,5 ml dung dịch bao gồm metanol / nước(50∶50 o/ø)và được lọc qua polyvinylidene fluoride(PVDF)bộ lọc ống tiêm (0. 2 mm). Các phép phân tích HPLC của các chất chiết phenol được tiến hành theo [56] với cùng một thiết bị như đã báo cáo ở trên. Hydroxytyrosol được phát hiện bằng cách sử dụng detector huỳnh quang (FLD) hoạt động ở bước sóng kích thích 280 nm và phát xạ 313 nm. Việc định lượng hydroxytyrosol được thực hiện bằng cách sử dụng đường chuẩn và kết quả được biểu thị bằng ug / kg.

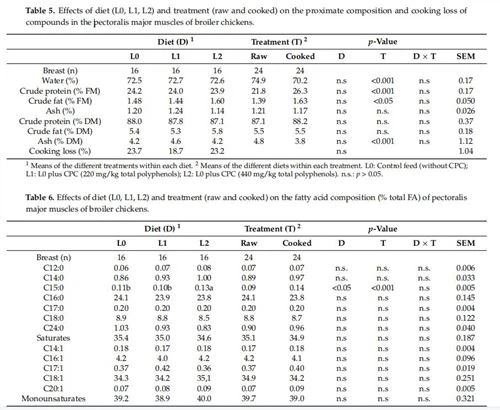
3.5. Phân tích thành phần gần đúng, tổn thất khi nấu và axit béo
Thành phần gần đúng, cấu hình axit béo và độ ổn định oxy hóa được đánh giá trên cả mẫu sống (P. chính bên phải) và mẫu nấu chín (P. maijor bên trái). Sau khi rã đông, tổn thất khi nấu được đánh giá theo [53] với các sửa đổi sau: Nửa bên trái của mỗi vú được cân, đóng gói chân không và nấu trong nồi cách thủy ở 8 0 độ trong 45 phút. Sau đó, vú được làm lạnh đến 4 độ và giữ trong tủ lạnh (4 độ) trong 72 giờ trước khi được đóng gói và cân lại để tính hao hụt khi nấu là [(trọng lượng thịt nấu chín) / trọng lượng thịt sống ] × 100). Phần cơ, cả sống và chín, được nghiền mịn (hai lần 2500 vòng / phút x 10 giây, Retsch, Dusseldorf, Đức) và đem đi phân tích độ ẩm, protein thô và tro [57], trong khi hàm lượng chất béo thô được xác định bằng phương pháp đã trình bày bởi [58]. Một cách ngắn gọn, 200 mL hỗn hợp diclometan / metanol 1: 1 được thêm vào 5g mẫu, được đồng nhất ở tốc độ 11, 000 / phút trong 1 phút (Ultraturrax T25 Basic, Ika Werke. Staufen, Đức), và ủ tại 60 C trong tủ sấy (hệ thống PID, M 120- VF, dụng cụ MPN, Bernaggio, MB, Ý) trong 20 phút. Sau đó, 100 mL diclometan khác được thêm vào, và sau khi đồng nhất (11, 000 / phút trong 1 phút) mẫu được lọc (giấy lọc nhanh) và 100 mL KCl 1 M được thêm vào dịch thấm. Sau khi ly tâm (AvantiJ-E, Beckman Coulter, Brea, CA, Hoa Kỳ) ở 1000 × g trong 30 m ở 4 độ, phần nổi phía trên được thải ra ngoài và dịch chiết hữu cơ được lọc qua natri sulphat khan. Một phần nhỏ (khoảng 10 g) được sử dụng để xác định trọng lượng phần trăm chất béo, phần còn lại được chưng cất (Rotavapor "R -210, Büchi, Essen, Đức) và chất béo khan được sử dụng để phân tích thêm. Axit béo metyl este (FAME) được điều chế bằng cách cân 0,015 g chất béo khan cho vào ống thủy tinh có nắp vặn [39], được hòa tan bằng 1 mL methanolic HCl 3 M (Sigma-Aldrich, St. Louis, MO, Hoa Kỳ) và ủ trong 2 giờ ở 60 độ. Sau đó, 1 mL nước khử ion được thêm vào và,sau khi trộn,FAME được thu hồi trong 1 mL n-hexan. FAME(1 μL)được phân tích bằng máy sắc ký khí (Shimadzu Italia Srl, kiểu 2 0 14, Milano, Ý) được trang bị đầu dò ion hóa ngọn lửa (đặt ở 25 0 độ) và một kim phun không chia tách (đặt ở 280 độ). Buồng nhiệt, giữ cột mao quản (Supelco SP -2560; 100 m × 0,25 mm × 0,2 um), được giữ ở 60 độ trong 8 phút. Sau đó, nhiệt độ được tăng lên 120 độ trong 1 phút với tốc độ 10 độ / phút, và sau đó từ 120 đến 240 độ với tốc độ 2,5 độ C / phút. Đường đẳng nhiệt cuối cùng được giữ ở 240 độ trong 20 phút. Axit béo được xác định bằng cách sử dụng hỗn hợp chuẩn bên ngoài (37 Thành phần FAME Mix, Supelco, Đức). Các phân tích được thực hiện trùng lặp.
3.6.Lipid Oxi hóa
Các hợp chất oxy hóa sơ cấp được xác định dưới dạng diene liên hợp bằng phân tích quang phổ trong trường tử ngoại sử dụng phiên bản sửa đổi của phương pháp được chỉ ra trong phụ lục của Council Reg.EU/2015/1833 [59]. Một cách ngắn gọn, 0. 0 1 ± 0,001g chất béo khan được cân vào bình chia độ 10 mL và được hòa tan bằng xyclohexan đo quang phổ đến vạch. Một máy quang phổ UV / Vis (Mod. 7800 Jasco UV / VIS, Thành phố Oklahoma, OK, Hoa Kỳ) đã được sử dụng để xác định các giá trị tắt cụ thể ở 232 (diene liên hợp) và 270 nm (trienes liên hợp) bằng cách sử dụng cùng dung môi với tài liệu tham khảo. Các sản phẩm thứ cấp của quá trình oxy hóa lipid được xác định theo phương pháp được trình bày bởi [60] với các sửa đổi, như sau: trong ống ly tâm, 8 mL dung dịch nước 5% (m / v) axit trichloroacetic và 5 mL n-hexan đã được thêm vào khoảng 2g mẫu đã đồng nhất. Sau khi đồng nhất với Ultraturrax trong 30s ở tốc độ cao. mẫu được ly tâm trong 3 phút ở 3000 × g ở 4C (Eppendorf 5810R; Eppendorf, Hamburg, Đức), và phần nổi phía trên được loại bỏ. Mẫu được lọc qua bộ lọc nhanh bằng giấy và 2,5 ml dịch lọc được thêm vào 2,5 ml dung dịch nước của axit thiobarbituric 0,02 M và ủ trong 35 phút ở 95 độ C trong bể điều nhiệt (lao động ED {{31} }; Seelbach, Baden-Württemberg, Đức). Sau khi làm nguội, độ hấp thụ được đo bằng máy quang phổ đặt ở bước sóng 532 nm. Dữ liệu được biểu thị bằng miligam malondialdehyde trên một kg thịt. Các phép đo được thực hiện lặp lại trên cả ức gà nấu chín và sống.
3.7. Trích xuất DNA và Chuẩn bị Thư viện NGS
DNA được tách chiết bằng Bộ tách DNA DNeasy PowerSoil (Qiagen, Hilden, Đức). Các viên thịt ức đồng nhất đã được rã đông với 6 0 0 uL dung dịch đệm L ly giải do bộ dụng cụ cung cấp. Các miếng gạc cloacal được cắt bằng kéo vô trùng, cho vào một ống siêu nhỏ chứa 600uL dung dịch đệm và 6 uL 2- mercaptoethanol (Sigma-Aldrich, St. Louis, MO, Hoa Kỳ). Các ống được trộn đều bằng cách sử dụng máy xoáy trong 5 phút và gạc được lấy ra. Đối với cả mẫu cloacal và viên thịt ức, tổng số 100 mg hạt 0,1 mm vô trùng (BioSpec, Bartlesville, OK, USA) đã được thêm vào, và một máy nghiền hạt (TissueLyser, Qiagen, Hilden, Đức) đã được sử dụng để thực hiện gián đoạn các bước lắc tốc độ cao (2 × 30 s ở 30 Hz). Tổng cộng 40 uL proteinase K (Qiagen, Hilden, Đức) đã được thêm vào và ủ ở 56 độ trong 90 phút. Sau bước này, hãy làm theo hướng dẫn của nhà sản xuất Bộ cách ly DNeasy PowerSoil9DNA. Nồng độ và độ tinh khiết của DNA được phân tích bằng máy quang phổ (NanoDrop ND -1000, Thermo Scientific, Waltham, MA, USA).
Phương pháp khuếch đại hai bước đã được sử dụng để xây dựng thư viện DNA 16S. Các mẫu được khuếch đại trong phản ứng 20- μL,mỗi bao gồm 5 μL DNA pha loãng,{{0}}. 4 uM của mỗi mồi (Bảng 1), 0,25 mM deoxynucleotide (dNTP), 1 × bộ đệm Phusion HF và 1 U Phusion DNA polymerase có độ trung thực cao (New England BioLabs, Inc., Ipswich , MA, Hoa Kỳ). PCR được tiến hành trong 2720 Thermal Cycler (Applied Biosystems, Foster City, CA, USA) với 25 chu kỳ 95 độ trong 30 giây, 60 độ hoặc 49 độ C trong 30 giây, 72 độ C trong 45 giây. Và phần mở rộng cuối cùng là 7 phút ở 72 độ. Ba lần lặp lại PCR được thực hiện trên mỗi mẫu.
Sản phẩm được tinh chế bằng Bộ công cụ làm sạch SPRIselect (Beckman Coulter Life Sciences, Indianapolis, IN, USA) và sau khi tinh chế hạt, dải mục tiêu được xác nhận bằng cách sử dụng 1,8% gel agarose. Mã vạch đã được giới thiệu bởi một phân tích PCR thứ hai với các mồi mang mã vạch dành riêng cho nền tảng. Mỗi phản ứng PCR 50- uL chứa sản phẩm PCR, 0. 2 μM cho mỗi mồi(Bảng 1),0. 3 mMdNTP,1 × Phusion HFbuffer,and1Phối hợp DNA polymerase có độ trung thực cao. Mười chu kỳ của hồ sơ PCR được mô tả ở trên đã được thực hiện.
Các sản phẩm PCR được tinh sạch bằng cách sử dụng bộ tinh lọc SPRIselect (Beckman Coulter Life Sciences, Indianapolis, IN, USA). Sau lần tinh chế cuối cùng, mỗi mẫu được định lượng bằng Qubit 2. 0 Fluorometer (Invitrogen, Life Technologies, Monza, Ý). Chất lượng thư viện amplicon đã được kiểm tra bằng Máy phân tích sinh học Agilent 2100 (Agilent Technologies, Palo Alto, CA, USA). Các thư viện được sắp xếp theo trình tự bằng cách sử dụng nền tảng Illumina MiSeq với một chu trình 300- kết thúc được ghép nối (Macrogen Inc., Seoul, Hàn Quốc).
4.Kết luận
Việc làm phong phú khẩu phần ăn của gà với phenol thu được bằng cách lọc và cô đặc nước thực vật của nhà máy dầu trong 24 ngày không liên quan đến sự khác biệt về tốc độ tăng trưởng của vật nuôi, tỷ lệ chuyển đổi thức ăn hoặc năng suất thân thịt. Nghiên cứu về hệ vi sinh vật đường ruột cho thấy ảnh hưởng đáng kể của thời gian cho ăn chứ không phải của khẩu phần đối với sự luân phiên của các nhóm vi sinh vật. Mặt khác, thành phần hệ vi sinh vật của thịt trong thời gian bảo quản cho thấy sự phát triển mạnh hơn của Pseudomonas trong các mẫu gà tiêu thụ thức ăn giàu phenol. Cuối cùng, không có sự khác biệt nào được quan sát thấy giữa các chế độ ăn đối với các chất đánh dấu phân tích (TBAR và dienes liên hợp) của quá trình oxy hóa lipid. Thay vào đó, hydroxytyrosol được xác định trong mô cơ của các mẫu gà ăn thức ăn có bổ sung phenol, cho thấy khả năng hấp thụ ở ruột phụ thuộc vào liều lượng. Vì quá trình oxy hóa chủ yếu xảy ra trong cấu trúc màng của tế bào cơ, nên các nghiên cứu sâu hơn là cần thiết để hiểu rõ hơn về sự phân bố của HT trong các ngăn tế bào và ngoại bào.
Bài viết này được trích từ Molecules 2021, 26, 4307. https://doi.org/10.3390/molecules26144307 https://www.mdpi.com/journal/molecules
