Căng thẳng oxy hóa và tổn thương do thiếu máu cục bộ/tái tưới máu trong ghép thận: Tập trung vào chứng Ferroptosis, Mitophagy và các chất chống oxy hóa mới
Nov 10, 2023
Trừu tượng:Mặc dù đã có nhiều tiến bộ về kỹ thuật và dược lý trongthuốc ghép thận, một số bệnh nhân có thể gặp phảibiến chứng cấp tính sau ghép tạng. Trong số các cơ chế liên quan đến những điều kiện này,thiếu máu cục bộ/tái tưới máu (I/R)chấn thươngcó thể có vai trò sinh lý bệnh chính vì đây là một trong những nguyên nhân hàng đầu gây chậm chức năng thận ghép (DGF), chức năng thận phục hồi chậm và cần phải lọc máu (thường là trong tuần đầu tiên sau ghép). DGF có tác động kinh tế và xã hội đáng kể vì nó liên quan đến việc nằm viện kéo dài và phát triển các biến chứng nghiêm trọng (bao gồm cả thải ghép cấp tính). Trong chấn thương I/R, stress oxy hóa đóng vai trò chính trong việc kích hoạt một số con đường bao gồmbệnh sắt từ, một cái chết tế bào do sắt gây ra, đặc trưng bởi sự tích tụ sắt và quá trình peroxid hóa lipid quá mức, và giảm phân, một sự thoái hóa có chọn lọc của ty thể bị tổn thương do quá trình tự thực. Ferroptosis có thể góp phần gây tổn thương thận, trong khi nguyên phân có thể có vai trò bảo vệ bằng cách giảm giải phóng các loại oxy phản ứng từ ty thể bị rối loạn chức năng. Sự hiểu biết sâu sắc về cả hai con đường có thể mang lại khả năng xác định các dấu ấn sinh học không xâm lấn chẩn đoán sớm mới của DGF và đưa ra các chiến lược dược lý mới có thể áp dụng trên lâm sàng. Trong bài đánh giá này, chúng tôi tóm tắt tất cả kiến thức liên quan trong lĩnh vực này và thảo luận về các chiến lược dược lý chống oxy hóa hiện tại mà trong tương lai có thể là phương pháp điều trị tiềm năng cho tổn thương I/R.
Từ khóa: tổn thương do thiếu máu cục bộ/tái tưới máu;căng thẳng oxy hóa; bệnh sắt từ;chứng giảm phân;ghép thận

CLICK VÀO ĐÂY ĐỂ NHẬN THẢO DƯỢC CHO THẬN
1. Giới thiệu
ghép thậnđại diện cho phương thức điều trị thay thế thận hiệu quả nhất về mặt chi phí cho bệnh nhân suy thận mãn tính không hồi phục (bệnh thận giai đoạn cuối, bệnh thận mãn tính giai đoạn 5) [1]. Tuy nhiên, bất chấp những tiến bộ liên tục về kỹ thuật và dược phẩm trong y học cấy ghép, một số bệnh nhân vẫn phát triển các biến chứng cấp tính sớm sau ghép tạng và chức năng thận phục hồi chậm do cần phải lọc máu (thường là trong tuần đầu tiên sau ghép). Tình trạng lâm sàng này, cụ thể là chức năng mảnh ghép bị trì hoãn (DGF), có tác động kinh tế và xã hội đáng kể vì nó liên quan đến việc nằm viện kéo dài [2], các phương pháp tiếp cận bằng nhiều loại thuốc (đặc biệt khi có tình trạng đào thải mảnh ghép cấp tính đồng thời) [3], và thời gian sống sót của mảnh ghép ngắn hơn [4]
Nguy cơ DGF cao hơn ở cơ quan cụ thểchương trình cấy ghép sử dụng thậntừ người hiến tặng không có nhịp tim, người già, mắc nhiều bệnh lý (ví dụ như tiểu đường, cao huyết áp), người nhận đã từng thất bại trong việc cấy ghép cùng loài và/hoặc tất cả đều nhạy cảm và các cơ quan bị tổn thương do chấn thương thận cấp tính và thời gian thiếu máu cục bộ kéo dài [5,6]
Đặc biệt, trong quá trình thiếu máu cục bộ, việc giảm đáng kể nguồn cung cấp oxy và hậu quả là tế bào chuyển từ chuyển hóa hiếu khí sang chuyển hóa kỵ khí, có thể làm giảm tốc độ sản xuất ATP [7] và gây ra sự tích tụ lactate (dẫn đến nhiễm toan). Do đó, các bơm Na+/K+ ATPase, Na+/H+ và Ca2+-ATPase có thể hoạt động không bình thường và natri, hydro và canxi tích tụ trong tế bào chất dẫn đến tăng thẩm thấu, tăng vận chuyển nước qua màng tế bào và sưng tế bào [8].
Trong quá trình tái tưới máu, sự gia tăng nhanh chóng lượng oxy và độ pH bình thường hóa có thểtăng cường canxi tế bàonồng độ kích hoạt protease cystein (ví dụ, calpains, caspase) và kích hoạt con đường apoptotic. Hơn nữa, tình trạng quá tải canxi kích thích mở các lỗ chuyển tiếp tính thấm của ty thể (mPTP) cho phép giải phóng các chất như cytochrom C, succinate và DNA ty thể có thể gây chết tế bào thông qua quá trình chết theo chương trình và hoại tử và đóng vai trò là các mẫu phân tử liên quan đến nguy hiểm/tổn thương (DAMP) thúc đẩy kích hoạt cả khả năng miễn dịch bẩm sinh và thích ứng [9–11]. Ngoài ra, các cơ chế này có thể dẫn đến xơ hóa kẽ tiến triển [12–14].
Hơn nữa, việc sản xuất quá mức các loại oxy phản ứng (ROS) sau thiếu máu cục bộ/tái tưới máu (I/R) có thể được gây ra bởi sự mất điều hòa của nhiều enzyme có khả năng làm giảm oxy phân tử tạo thành superoxide và/hoặc hydro peroxide như NADPH oxyase, nitric oxit synthase (NOS). ), chuỗi vận chuyển điện tử của ty thể và xanthine oxyoreductase (XOR).

XOR là một molybdoflavoenzym phức hợp kiểm soát bước giới hạn tốc độ của quá trình dị hóa purin và tồn tại ở hai dạng có thể chuyển đổi lẫn nhau là xanthine dehydrogenase (XDH) và xanthine oxidase (XO). XDH ưu tiên sử dụng NAD+ làm chất nhận điện tử, trong khi XO sử dụng O2 làm chất nhận điện tử cuối cùng, do đó thể hiện khả năng tạo ra ROS [15]. Enzyme này chuyển đổi hypoxanthine thành superoxide tạo ra xanthine (O2 −) và hydro peroxide (H2O2) có vai trò quan trọng trong việc điều hòa việc tuyển dụng và/hoặc kích hoạt bạch cầu điều phối tổn thương mô [16].
Ngoài ra, NADPH oxydase, phức hợp đa phân tử tạo ra superoxide hoặc H2O2, bao gồm bảy thành viên trong họ (NOX1–5, DUOX1–2) [17], có liên quan đến việc sản xuất ROS sau I/R. Enzyme NOX sử dụng oxy làm chất nhận điện tử cuối cùng thông qua các nhóm NADPH, FAD và heme. Các enzyme DUOX chủ yếu tạo ra hydro peroxide cùng với NOX-4, trong khi các isoenzym NOX còn lại chủ yếu tạo ra superoxide. NOX về cơ bản là không hoạt động và cần được kích thích tế bào để di chuyển vào màng và tạo ra ROS [16]. Trong I/R, phức hợp enzym này có thể được kích hoạt bởi một số chất trung gian hóa học do tế bào sản xuất và giải phóng, chẳng hạn như yếu tố ức chế thiếu oxy-1 (HIF-1 ) [18], phospholipase A2 [19], axit arachidonic [20], hệ thống bổ thể [21], các cytokine như TNF- và IL{17}} từ đại thực bào và tế bào mast [22].
Một nguồn ROS khác là NOS tách rời tạo ra oxit nitric (NO) bằng cách chuyển đổi L-arginine thành L-citrulline bằng cách sử dụng NADPH làm cơ chất khử và tetrahydrobiopterin (BH4) làm đồng yếu tố nhạy cảm với oxy hóa khử. Enzyme này, trong điều kiện thiếu oxy, có thể được chuyển đổi thành enzyme tạo O2- do nồng độ BH4 giảm, làm tăng tổn thương oxy hóa [23].
Hơn nữa, ty thể, bào quan tạo ra hầu hết năng lượng hóa học cần thiết để cung cấp năng lượng cho tế bào, góp phần sản xuất ROS thông qua quá trình khử hóa trị một của O2, chủ yếu do sự rò rỉ electron ở phức hợp I và -ketoglutarate dehydrogenase [24].
Trong quá trình thiếu máu cục bộ, sự thay đổi cấu trúc ty thể, tỷ lệ NADH/NAD+ cao và sự tích tụ chất chuyển hóa chu trình axit citric succinate làm trầm trọng thêm quá trình này [25,26].
Do đó, stress oxy hóa đóng một vai trò quan trọng trong việc gây tổn thương các cơ quan sau I/R bằng cách kích hoạt bệnh ferroptosis, hiện tượng chết tế bào do sắt gây ra, đặc trưng bởi sự tích tụ sắt, ROS quá mức và các sản phẩm peroxid hóa lipid, và giảm phân, sự thoái hóa có chọn lọc của ty thể bị tổn thương do quá trình tự thực bào

2. Ferroptosis: Vai trò trong chấn thương I/R ghép thận
Ferroptosis là một dạng chết tế bào được điều hòa do sự tích tụ sắt, peroxid hóa lipid và vỡ màng huyết tương sau đó [27]. Nó được đặc trưng chủ yếu bởi: nhân thiếu sự ngưng tụ chất nhiễm sắc, ty thể với thể tích và màng tế bào giảm, tế bào mở rộng đáng kể và vỡ màng sinh chất [28,29].
Trong bối cảnh I/R ở thận, sự tích lũy sắt, thông qua phản ứng Fenton, có thể tạo ra một lượng lớn ROS (cũng tăng lên do rối loạn chức năng ty thể đồng thời và hoạt động của họ NOX) có thể làm tăng nghiêm trọng stress oxy hóa nội bào và peroxid hóa lipid (Hình 1)
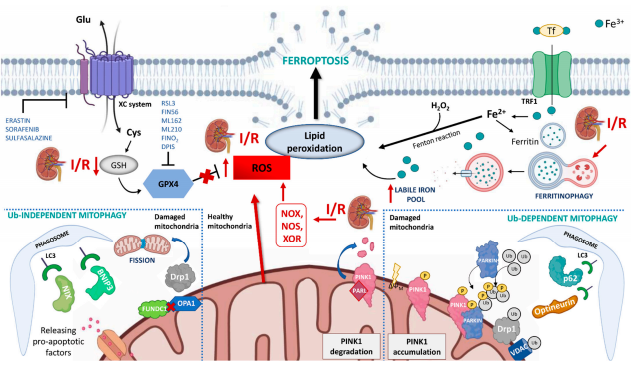
Hình 1. Sơ đồ trình bày các cơ chế của bệnh ferroptosis và bệnh thiểu năng trong tổn thương do thiếu máu cục bộ/tái tưới máu thận (I/R). Trong I/R, một số con đường góp phần gây ra bệnh ferroptosis: (i) sự sản xuất quá mức ROS bởi NADPH oxydase (NOX), nitric oxit synthase (NOS), xanthine oxyoreductase (XOR) và ty thể thúc đẩy quá trình peroxid hóa lipid và vỡ màng huyết tương; (ii) việc giảm hàm lượng glutathione (GSH) sẽ ức chế hoạt động của glutathione peroxidase 4 (GPX4) và tác dụng bảo vệ của nó chống lại quá trình peroxid hóa lipid màng; (iii) I/R có thể gián tiếp tạo ra ferritinophagy, nguyên nhân gây ra sự thoái hóa ferritin nội bào và làm tăng lượng sắt không ổn định nội bào. Mitophagy được kích hoạt trong I/R thông qua cả cơ chế phụ thuộc ubiquitin và độc lập với ubiquitin và dường như có vai trò bảo vệ trong tổn thương I/R bằng cách giảm giải phóng các loại oxy phản ứng từ ty thể bị rối loạn chức năng. Trong điều kiện sinh lý, PINK1 được nhập vào ty thể, nơi nó bị phân cắt bởi serine protease presenilin nội màng liên quan đến hình thoi (PARL) và cuối cùng bị thoái hóa. Khi ty thể bị tổn thương và mất đi tiềm năng màng tế bào, PINK1 sẽ tích tụ trên màng ngoài ty thể (MOM) và thu hút Parkin. Parkin phổ biến một số chất nền của ty thể như protein kênh chọn lọc anion phụ thuộc vào điện áp (VDAC) và protein giống thuốc nổ (DRP1). Những protein được phổ biến hóa này có thể tuyển dụng các thụ thể ty thể (chẳng hạn như optineurin, p62) liên kết ty thể với au tophagosome thông qua tương tác với LC3. Điều này gây ra sự nhấn chìm tự thực của cơ quan cần thiết cho sự thoái hóa của nó. Cơ chế độc lập với ubiquitin được điều chỉnh bởi các thụ thể nguyên phân định vị trên MOM, chẳng hạn như protein tương tác BCL2 3 (BNIP3), BNIP{18}}như (BNIP3L/NIX) và miền FUN14 chứa 1 (FUNDC1). Những protein này kết nối ty thể với autophagosome bằng cách tương tác trực tiếp với LC3.
Hai con đường có thể kích hoạt bệnh ferroptosis: con đường bên ngoài và con đường bên trong [27]. Con đường bên ngoài được bắt đầu thông qua sự ức chế chất trao đổi Cystine/glutamate của màng, cụ thể là hệ thống XC, làm trung gian cho sự xâm nhập của Cystine vào tế bào, được sử dụng để tổng hợp glutathione (GSH) [30], một đồng yếu tố được sử dụng bởi glutathione peroxidase 4 (GPX4) để loại bỏ peroxid lipid trong màng tế bào. Do đó, việc ức chế hệ thống XC gián tiếp làm giảm hoạt động của GPX4 dẫn đến sự tích tụ các peroxit lipid gây chết người và gây ra bệnh ferroptosis. Một số tác nhân như Elastin, sulfasalazine và sorafenib, bằng cách ngăn chặn hệ thống XC, có thể gây ra bệnh ferroptosis thông qua cơ chế này.
Con đường nội tại chủ yếu được gây ra bởi thuốc hoặc chất ức chế phân tử nhỏ như RSL3, ML162, ML210, FIN56 và FINO2 có thể ức chế trực tiếp hoặc gián tiếp hoạt động GPX4 [31]. Ngoài ra, các phân tử điều chỉnh sự hấp thu, dự trữ và sử dụng sắt (như ferritin, transferrin và lactotransferrin) có thể ảnh hưởng đến tình trạng ferroptosis bằng cách tăng mức độ sắt không ổn định (nguồn sắt tự do tương đối dễ tiếp cận đối với phản ứng Fenton) trong tế bào [32 ]. Transferrin và lactotransferrin là các protein chịu trách nhiệm vận chuyển sắt, liên kết với các thụ thể của chúng, làm trung gian đưa Fe vào tế bào chất. Ferritin là protein lưu trữ sắt nội bào có thể bị phân hủy bởi lysosome trong một quá trình gọi là ferritinophagy và làm tăng nồng độ sắt tự do do đó thúc đẩy quá trình ferroptosis [33] (Hình 1).
Ngược lại, các hệ thống enzyme và không enzyme (CoQ10, vitamin E, ferrostatin và lipproxstatin), cùng với hệ thống sửa chữa màng, ngăn chặn quá trình peroxid hóa lipid và bảo vệ tế bào khỏi bệnh ferroptosis [34–37].
Các nghiên cứu gần đây đã báo cáo rằng bệnh ferroptosis có thể liên quan đến con đường sinh lý bệnh liên quan đến chấn thương I/R [29,38].
Su và cộng sự. [39] đã chứng minh rằng pannexin 1, một kênh màng liên quan đến việc điều chỉnh giải phóng ATP dưới dạng phân tử DAMP có thể kích hoạt tín hiệu apoptosis hoặc autophagy trong điều kiện oxy hóa [40,41], có thể kích hoạt bệnh ferroptosis trong mô hình chuột bị tổn thương I/R ở thận [ 39]. Việc loại bỏ gen panx1 ở chuột bị I/R có liên quan đến mức tăng creatinine huyết thanh thấp hơn và giảm sự chết của tế bào ống thận cùng với giảm peroxid hóa lipid so với chuột hoang dã. Tác dụng bảo vệ này dường như được điều hòa bởi sự bất hoạt của con đường MAPK/ERK và sự điều chỉnh tăng của gen chống oxy hóa heme oxyase-1 (HO-1).
Tác dụng bảo vệ chống nhiễm sắt cũng có thể được phát huy nhờ hoạt động của Chất tăng cường tái tạo gan (ALR), một loại enzyme sulfhydryl oxydase được định vị trong không gian giữa các màng của ty thể. Enzyme này tham gia vào "hệ thống chuyển tiếp disulfide" làm trung gian cho việc nhập khẩu protein vào khoảng gian màng [42] và có đặc tính chống apoptotic và chống oxy hóa. Biểu hiện ALR đã tăng lên đáng kể ở chuột thiếu máu cục bộ và sử dụng ALR tái tổ hợp ở người, bằng cách tăng cường sự tăng sinh của tế bào ống thận và làm giảm quá trình chết theo chương trình của tế bào ống thận, làm giảm hiệu quả tổn thương ống thận và cải thiện tình trạng suy giảm chức năng thận [43,44].
Vai trò bảo vệ của ALR trong bệnh ferroptosis cũng có thể được điều hòa bằng cách giảm nồng độ ROS thông qua sự tương tác của nó với hệ thống GSH-GPX4 [45] và bằng cách thúc đẩy quá trình thanh thải ty thể bị tổn thương (một cơ chế gọi là ty thể) [46].
Do đó, kích hoạt ALR có thể là một chiến lược điều trị phòng ngừa khả thi trong tương lai đối với tổn thương do mảnh ghép giả do I/R gây ra.
3. Mitophagy: Một cầu thủ khác trong chấn thương I/R ghép thận
Ty thể bị hư hỏng hoặc rối loạn chức năng sẽ gây hại cho tế bào bằng cách tạo ra một lượng lớn ROS và giải phóng các yếu tố gây apoptotic. Vì vậy, việc loại bỏ kịp thời các bào quan này là rất quan trọng đối với cân bằng nội môi và khả năng tồn tại của tế bào [47].
Mitophagy là cơ chế thoái hóa có chọn lọc của ty thể bị tổn thương thông qua quá trình tự thực bào [48] được thực hiện bằng con đường phụ thuộc ubiquitin và không phụ thuộc vào ubiquitin. Cái trước được điều chỉnh bởi con đường kinase 1 (PINK1) -Parkin giả định do PTEN gây ra. PINK1 là một serine/threonine kinase của ty thể và Parkin là một ligase ubiquitin E3 tế bào. Trong điều kiện sinh lý, PINK1 được nhập vào ty thể, nơi nó bị phân cắt bởi serine protease presenilin nội màng liên quan đến hình thoi (PARL) và cuối cùng bị thoái hóa [49]. Khi ty thể bị tổn thương và mất đi tiềm năng màng tế bào, việc nhập khẩu PINK1 bị cản trở dẫn đến sự tích tụ kinase này ở màng ngoài ty thể (MOM). Sau đó, PINK1 tuyển dụng Parkin và kích hoạt hoạt động ligase của nó [50]. Parkin phổ biến một số chất nền của ty thể như Mitofusin 2 (Mfn2), protein kênh chọn lọc anion phụ thuộc vào điện áp (VDAC) và protein giống thuốc nổ (DRP1). Các protein được phổ biến hóa này có thể tuyển dụng các thụ thể ty thể (như optineurin, p62, NBR1) liên kết ty thể với autophagosome thông qua tương tác với LC3. Điều này gây ra sự nhấn chìm tự thực của cơ quan cần thiết cho sự thoái hóa của nó [49,51].
Cơ chế độc lập với ubiquitin được điều chỉnh bởi các thụ thể nguyên phân định vị trên MOM chẳng hạn như protein tương tác BCL2 3 (BNIP3), BNIP3-like (BNIP3L/NIX) và miền FUN14 chứa 1 (FUNDC1) [52,53] . Những protein này kết nối ty thể với autophagosome bằng cách tương tác trực tiếp với LC3 [54] (Hình 1).
Mitophagy cũng được điều hòa bởi các protein tham gia vào cơ chế hợp nhất và phân hạch của các bào quan này. Sự kết hợp dẫn đến một ty thể đơn lẻ được hình thành từ các cấu trúc độc lập trước đó [55], tạo ra các mạng lưới có màng liên tục và lòng ma trận [56]. Sự phân hạch tạo ra một hoặc nhiều bào quan con và, trong trường hợp tiềm năng màng ty thể giảm, sẽ phân tách cơ quan này để loại bỏ bằng cơ chế tự thực [56].

Sự phối hợp giữa phân hạch/hợp hạch và nguyên phân dường như được điều hòa bởi FUNDC1. Trong điều kiện sinh lý, thụ thể này neo giữ chứng teo quang GTPase 1 (OPA1) liên quan đến thuốc nổ về phía bề mặt bên trong của MOM. Để đối phó với căng thẳng của ty thể, việc tháo gỡ phức hợp FUNDC1–OPA1 và việc tuyển dụng Drp1 sẽ thúc đẩy quá trình phân hạch và ty thể [57].
Cơ chế tự thực đa yếu tố phức tạp và hấp dẫn này có thể đóng một vai trò bảo vệ trong các mảnh ghép giả kim đang trải qua chấn thương I / R. Sự thiếu hụt BNIP3 hoặc Pink1 và/hoặc Parkin trong mô hình chuột bị tổn thương I/R ở thận dẫn đến sự gia tăng sản xuất ROS, apoptosis và viêm ống kẽ thận [58–61]. Những tác động tương tự đạt được bằng cách ngăn chặn dòng thác nguyên phân bằng cách tác động lên các protein điều chỉnh quá trình phân hạch (ví dụ: Drp1) hoặc phản ứng tổng hợp (ví dụ: OPA1) [62,63]. Tác dụng bảo vệ của quá trình giảm phân đối với thận đang bị tổn thương I/R đã được quan sát thấy sau điều kiện tiên quyết do thiếu máu cục bộ [64], một thời gian ngắn tái tưới máu do thiếu máu cục bộ không gây chết người giúp bảo vệ cơ quan rắn chống lại tổn thương I/R kéo dài sau đó [65]. Việc tăng cường điều chỉnh quá trình giảm thiểu thông qua con đường PINK{13}}Parkin đã cải thiện chức năng của ty thể, giảm thiểu việc sản xuất ROS và tăng cường khả năng sống sót của tế bào [64]. Tất cả những phát hiện này cho thấy rằng quá trình giảm thiểu, bảo tồn chất lượng ty thể và sự sống sót của tế bào ống thận, có thể là một cơ chế bảo vệ có giá trị chống lại tổn thương I/R cần được thúc đẩy bằng các biện pháp can thiệp dược lý.
Dịch vụ hỗ trợ của Wecistanche-Nhà xuất khẩu cistanche lớn nhất ở Trung Quốc:
Email:wallence.suen@wecistanche.com
Whatsapp/Điện thoại:+86 15292862950
Mua sắm để biết thêm thông số kỹ thuật
https://www.xjcistanche.com/cistanche-shop






