Phần Một Di Truyền Bệnh Thận: Vai Trò Bất Ngờ Của Các Chứng Rối Loạn Hiếm Gặp
Jun 09, 2023
trừu tượng
Hàng trăm nguyên nhân di truyền khác nhau của bệnh thận mãn tính hiện đã được công nhận, và mặc dù hiếm gặp riêng lẻ, nhưng khi kết hợp với nhau, chúng là những nguyên nhân đáng kể gây ra tình trạng của cả người lớn và trẻ em. Các phương pháp tiếp cận di truyền học truyền thống chủ yếu dựa vào việc xác định các gia đình lớn có nhiều thành viên bị ảnh hưởng và là cơ sở để xác định các bệnh thận di truyền. Với việc sử dụng ngày càng nhiều trình tự song song ồ ạt và những cải tiến đối với việc loại bỏ kiểu gen, chúng ta có thể phân tích các biến thể hiếm gặp trong các nhóm lớn của các cá nhân không liên quan, dẫn đến việc chăm sóc bệnh nhân được cá nhân hóa và những tiến bộ nghiên cứu quan trọng. Đánh giá này đánh giá sự đóng góp của các rối loạn hiếm gặp đối với việc chăm sóc bệnh nhân và nghiên cứu về các bệnh thận di truyền, đồng thời nêu bật những tiến bộ quan trọng sử dụng các kỹ thuật mới để cải thiện khả năng xác định các mối liên quan giữa gen và bệnh mới.
từ khóa
bệnh thận di truyền, phân tích sụp đổ, y học chính xác, giải trình tự song song ồ ạt, bộ gen, bệnh thận mãn tính

Bấm vào đây để biếtlợi ích của Cistanche là gì
GIỚI THIỆU
Bệnh thận mãn tính (CKD) là một tình trạng phức tạp bao gồm nhiều bệnh riêng lẻ được đặc trưng bởi những bất thường về cấu trúc hoặc chức năng của thận (1). Trên toàn cầu, bệnh thận phổ biến, với tỷ lệ hiện mắc ước tính là 9%, và là nguyên nhân chính gây ra bệnh tật và tử vong (2). Tương tự như các bệnh thông thường khác, CKD có khả năng di truyền tương đối cao, với ước tính khả năng di truyền theo nghĩa rộng nằm trong khoảng từ 19% đến 54% tùy thuộc vào dấu ấn sinh học được sử dụng (3–5).
Genetic variation can be broadly dichotomized into common variants, present in more than 1% of the alleles of the population [a minor allele frequency (MAF) of >0.01] và các biến thể hiếm (MAF<0.01) (6–8). The role of common variants in kidney disease has been assessed using genome-wide association studies (GWAS), which have explained only 20% of an estimated 54% heritability in creatinine-based estimated glomerular filtration rate (4). On the other side of the spectrum, rare pathogenic variants are responsible for most Mendelian (monogenic) diseases. There are over 600 Mendelian forms of kidney disease, responsible for 50% of childhood-onset kidney disease; the majority of the causative variants are very rare or private within a specific family (9, 10). Although present at a lower frequency, Mendelian kidney diseases are identified in approximately 10% of adult patients, with the specific diagnostic yield of testing varying based on the individual's type of kidney disease, family history, age at onset, and extra-renal manifestations (11). Similar to pediatric cases, rare and private variants drive most diagnoses in adult cases. The data on the impact of rare disorders in CKD are now emerging and are consistent with analyses of other complex traits, which have demonstrated that a significant amount of missing heritability is explained by rare protein-altering variants that are not well captured by current genotyping and imputation techniques but can be analyzed using massively parallel sequencing of the exome (exome sequencing, ES) or genome (12, 13).
Các biến thể hiếm liên quan đến bệnh thận rất đa dạng về loại, di truyền, gen bị ảnh hưởng và kiểu hình lâm sàng. Ví dụ, các biến thể cấu trúc hiếm gặp và các biến thể về số lượng bản sao gen có liên quan đến sự phát triển của các dị tật bẩm sinh ở thận và đường tiết niệu (CAKUT), và các biến thể đơn nucleotide cũng như các phần chèn và xóa nhỏ (indels) có liên quan đến các bệnh về thận trên phổ kiểu hình (14, 15). Các biến thể soma hiếm gặp được cho là tác nhân thứ hai trong quá trình phát triển nang ở bệnh thận đa nang nhiễm sắc thể thường chiếm ưu thế (ADPKD) và là các biến thể điều khiển trong tạo máu vô tính có tiềm năng không xác định (CHIP), một tình trạng không ác tính liên quan đến tuổi tác có thể gây tăng nguy cơ suy thận và các biến chứng của CKD (16, 17). Các biến thể khảm hiếm gặp cũng ảnh hưởng đến mức độ nghiêm trọng của hội chứng Alport liên kết X, cho thấy sự phức tạp hơn nữa trong việc xác định ảnh hưởng của một biến thể (18).
Trong tổng quan này, chúng tôi mô tả vai trò của các biến thể hiếm gặp trong di truyền của bệnh thận. Chúng tôi xem xét vị trí trung tâm của chúng trong các nghiên cứu chẩn đoán, bao gồm cả ý nghĩa đối với việc chăm sóc bệnh nhân và việc sử dụng xét nghiệm di truyền trong tiên lượng và điều trị. Sau đó, chúng tôi khám phá các phương pháp điển hình được sử dụng để xác định và xác nhận các mối liên hệ biến thể hiếm gặp mới với bệnh tật. Chúng tôi kết luận với việc điều tra các tập dữ liệu lớn và tích hợp dữ liệu lâm sàng từ hồ sơ sức khỏe điện tử, mang đến cơ hội đánh giá tác động di truyền ở quy mô mà trước đây không thể thực hiện được.

chất bổ sung cistache
CÀI ĐẶT CHẨN ĐOÁN LÂM SÀNG
Bệnh thận di truyền là một thuật ngữ bao gồm hàng trăm rối loạn hiếm gặp với nguyên nhân di truyền đã được xác định. Cho đến nay, hơn 600 rối loạn đơn gen với kiểu hình thận và tiết niệu đã được xác định (Hình 1) (19). Hầu như tất cả các tình trạng di truyền này được phát hiện ở ít hơn 1 trên 2000 người, nhưng về tổng thể, chúng đại diện cho nguyên nhân phổ biến thứ năm gây suy thận (20). Trong khi một số rối loạn đơn gen chiếm phần lớn các trường hợp, các trường hợp còn lại là do một số lượng lớn các rối loạn hiếm gặp. Cái đuôi dài này trong sự phân bố các bệnh thận đơn gen có ý nghĩa quan trọng đối với các thuật toán chẩn đoán lâm sàng và các nỗ lực khám phá gen. Một số nghiên cứu chẩn đoán đã được thực hiện để xác định rõ hơn năng suất chẩn đoán và ý nghĩa lâm sàng của xét nghiệm di truyền ở các quần thể bệnh nhân mắc bệnh thận khác nhau. Một trong những phát hiện quan trọng trong các nghiên cứu này là phần lớn các biến thể gây bệnh được xác định là rất hiếm, với MAF tối đa (tối đa) nhỏ hơn 1 × 10–4 hoặc riêng tư trong một gia đình.

1. Tình trạng nhi khoa
Các bệnh di truyền ban đầu được cho là chủ yếu xảy ra ở trẻ em, vì vậy các nghiên cứu chẩn đoán trước đó tập trung vào việc đánh giá bệnh nhi (11, 21). Một nghiên cứu như vậy đã sử dụng ES để đánh giá 187 bệnh nhi mắc hội chứng thận hư kháng steroid và xác định nguyên nhân di truyền trong 49 (26%) trường hợp và 77 biến thể chẩn đoán (22). Điều thú vị là, bất chấp sự di truyền lặn của những điều kiện này, tất cả các biến thể đều cực kỳ hiếm; 32 (42 phần trăm ) không có trong tài liệu, 39 (51 phần trăm ) không có trong Exome Aggregation Consortium (ExAC) và 25 (32 phần trăm ) khác có MAF tối đa nhỏ hơn 1 × 10− 4. Một ngoại lệ là hội chứng thận hư kháng steroid ở trẻ em do các biến thể trong NPHS2 gây ra, đây là một ví dụ thú vị về sự tương tác của các biến thể phổ biến và hiếm gặp trong bệnh. NPHS2 p.R229Q là biến thể gây bệnh được xác định phổ biến nhất trong quần thể bệnh nhân này, với MAF tối đa trong ExAC là 0.029. Tuy nhiên, biến thể NPHS2 p.R229Q không gây bệnh khi xuất hiện ở trạng thái đồng hợp tử và chỉ gây bệnh khi kết hợp với một số biến thể NPHS2 hiếm gặp khác (23). Trong nghiên cứu được trích dẫn, các biến thể có hại được tìm thấy trong quá trình chuyển đổi sang NPHS2 p.R229Q ở những người bị ảnh hưởng luôn hiếm gặp và thường là riêng tư, trong đó NPHS2 p.E264Q là biến thể phổ biến nhất trong ExAC, có MAF tối đa là 0,003. Tương tự, việc đánh giá nguyên nhân di truyền của CAKUT ở 232 họ đã xác định được 32 biến thể gây bệnh khác nhau trong 32 trường hợp (14 phần trăm ) ảnh hưởng đến 22 gen với 16 (50 phần trăm ) biến thể này không có trong tài liệu và 28 (88 phần trăm ) rất hiếm hoặc không có từ Cơ sở dữ liệu tổng hợp bộ gen (gnomAD) (24).
2. Mở rộng cho bệnh nhân người lớn
ES đã được sử dụng để đánh giá các nhóm bệnh nhân mắc bệnh thận đa dạng, bao gồm cả những người mắc bệnh khởi phát ở người trưởng thành. Nghiên cứu lớn nhất bao gồm 3.315 người mắc CKD do mọi nguyên nhân, trong đó 2.144 người bị suy thận và 2.837 người trưởng thành khi tham gia nghiên cứu (15). Nghiên cứu này đã xác định chẩn đoán phân tử ở 307 cá nhân (9,1 phần trăm ) dẫn đến chẩn đoán 66 bệnh thận Mendel khác nhau. Nghiên cứu đã xác định 343 biến thể chẩn đoán, trong đó 340 99 phần trăm ) rất hiếm trong gnomAD. Hầu hết các biến thể đều rất hiếm, với MAF tối đa nhỏ hơn 1 × 10−4 (n=84, 24 phần trăm ) hoặc riêng tư (n=229, 67 phần trăm ) (Hình 2a).

3. Tác động của chẩn đoán di truyền
Một trong những phát hiện quan trọng của các nghiên cứu chẩn đoán là hầu hết các chẩn đoán di truyền đều ảnh hưởng trực tiếp đến việc chăm sóc bệnh nhân, ngay cả với số lượng hạn chế các phương pháp điều trị nhắm mục tiêu hiện có. Groopman và cộng sự. (15) phát hiện ra rằng chẩn đoán di truyền dẫn đến tác động lâm sàng trong 89% trường hợp, bao gồm 76% trường hợp nghi ngờ mắc bệnh thận di truyền trước khi xét nghiệm. Những tác động lâm sàng này đã được đánh giá hồi cứu và nằm trong phạm vi từ thông báo tiên lượng đến thay đổi quyết định cấy ghép và điều trị. Điều quan trọng là chẩn đoán di truyền ở bệnh nhân CKD không rõ nguyên nhân đã làm rõ nguyên nhân của bệnh thận trong mọi trường hợp, mang ý nghĩa tiên lượng cho 77% , bắt đầu chăm sóc chuyên khoa mục tiêu cho 77% và thay đổi liệu pháp cho 62%. Dữ liệu triển vọng hỗ trợ tiện ích lâm sàng của xét nghiệm di truyền cho bệnh thận gần đây đã được công bố trên 204 bệnh nhân nghi ngờ mắc bệnh thận di truyền đã trải qua ES. Một tác động lâm sàng trực tiếp đã được báo cáo đối với 47 (59 phần trăm) mẫu thử có chẩn đoán di truyền và 73 (91 phần trăm) gia đình (25). Các tác động lâm sàng bao gồm ngăn chặn 10 ca sinh thiết thận, thay đổi kế hoạch điều trị trong 16 trường hợp và thay đổi giám sát trong 35 trường hợp một lần nữa được thúc đẩy bởi các biến thể hiếm gặp (Hình 2b).

chiết xuất hạt dẻ cười
4. Tiên lượng
Sự thay đổi trong biểu hiện lâm sàng của các dạng di truyền của bệnh thận đã làm phức tạp việc cung cấp thông tin tiên lượng cho bệnh nhân, ngay cả khi nguyên nhân di truyền được xác định. Ngoài ra, phần lớn các biến thể gây bệnh liên quan đến bệnh thận là rất hiếm hoặc riêng tư trong một gia đình, điều này hạn chế khả năng đưa ra tiên lượng dựa trên các biến thể của từng cá nhân. Tuy nhiên, mối tương quan giữa kiểu gen và kiểu hình đã là một phần của di truyền học người kể từ khi bắt đầu, thường sử dụng các đặc điểm biến thể có thể khái quát hóa như loại tác động lên protein, tính chất của axit amin bị thay đổi hoặc vị trí của biến thể trong protein. Trong thận học, hai ứng dụng trưởng thành nhất của phương pháp này là xem xét hội chứng ADPKD và Alport. Đối với bệnh nhân mắc ADPKD, hệ thống tính điểm PROPKD (dự đoán kết quả thận trong bệnh thận đa nang) đã được phát triển và xác nhận để dự đoán tuổi trung bình của một cá nhân khi bị suy thận bằng cách tích hợp dữ liệu lâm sàng và biến thể (26). Các biến thể cắt bớt trong PKD1 có nguy cơ suy thận cao nhất, tiếp theo là các biến thể PKD1 không cắt ngắn, sau đó là các biến thể trong PKD2, và cũng có vẻ như việc chèn và xóa trong khung không cắt ngắn trong PKD1 làm thay đổi độ dài protein có rủi ro cao hơn các biến thể sai nghĩa ( 27). Tương tự như vậy, đối với những bệnh nhân mắc hội chứng Alport, các biến thể vô nghĩa mang tiên lượng nặng nhất trong khi các biến thể nối và tên lửa lần lượt biểu hiện các kiểu hình trung bình và nhẹ. Các yếu tố khác như vị trí của biến thể trong gen, vị trí của nó so với sự gián đoạn không tạo collagen và axit amin thay thế cũng đã được chứng minh là có ảnh hưởng đến tiên lượng của bệnh nhân (28–30). Các công cụ trong tương lai cũng có thể bao gồm thông tin dự đoán từ cả biến thể phổ biến và biến thể hiếm để cải thiện sức mạnh của chúng (31). Sự sẵn có của các tập dữ liệu lớn hơn sẽ cho phép tích hợp nhiều biến thể hơn và lý tưởng nhất là các họ khác biệt hơn với cùng các biến thể, vào việc phát triển các công cụ tiên lượng mạnh mẽ để cho phép dự đoán tốt hơn. Những công cụ như vậy có thể tác động đáng kể đến các thử nghiệm lâm sàng, vì những người tham gia có thể được phân tầng dựa trên sự tiến triển dự kiến của bệnh của họ.

thuốc trị rạn da
5. Điều trị
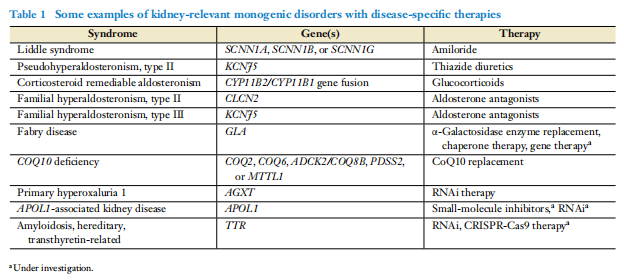
Các nghiên cứu chẩn đoán đã chỉ ra rằng việc chẩn đoán di truyền có thể có tác động trực tiếp đến việc điều trị (Bảng 1). Các ví dụ bao gồm việc sử dụng bổ sung coenzym Q10 (CoQ10) liều cao cho bệnh nhân mắc hội chứng thận hư và các biến thể chẩn đoán trong lộ trình CoQ10 (COQ2, COQ6, ADCK2/COQ8B, PDSS2, MTTL1) và việc sử dụng chất ức chế xanthine oxidase cho bệnh nhân APRT thiếu hụt (adenine phosphoribosyltransferase) (32, 33). Chẩn đoán di truyền có thể hạn chế tiếp xúc với các phương pháp điều trị không hiệu quả; ví dụ, khi xác định được nguyên nhân di truyền của hội chứng thận hư, thuốc ức chế miễn dịch thường không được sử dụng, vì phần lớn các trường hợp mắc hội chứng thận hư do di truyền sẽ không đáp ứng và những phương pháp điều trị này có rủi ro đáng kể (34). Các nghiên cứu trong tương lai nên đánh giá lợi ích của việc tránh các tác dụng phụ, chẳng hạn như giảm nguy cơ nhiễm trùng và ung thư do hạn chế ức chế miễn dịch do xét nghiệm di truyền. Hơn nữa, khả năng phát hiện những bệnh nhân mắc các bệnh đơn gen chưa được chẩn đoán có thể giúp phân tầng rủi ro trong các thử nghiệm lâm sàng để tối ưu hóa sức mạnh và giảm khả năng tiếp xúc với các tác dụng phụ.
Mục tiêu cuối cùng là phát triển các phương pháp điều trị chữa bệnh. Một trong những ví dụ tiên tiến nhất trong thận học là ứng dụng liệu pháp gen cho bệnh Fabry (35). Bệnh Fabry gây ra bởi hơn 1,000 biến thể khác nhau trong gen GLA, hầu hết rất hiếm gặp hoặc riêng lẻ, dẫn đến giảm hoạt động -galactosidase A và tích tụ glycosphingolipids (36). Phương pháp điều trị tiêu chuẩn cho bệnh này là liệu pháp thay thế enzyme (ERT), đòi hỏi phải truyền dịch thường xuyên và có thể dẫn đến các kháng thể kháng thuốc hạn chế điều trị. Tuy nhiên, trong một nghiên cứu về độ an toàn của phi công, năm nam giới mắc bệnh Fabry cổ điển do các biến thể tên lửa rất hiếm gặp đã được điều trị ổn định bằng ERT đã được điều trị bằng liệu pháp gen (35). Họ đã trải qua liệu pháp gen ex vivo qua trung gian lentilvirus, trong đó tế bào gốc/tế bào tiền thân tạo máu được tải nạp gen GLA chức năng, sau đó được đưa vào lại thông qua cấy ghép tế bào gốc tạo máu tự thân. Những bệnh nhân này đã chứng minh sự bình thường hóa bền vững hoạt tính của bạch cầu -galactosidase A và mức glycosphingolipid ổn định cho phép ba người (60 phần trăm ) trong số họ ngừng ERT, với hồ sơ tác dụng phụ hợp lý. Nghiên cứu này cho chúng tôi hy vọng rằng với sự cải tiến hơn nữa, các phương pháp điều trị chữa bệnh có thể sẵn có cho nhiều bệnh nhân hơn.
Bệnh Fabry cũng cung cấp các ví dụ thú vị khác về liệu pháp cá nhân hóa, bao gồm liệu pháp đi kèm và quyết định điều trị cho bệnh nhân nữ. Một cơ chế phổ biến của bệnh trong tình trạng này là sự vận chuyển protein bị thay đổi dẫn đến giảm hoạt động của enzyme. Migalastat là một phân tử chaperone phục hồi chức năng enzyme và cho thấy hiệu quả lâm sàng tương tự như ERT ở 35–50% cá nhân có biến thể có thể điều chỉnh được nhưng không có tác dụng ở những cá nhân có biến thể không thể đặt tên (37, 38). Tính đặc hiệu của biến thể này làm cho xét nghiệm di truyền trở thành một bước quan trọng trong việc tối ưu hóa liệu pháp cho bệnh nhân mắc bệnh Fabry. Từ lâu, người ta đã nghĩ rằng do bản chất liên kết với X của bệnh, phụ nữ là những người mang mầm bệnh không bị ảnh hưởng; tuy nhiên, hiện nay rõ ràng là nhiều phụ nữ bị ảnh hưởng và có sự tương tác phức tạp giữa các đặc điểm biến thể cụ thể và sự bất hoạt X bị lệch dẫn đến các biểu hiện lâm sàng rất không đồng nhất (39). Điều này đã làm phức tạp quyết định về thời điểm và cách điều trị bệnh nhân nữ mắc bệnh Fabry, vì một số cá nhân được hưởng lợi từ liệu pháp nhưng chúng tôi thiếu các công cụ để dự đoán phản ứng trước khi bệnh nhân có triệu chứng, làm nổi bật một lĩnh vực cần nghiên cứu thêm.

bột hồ đào
Các liệu pháp nhắm mục tiêu khác đang có sẵn cho bệnh nhân mắc bệnh thận di truyền, sử dụng các kỹ thuật mới như can thiệp RNA (RNAi), antisense-oligonucleotides (ASO) và CRISPR-Cas9. RNAi đã cho thấy nhiều hứa hẹn trong việc điều trị các bệnh thận di truyền, với các thử nghiệm tích cực ở giai đoạn III sử dụng patisiran để điều trị bệnh amyloidosis transthyretin di truyền do các biến thể TTR và lumasiran để điều trị chứng tăng oxy máu nguyên phát loại 1 do các biến thể AGT (40, 41). Những phương pháp điều trị này đã được thiết kế để không biến đổi, cho phép chúng được sử dụng để điều trị cho những người mắc nhiều biến thể hiếm gặp khác nhau. CRISPR-Cas9 đã được nghiên cứu trong một nhóm nhỏ những người mắc bệnh amyloidosis transthyretin và được chứng minh là làm giảm sản xuất TTR huyết thanh thông qua việc loại bỏ gen mục tiêu bằng kỹ thuật phân phối in vivo (42). Phương pháp điều trị ASO bỏ qua exon đối với các biến thể COL4A5 bị cắt ngắn đã được chứng minh ở chuột để tạo ra những cải thiện về mặt lâm sàng và mô học bằng cách thay đổi hiệu ứng protein thành quá trình xóa exon trong khung (43). Điều này có thể trở thành một lựa chọn điều trị cho những bệnh nhân mắc nhiều biến thể COL4A5 cắt ngắn hiếm gặp thường gây bệnh nặng nhưng vẫn chưa được nghiên cứu ở người. Các phương pháp điều trị bệnh thận liên quan đến APOL1-bao gồm sử dụng phương pháp điều trị ASO để giảm biểu hiện APOL1 và sử dụng chất ức chế phân tử nhỏ của APOL1 để giảm chức năng của nó (44). Những liệu pháp nhắm mục tiêu và cá nhân hóa này có khả năng được áp dụng cho các bệnh di truyền khác nhau và mang đến cho bệnh nhân của chúng tôi hy vọng về các phương pháp điều trị tốt hơn trong tương lai.
NGƯỜI GIỚI THIỆU
1. Levin A, Stevens PE, Bilous RW, et al. 2013. Bệnh thận: Cải thiện kết quả toàn cầu (KDIGO) Nhóm công tác CKD. Hướng dẫn thực hành lâm sàng KDIGO 2012 để đánh giá và quản lý bệnh thận mãn tính. Thận Int. bổ sung 3(1):1–150
2. Bikbov B, Purcell CA, Levey AS, et al. 2020. Gánh nặng bệnh thận mãn tính toàn cầu, khu vực và quốc gia, 1990–2017: phân tích có hệ thống cho Nghiên cứu Gánh nặng Bệnh tật Toàn cầu 2017. Lancet 395(10225):709–33
3. Arpegård J, Viktorin A, Chang Z, et al. 2015. So sánh khả năng di truyền của cystatin C- và ước tính chức năng thận dựa trên creatinine và mối quan hệ của chúng với khả năng di truyền của bệnh tim mạch. Mứt. Tim PGS. 4(1):e001467
4. Wuttke M, Li Y, Li M, et al. 2019. Một danh mục các cơ địa di truyền liên quan đến chức năng thận từ các phân tích của một triệu cá nhân. tự nhiên gien. 51(6):957–72
5. Zhang J, Thio CHL, Gansevoort RT, et al. 2021. Tập hợp gia đình của CKD và khả năng di truyền của các dấu ấn sinh học thận trong dân số nói chung: Nghiên cứu đoàn hệ Lifelines. Là. J. Thận Dis. 77(6):869–78
6. Karczewski KJ, Francioli LC, Tiao G, et al. 2020. Phổ giới hạn đột biến được định lượng từ sự biến đổi ở 141.456 người. Thiên nhiên 581(7809):434–43
7. Lek M, Karczewski KJ, Minikel EV, et al. 2016. Phân tích biến thể di truyền mã hóa protein ở 60.706 người. Tự nhiên 536(7616):285–91
8. Dự án 1000 bộ gen. phối ngẫu. 2015. Một tài liệu tham khảo toàn cầu về biến thể di truyền của con người. Tự nhiên 526(7571):68–74
9. Ars E, Ballarin J, Ruiz P, et al. 2011. Tiện ích lâm sàng của xét nghiệm di truyền ở trẻ em và người lớn mắc hội chứng thận hư kháng steroid. lâm sàng. Mứt. Sóc. Nephrol. 6(5):1139–48
10. Wühl E, van Stralen KJ, Wanner C, et al. 2014. Liệu pháp thay thế thận cho các bệnh hiếm gặp ảnh hưởng đến thận: phân tích Cơ quan đăng ký ERA-EDTA. Nephrol. Chạy thận nhân tạo. 29(Bổ sung 4):iv1–8
11. Cocchi E, Nestor JG, Gharavi AG. 2020. Sàng lọc di truyền lâm sàng ở bệnh nhân trưởng thành mắc bệnh thận. lâm sàng. Mứt. Sóc. Nephrol. 15(10):1497–510
12. Génin E. 2020. Mất khả năng di truyền của các bệnh phức tạp: trường hợp được giải quyết? Hum Genet. 139(1):103–13
13. Wainschtein P, Jain D, Zheng Z, et al. 2022. Đánh giá sự đóng góp của các biến thể hiếm vào khả năng di truyền tính trạng phức tạp từ dữ liệu trình tự toàn bộ bộ gen. tự nhiên gien. 54(3):263–73
14. Verbitsky M, Westland R, Perez A, et al. 2019. Bối cảnh biến đổi số lượng bản sao của dị tật bẩm sinh thận và đường tiết niệu. tự nhiên gien. 51(1):117–27
15. Groopman EE, Marasa M, Cameron-Christie S, et al. 2018. Tiện ích chẩn đoán của giải trình tự exome cho bệnh thận. N. Anh. J. Med. 380(2):142–51
16. Tan AY, Zhang T, Michael A, et al. 2018. Đột biến soma ở biểu mô nang thận trong bệnh thận đa nang trội nhiễm sắc thể thường. Mứt. Sóc. Nephrol. 29(8):2139–56
17. Vlasschaert C, McNaughton AJM, Chong M, et al. 2022. Hiệp hội tạo máu vô tính có tiềm năng không xác định với chức năng thận kém hơn và thiếu máu ở hai nhóm bệnh nhân mắc bệnh thận mãn tính tiến triển. Mứt. Sóc. Nephrol. 33(5):985–95
18. Fu XJ, Nozu K, Kaito H, et al. 2016. Chủ nghĩa khảm soma và tần số biến thể được phát hiện bằng giải trình tự thế hệ tiếp theo trong hội chứng Alport liên kết X. Ơ. J. Hừm. gien. 24(3):387–91
19. Rasouly HM, Groopman EE, Heyman-Kantor R, et al. 2019. Gánh nặng của các biến thể gây bệnh ứng cử viên cho các rối loạn thận và sinh dục tiết niệu phát sinh từ giải trình tự exome. Ann. thực tập sinh. y tế. 170(1):11–21
20. Devuyst O, Knoers NVAM, Remuzzi G, et al. 2014. Bệnh thận di truyền hiếm gặp: thách thức, cơ hội và triển vọng. Lancet 383(9931):1844–59
21. Ingelfinger JR, Kalantar-Zadeh K, Schaefer F, et al. 2016. Ngăn chặn di chứng của bệnh thận—tập trung vào thời thơ ấu. Thận Dis. 2(1):46–52
22. Bierzynska A, McCarthy HJ, Soderquest K, et al. 2017. Hồ sơ bộ gen và lâm sàng của đoàn hệ quốc gia về hội chứng thận hư ủng hộ cách tiếp cận y học chính xác để quản lý bệnh. Thận Int. 91(4):937–47
23. Mikó Á, Menyhárd DK, Kaposi A, et al. 2018. Khả năng gây bệnh phụ thuộc đột biến của NPHS2 p.R229Q: hướng dẫn đánh giá lâm sàng. Hừm. đột biến. 39(12):1854–60
24. van der Ven AT, Connaughton DM, Ityel H, et al. 2018. Giải trình tự toàn bộ exome xác định các đột biến nguyên nhân trong các gia đình có dị tật bẩm sinh ở thận và đường tiết niệu. Mứt. Sóc. Nephrol. 29(9):2348–61
25. Jayasinghe K, Stark Z, Kerr PG, et al. 2021. Tác động lâm sàng của xét nghiệm bộ gen ở những bệnh nhân nghi ngờ mắc bệnh thận đơn gen. gien. y tế. 23:183–91
26. Cornec-Le Gall E, Audrézet MP, Rousseau A, et al. 2016. Điểm số PROPKD: một thuật toán mới để dự đoán tỷ lệ sống sót của thận trong bệnh thận đa nang nhiễm sắc thể thường chiếm ưu thế. Mứt. Sóc. Nephrol. 27(3):942–51
27. Hwang YH, Conklin J, Chan W, et al. 2016. Tinh chỉnh mối tương quan kiểu gen-kiểu hình trong bệnh thận đa nang trội nhiễm sắc thể thường. Mứt. Sóc. Nephrol. 27(6):1861–68
28. Gibson JT, Huang M, Shenelli Croos Cabrera M, et al. 2022. Mối tương quan giữa kiểu gen-kiểu hình đối với các biến thể COL4A3–COL4A5 dẫn đến sự thay thế Gly trong hội chứng Alport. Khoa học. Dân biểu 12:2722
29. Yamamura T, Horinouchi T, Nagano C, et al. 2020. Mối tương quan kiểu gen-kiểu hình ảnh hưởng đến đáp ứng với thuốc nhắm mục tiêu angiotensin ở bệnh nhân Nhật Bản mắc hội chứng Alport liên kết với nhiễm sắc thể giới tính nam. Thận Int. 98(6):1605–14
30. Bekheirnia MR, Reed B, Gregory MC, et al. 2010. Tương quan kiểu gen-kiểu hình trong hội chứng Alport liên kết X. Mứt. Sóc. Nephrol. 21(5):876–83
31. Fahed AC,Wang M,Homburger JR, et al. 2020. Nền tảng đa gen điều chỉnh sự xâm nhập của các biến thể đơn gen đối với các điều kiện gen cấp 1. tự nhiên cộng đồng. 11(1):3635
32. Wang N, Zheng Y, Zhang L, et al. Năm 2022. Một họ phân biệt tình trạng thiếu coenzyme Q10 sơ cấp gây chết người do hai biến thể COQ6 mới. Đằng trước. gien. 12:811833
33. Bollée G, Harambat J, Bensman A, et al. 2012. Thiếu adenine phosphoribosyltransferase. lâm sàng. Mứt. Sóc. Nephrol. 7(9):1521–27
34. Kemper MJ, Lemke A. 2018. Điều trị các dạng di truyền của hội chứng thận hư. Đằng trước. trẻ em 6:72
35. Khan A, Thợ cắt tóc DL, Huang J, et al. 2021. Liệu pháp gen qua trung gian lentillin cho bệnh Fabry. tự nhiên cộng đồng. 12(1):1178
36. McCafferty EH, Scott LJ. 2019. Migalastat: đánh giá về bệnh Fabry. Thuốc 79(5):543–54
37. Hughes DA, Nicholls K, Shankar SP, et al. 2017. Thuốc uống chaperone migalastat so với liệu pháp thay thế enzyme trong bệnh Fabry: 18-kết quả tháng từ nghiên cứu ATTRACT ngẫu nhiên giai đoạn III. J. Med. gien. 54(4):288–96
38. Germain DP, Hughes DA, Nicholls K, et al. 2016. Điều trị bệnh Fabry bằng dược chất chaperone migalastat. N. Anh. J. Med. 375(6):545–55
39. Germain DP, Arad M, Burlina A, et al. 2019. Hiệu quả của liệu pháp thay thế enzyme đối với kết quả lâm sàng ở bệnh nhân nữ mắc bệnh Fabry—một tổng quan tài liệu có hệ thống của một hội đồng chuyên gia châu Âu. mol. gien. Metab. 126(3):224–35
40. Adams D, Gonzalez-Duarte A, O'Riordan WD, et al. 2018. Patisiran, một liệu pháp RNAi, cho bệnh amyloidosis transthyretin di truyền. N. Anh. J. Med. 379(1):11–21
41. Garrelfs SF, Frishberg Y, Hulton SA, et al. 2021. Lumasiran, một liệu pháp RNAi cho chứng tăng oxy máu nguyên phát loại 1. N. Engl. J. Med. 384(13):1216–26
42. Gillmore JD, Gane E, Taubel J, et al. 2021. Chỉnh sửa gen CRISPR-Cas9 in vivo cho bệnh amyloidosis transthyretin. N. Anh. J. Med. 385(6):493–502
43. Yamamura T, Horinouchi T, Adachi T, et al. Năm 2020. Phát triển liệu pháp bỏ qua exon cho hội chứng Alport liên kết X với các biến thể cắt ngắn trong COL4A5. tự nhiên cộng đồng. 11(1):2777
44. Daneshpajouhnejad P, Kopp JB, Winkler CA, et al. 2022. Câu chuyện tiến triển của bệnh thận apolipoprotein L1: kết thúc của sự khởi đầu. tự nhiên Mục sư Nephrol. 18(5):307–20
Mark D. Elliott,1,2,3 Hila Milo Rasouly,1,2 và Ali G. Gharavi1,2,3
1 Division of Nephrology, Department of Medicine, Columbia University Vagelos College of Physicians and Surgeons, New York, NY, USA; email: ag2239@columbia.edu
2 Trung tâm Y học Chính xác và Bộ gen, Khoa Y, Đại học Columbia Đại học Bác sĩ và Bác sĩ phẫu thuật, New York, NY, Hoa Kỳ
3 Viện Y học Bộ gen, Đại học Columbia Đại học Bác sĩ và Bác sĩ phẫu thuật Vagelos, New York, NY, Hoa Kỳ






